よむ、つかう、まなぶ。
参考資料2:臨床研究中核病院概要 (59 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第35回 8/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
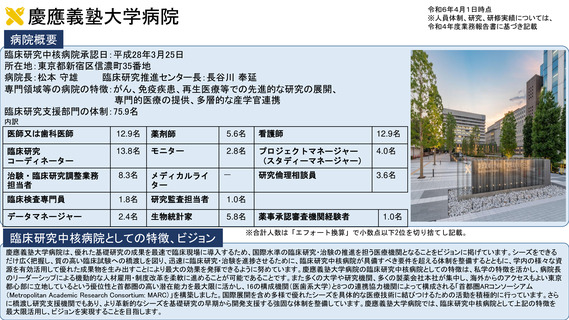
先進医療への対応
当院医事課内に先進医療に係る通知、流れ、申請書式等についての整備をしており、臨床研究センターとも協力しながら、研究者への支援
体制を運用している。
患者申出療養への対応
臨床研究センター治験ユニットに患者申出療養の患者相談窓口を設置し、患者、医師、その他医療関係者からの問い合わせに対応している。
申出内容に対する情報収集、臨床試験における効果の科学的妥当性、安全性などについて、適宜関連診療科や関係部門と連携しながら検
討を行い、円滑に計画、実施するための体制を整備している。
国際共同臨床研究・治験の実施状況
2023年度契約中の治験についての国際共同治験の実施数
企業治験 : 146件中、国際共同治験 104件 / 医師主導治験 : 14件中、国際共同治験(他施設主幹) 1件
企業治験における国際共同治験数の割合は、年々、増加傾向にある。
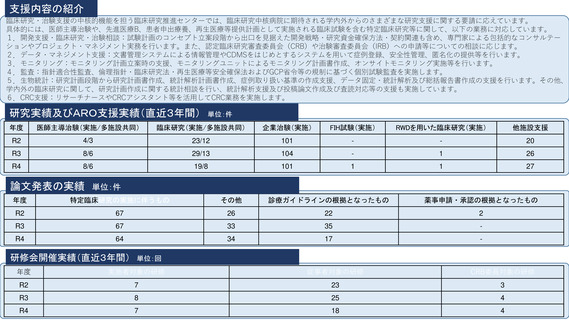
ベンチャー企業への支援実施状況
長崎大学では、研究推進機構、創薬イノベーションセンター、病院臨床研究センターが連携して共同支援を行うことで、研究開発初期から事
業化・臨床試験まで、シームレスに支援を行う体制を整備している。学内外の研究者へのアカデミア創薬についての啓発活動、MEDISO利活
用の促進や利用支援、ジャパン・ヘルスケアベンチャー・サミット参加支援などを行っている。
当院医事課内に先進医療に係る通知、流れ、申請書式等についての整備をしており、臨床研究センターとも協力しながら、研究者への支援
体制を運用している。
患者申出療養への対応
臨床研究センター治験ユニットに患者申出療養の患者相談窓口を設置し、患者、医師、その他医療関係者からの問い合わせに対応している。
申出内容に対する情報収集、臨床試験における効果の科学的妥当性、安全性などについて、適宜関連診療科や関係部門と連携しながら検
討を行い、円滑に計画、実施するための体制を整備している。
国際共同臨床研究・治験の実施状況
2023年度契約中の治験についての国際共同治験の実施数
企業治験 : 146件中、国際共同治験 104件 / 医師主導治験 : 14件中、国際共同治験(他施設主幹) 1件
企業治験における国際共同治験数の割合は、年々、増加傾向にある。
ベンチャー企業への支援実施状況
長崎大学では、研究推進機構、創薬イノベーションセンター、病院臨床研究センターが連携して共同支援を行うことで、研究開発初期から事
業化・臨床試験まで、シームレスに支援を行う体制を整備している。学内外の研究者へのアカデミア創薬についての啓発活動、MEDISO利活
用の促進や利用支援、ジャパン・ヘルスケアベンチャー・サミット参加支援などを行っている。