よむ、つかう、まなぶ。
資料1-2:日本CRO協会 提出資料 (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46147.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第38回 11/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
臨床研究中核病院への期待 (CROとしての視点で)
臨床研究中核病院
我が国の国際水準の臨床研究や医師主導治験の中心的役割を担う拠点
◼
◼
◼
◼
◼
◼
◼
◼
◼
◼
◼
人材育成のための集中投資が行われ、専門性が高い人員が豊富なこと
人員に対し、専門性と実績に相応しいインセンティブが用意されていること
初期フェーズ(First in Human試験を含む)の臨床試験実施体制が整備されていること
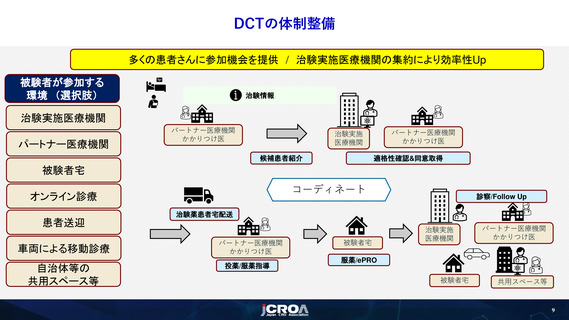
必要に応じてDCTが可能なこと(パートナー医療機関との連携含む)
治験や臨床研究の症例集積性が優れていること(1プロトコールあたりの症例数)
手続きや準備のスピードが速いこと
共同IRBを利用できること
共通書式を利用できること
かなりの部分で英語対応が可能なこと
FMV/BMCによる治験費用算定ができること
リモートアクセスモニタリングが可能なこと
18
臨床研究中核病院
我が国の国際水準の臨床研究や医師主導治験の中心的役割を担う拠点
◼
◼
◼
◼
◼
◼
◼
◼
◼
◼
◼
人材育成のための集中投資が行われ、専門性が高い人員が豊富なこと
人員に対し、専門性と実績に相応しいインセンティブが用意されていること
初期フェーズ(First in Human試験を含む)の臨床試験実施体制が整備されていること
必要に応じてDCTが可能なこと(パートナー医療機関との連携含む)
治験や臨床研究の症例集積性が優れていること(1プロトコールあたりの症例数)
手続きや準備のスピードが速いこと
共同IRBを利用できること
共通書式を利用できること
かなりの部分で英語対応が可能なこと
FMV/BMCによる治験費用算定ができること
リモートアクセスモニタリングが可能なこと
18