よむ、つかう、まなぶ。
別紙1○【先進医療合同会議】先進医療Bに係る新規技術の科学的評価等について (15 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00053.html |
| 出典情報 | 先進医療会議(第117回先進医療会議、第142回先進医療技術審査部会 12/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
先進医療審査の事前照会事項に対する回答4
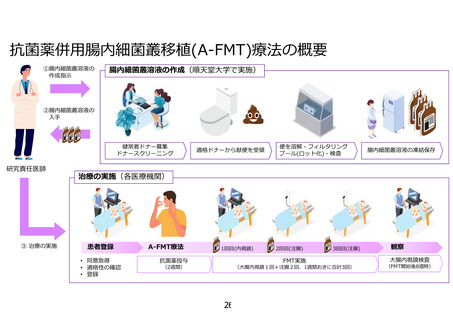
先進医療技術名: 抗菌薬併用腸内細菌叢移植療法(A-FMT 療法)
2022 年 11 月 30 日
所属・氏名: 順天堂大学医学部附属順天堂医院 消化器内科 永原章仁
1.研究計画書 10.個々の研究対象者における中止基準 について、照会事項 2-2 への回答①②に
ついて確認いたしました。③8 週時に MMDAI が評価されなかった症例に係る主要評価の取扱いに
ついて、につきまして以下の回答がなされております。
「8 週時に MMDAI が評価されなかった症例において、8 週時より前に MMDAI の評価に基づいて寛解
が確認できた症例は寛解として扱い、それ以外の場合において 8 週時に MMDAI が評価されていな
い症例は非寛解として扱います(回答②のケース)。ただし、8 週時に MMDAI が評価されておらず、
それ以降に MMDAI が評価された症例については、中央評価委員会にて症例の取扱いを検討する
予定です。」
下線部につきまして、8 週時に設定されている許容範囲は±14 日でございますが、許容範囲外(特
に-14 日以前)に MMDAI が評価され、寛解と判断された場合に、その症例を寛解として扱う適切性
についてご回答ください。なお、3.4.1 の主要評価項目の設定根拠では「A-FMT によるUCへの治療
効果を評価するには、これまでの順天堂大学の A-FMT の実績より FMT 治療開始 6 週時以降が適
している」との記載もあり、それを踏まえて主要評価項目で寛解と判断可能な許容範囲についての
検討が必要かと考えますが、いかがでしょうか。
【回答】
ご指摘ありがとうございます。本研究では A-FMT 療法の寛解導入効果を評価します。そのため、前回
答においては寛解が認められた時点が FMT 治療開始後 8 週時-14 日より前であっても、「寛解」と評価
することができるものと考えました。
一方、ご指摘により再検討しました結果、本研究では抗菌薬の投与および 3 回の FMT を 1 セットのレジ
メンと考えており、ご指摘のとおり治療効果の評価時期は「これまでの順天堂大学の A-FMT の実績より
FMT 治療開始 6 週時以降が適している」ことから、主要評価項目の評価時期は FMT 治療開始後 6 週
時以降(FMT 治療開始後 8 週時-14 日以降)が妥当であるとの結論に至りました。
したがって、FMT 治療開始後 8 週時(±14 日)に MMDAI が評価されず、当該時点以外の時期に MMDAI
が評価された症例については、中央判定委員会において症例の取扱いを検討することと致します。
以上の内容を研究計画書に下記のとおり修正いたします(修正点は下線部)。
--11.4. 欠落、不採用及び異常データの取扱いの手順
解析時に欠損データを認める場合は、得られたデータで解析を行う。外れ値については、個々に検討す
る。中止・脱落例について、侵襲を伴わない観察項目は可能な限り取得する。
1
15
先進医療技術名: 抗菌薬併用腸内細菌叢移植療法(A-FMT 療法)
2022 年 11 月 30 日
所属・氏名: 順天堂大学医学部附属順天堂医院 消化器内科 永原章仁
1.研究計画書 10.個々の研究対象者における中止基準 について、照会事項 2-2 への回答①②に
ついて確認いたしました。③8 週時に MMDAI が評価されなかった症例に係る主要評価の取扱いに
ついて、につきまして以下の回答がなされております。
「8 週時に MMDAI が評価されなかった症例において、8 週時より前に MMDAI の評価に基づいて寛解
が確認できた症例は寛解として扱い、それ以外の場合において 8 週時に MMDAI が評価されていな
い症例は非寛解として扱います(回答②のケース)。ただし、8 週時に MMDAI が評価されておらず、
それ以降に MMDAI が評価された症例については、中央評価委員会にて症例の取扱いを検討する
予定です。」
下線部につきまして、8 週時に設定されている許容範囲は±14 日でございますが、許容範囲外(特
に-14 日以前)に MMDAI が評価され、寛解と判断された場合に、その症例を寛解として扱う適切性
についてご回答ください。なお、3.4.1 の主要評価項目の設定根拠では「A-FMT によるUCへの治療
効果を評価するには、これまでの順天堂大学の A-FMT の実績より FMT 治療開始 6 週時以降が適
している」との記載もあり、それを踏まえて主要評価項目で寛解と判断可能な許容範囲についての
検討が必要かと考えますが、いかがでしょうか。
【回答】
ご指摘ありがとうございます。本研究では A-FMT 療法の寛解導入効果を評価します。そのため、前回
答においては寛解が認められた時点が FMT 治療開始後 8 週時-14 日より前であっても、「寛解」と評価
することができるものと考えました。
一方、ご指摘により再検討しました結果、本研究では抗菌薬の投与および 3 回の FMT を 1 セットのレジ
メンと考えており、ご指摘のとおり治療効果の評価時期は「これまでの順天堂大学の A-FMT の実績より
FMT 治療開始 6 週時以降が適している」ことから、主要評価項目の評価時期は FMT 治療開始後 6 週
時以降(FMT 治療開始後 8 週時-14 日以降)が妥当であるとの結論に至りました。
したがって、FMT 治療開始後 8 週時(±14 日)に MMDAI が評価されず、当該時点以外の時期に MMDAI
が評価された症例については、中央判定委員会において症例の取扱いを検討することと致します。
以上の内容を研究計画書に下記のとおり修正いたします(修正点は下線部)。
--11.4. 欠落、不採用及び異常データの取扱いの手順
解析時に欠損データを認める場合は、得られたデータで解析を行う。外れ値については、個々に検討す
る。中止・脱落例について、侵襲を伴わない観察項目は可能な限り取得する。
1
15