よむ、つかう、まなぶ。
資料2-1 医薬品等の使用上の注意の改訂について (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31510.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第4回 3/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令和5年 1 月 12 日発出
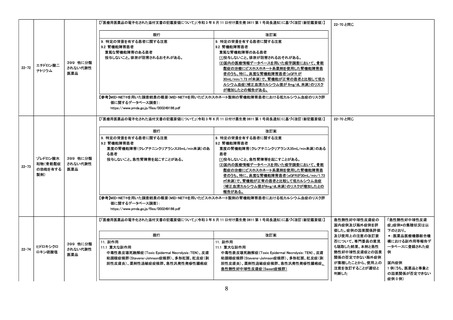
【「医療用医薬品添付文書の記載要領について」(平成 9 年 4 月 25 日付け薬発第 606 号局長通知)に基づく改訂(旧記載要領)】
現行
22-65
ヒドロキシエチ
ルデンプン
70000
ヒドロキシエチ
ルデンプン
70000・塩化ナト
リウム・塩化カ
リウム・塩化カ
ルシウム水和
物・乳酸ナトリ
ウム
改訂案
禁忌
(新設)
禁忌
重症の敗血症の患者〔患者の状態を悪化させるおそれがある。〕
効能・効果に関連する使用上の注意
重症敗血症等の重症患者管理における相対的な循環血液量低下に
は使用しないこと。
効能・効果に関連する使用上の注意
重症患者管理における相対的な循環血液量低下には使用しないこ
と。
(新設)
慎重投与
敗血症の患者(重症の敗血症の患者を除く)〔重症化した場合に、患
者の状態を悪化させるおそれがある。〕
その他の注意
海外臨床試験において、重症敗血症患者にHES製剤注)を使用した場
合、酢酸リンゲル液を使用した場合と比較して投与後90日時点での
死亡のリスクが増加し腎代替療法を要した患者の割合が高かったと
の報告がある。また、敗血症患者を含むICUの入院患者にHES製剤
を使用した場合、生理食塩液を使用した場合と比較して投与後90日
までの死亡のリスクは増加しなかったが、腎代替療法を要した患者
の割合が高かったとの報告がある。
注)本剤とは分子量及び置換度等の異なるもの。
その他の注意
海外臨床試験において、重症敗血症患者(感染が確認され、かつ
全身性炎症反応症候群(SIRS)基準を有し、少なくとも1つの臓器不
全(=SOFAスコア3以上)を呈した患者)にHES製剤注)を使用した場
合、酢酸リンゲル液を使用した場合と比較して投与後90日時点で
の死亡のリスクが増加し腎代替療法を要した患者の割合が高かっ
たとの報告がある。また、敗血症患者を含むICUの入院患者にHES
製剤を使用した場合、生理食塩液を使用した場合と比較して投与
後90日までの死亡のリスクは増加しなかったが、腎代替療法を要
した患者の割合が高かったとの報告がある。
注)本剤とは分子量及び置換度等の異なるもの。
331 血液代用
剤
【「医療用医薬品添付文書の記載要領について」(平成 9 年 4 月 25 日付け薬発第 606 号局長通知)に基づく改訂(旧記載要領)】
現行
22-66
ヒドロキシエチ
ルデンプン
130000
改訂案
警告
警告
重症敗血症等の重症患者管理における相対的な循環血液量低下で
重症患者管理における相対的な循環血液量低下で本剤を使用した
本剤を使用した場合には、患者の状態を悪化させるおそれがあるた
場合には、患者の状態を悪化させるおそれがあるため、治療上の有
め、治療上の有益性が危険性を上回る場合にのみ投与すること。
益性が危険性を上回る場合にのみ投与すること。
331 血液代用
剤
※調査結果報告書
(https://www.pmda.go.jp/files/000249783.pdf)参照
禁忌
(新設)
禁忌
重症の敗血症の患者〔患者の状態を悪化させるおそれがある。〕
慎重投与
(新設)
慎重投与
敗血症の患者(重症の敗血症の患者を除く)〔重症化した場合に、患
者の状態を悪化させるおそれがある。〕
その他の注意
海外臨床試験において、重症敗血症患者にHES製剤を使用した場
合、酢酸リンゲル液を使用した場合と比較して投与後90日時点での
その他の注意
海外臨床試験において、重症敗血症患者(感染が確認され、かつ
全身性炎症反応症候群(SIRS)基準を有し、少なくとも1つの臓器
3
22-65 と同じ
【「医療用医薬品添付文書の記載要領について」(平成 9 年 4 月 25 日付け薬発第 606 号局長通知)に基づく改訂(旧記載要領)】
現行
22-65
ヒドロキシエチ
ルデンプン
70000
ヒドロキシエチ
ルデンプン
70000・塩化ナト
リウム・塩化カ
リウム・塩化カ
ルシウム水和
物・乳酸ナトリ
ウム
改訂案
禁忌
(新設)
禁忌
重症の敗血症の患者〔患者の状態を悪化させるおそれがある。〕
効能・効果に関連する使用上の注意
重症敗血症等の重症患者管理における相対的な循環血液量低下に
は使用しないこと。
効能・効果に関連する使用上の注意
重症患者管理における相対的な循環血液量低下には使用しないこ
と。
(新設)
慎重投与
敗血症の患者(重症の敗血症の患者を除く)〔重症化した場合に、患
者の状態を悪化させるおそれがある。〕
その他の注意
海外臨床試験において、重症敗血症患者にHES製剤注)を使用した場
合、酢酸リンゲル液を使用した場合と比較して投与後90日時点での
死亡のリスクが増加し腎代替療法を要した患者の割合が高かったと
の報告がある。また、敗血症患者を含むICUの入院患者にHES製剤
を使用した場合、生理食塩液を使用した場合と比較して投与後90日
までの死亡のリスクは増加しなかったが、腎代替療法を要した患者
の割合が高かったとの報告がある。
注)本剤とは分子量及び置換度等の異なるもの。
その他の注意
海外臨床試験において、重症敗血症患者(感染が確認され、かつ
全身性炎症反応症候群(SIRS)基準を有し、少なくとも1つの臓器不
全(=SOFAスコア3以上)を呈した患者)にHES製剤注)を使用した場
合、酢酸リンゲル液を使用した場合と比較して投与後90日時点で
の死亡のリスクが増加し腎代替療法を要した患者の割合が高かっ
たとの報告がある。また、敗血症患者を含むICUの入院患者にHES
製剤を使用した場合、生理食塩液を使用した場合と比較して投与
後90日までの死亡のリスクは増加しなかったが、腎代替療法を要
した患者の割合が高かったとの報告がある。
注)本剤とは分子量及び置換度等の異なるもの。
331 血液代用
剤
【「医療用医薬品添付文書の記載要領について」(平成 9 年 4 月 25 日付け薬発第 606 号局長通知)に基づく改訂(旧記載要領)】
現行
22-66
ヒドロキシエチ
ルデンプン
130000
改訂案
警告
警告
重症敗血症等の重症患者管理における相対的な循環血液量低下で
重症患者管理における相対的な循環血液量低下で本剤を使用した
本剤を使用した場合には、患者の状態を悪化させるおそれがあるた
場合には、患者の状態を悪化させるおそれがあるため、治療上の有
め、治療上の有益性が危険性を上回る場合にのみ投与すること。
益性が危険性を上回る場合にのみ投与すること。
331 血液代用
剤
※調査結果報告書
(https://www.pmda.go.jp/files/000249783.pdf)参照
禁忌
(新設)
禁忌
重症の敗血症の患者〔患者の状態を悪化させるおそれがある。〕
慎重投与
(新設)
慎重投与
敗血症の患者(重症の敗血症の患者を除く)〔重症化した場合に、患
者の状態を悪化させるおそれがある。〕
その他の注意
海外臨床試験において、重症敗血症患者にHES製剤を使用した場
合、酢酸リンゲル液を使用した場合と比較して投与後90日時点での
その他の注意
海外臨床試験において、重症敗血症患者(感染が確認され、かつ
全身性炎症反応症候群(SIRS)基準を有し、少なくとも1つの臓器
3
22-65 と同じ