よむ、つかう、まなぶ。
【資料3-1】鹿野参考人提出資料:小児がん及び小児希少難治性疾患に係る医薬品開発の推進制度に資する調査研究 (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00028.html |
| 出典情報 | 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会(第1回 7/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
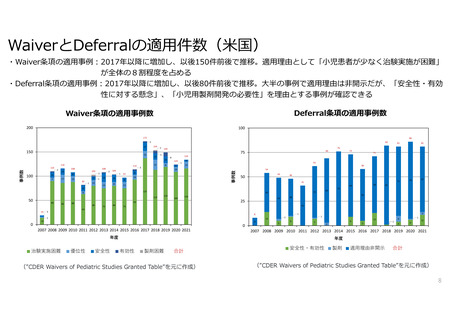
WaiverとDeferralの適用件数(米国)
・Waiver条項の適用事例:2017年以降に増加し、以後150件前後で推移。適用理由として「小児患者が少なく治験実施が困難」
が全体の8割程度を占める
・Deferral条項の適用事例:2017年以降に増加し、以後80件前後で推移。大半の事例で適用理由は非開示だが、「安全性・有効
性に対する懸念」、「小児用製剤開発の必要性」を理由とする事例が確認できる
Deferral条項の適用事例数
Waiver条項の適用事例数
200
100
172
86
3
150
15
154
13
2
5
14
事例数
110
100
116
2
13
11
7
17
108
103
8
12
7
82
1
12
108
3
1
114
104
2
1
18
15
8
13
97
9
21
3
8
124
1
4
10
4
58
49
50
48
71
41
12
137
90
19
3
86
109
116
93
88
80
63
80
75
41
2007 2008 2009 2010 2011 2012 2013 2014 2015 2016 2017 2018 2019 2020 2021
0
8
3
1
8
14
1
2
14
5
9
7
優位性
安全性
9
3
13
5
1
1
6
4
6
11
2007 2008 2009 2010 2011 2012 2013 2014 2015 2016 2017 2018 2019 2020 2021
年度
治験実施困難
67
79
81
53
75
2
0
76
58
64
38
42
25
66
53
40
113
50
71
54
13
119
81
61
14
10
73
69
75
134
8
8
6
81
76
149
事例数
17
82
年度
有効性
製剤困難
合計
(”CDER Waivers of Pediatric Studies Granted Table”を元に作成)
安全性・有効性
製剤
適用理由非開示
合計
(”CDER Waivers of Pediatric Studies Granted Table”を元に作成)
8
・Waiver条項の適用事例:2017年以降に増加し、以後150件前後で推移。適用理由として「小児患者が少なく治験実施が困難」
が全体の8割程度を占める
・Deferral条項の適用事例:2017年以降に増加し、以後80件前後で推移。大半の事例で適用理由は非開示だが、「安全性・有効
性に対する懸念」、「小児用製剤開発の必要性」を理由とする事例が確認できる
Deferral条項の適用事例数
Waiver条項の適用事例数
200
100
172
86
3
150
15
154
13
2
5
14
事例数
110
100
116
2
13
11
7
17
108
103
8
12
7
82
1
12
108
3
1
114
104
2
1
18
15
8
13
97
9
21
3
8
124
1
4
10
4
58
49
50
48
71
41
12
137
90
19
3
86
109
116
93
88
80
63
80
75
41
2007 2008 2009 2010 2011 2012 2013 2014 2015 2016 2017 2018 2019 2020 2021
0
8
3
1
8
14
1
2
14
5
9
7
優位性
安全性
9
3
13
5
1
1
6
4
6
11
2007 2008 2009 2010 2011 2012 2013 2014 2015 2016 2017 2018 2019 2020 2021
年度
治験実施困難
67
79
81
53
75
2
0
76
58
64
38
42
25
66
53
40
113
50
71
54
13
119
81
61
14
10
73
69
75
134
8
8
6
81
76
149
事例数
17
82
年度
有効性
製剤困難
合計
(”CDER Waivers of Pediatric Studies Granted Table”を元に作成)
安全性・有効性
製剤
適用理由非開示
合計
(”CDER Waivers of Pediatric Studies Granted Table”を元に作成)
8