よむ、つかう、まなぶ。
04 資料1-2 MSD株式会社提出資料 (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36248.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第21回 11/9)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
Public
多価の結合型ワクチンの開発における課題とV114の取り組み
多価の結合型ワクチンの開発の課題
多価にすることにより、キャリアタンパク質の量が多くなると、莢膜多糖体に対する免疫誘導を損なう可能性があるため、
ワクチンに含有可能な⾎清型数には限りがある1,2)。
V114の製剤開発︓有効性の維持に係る免疫原性の追求
①初期製剤の開発
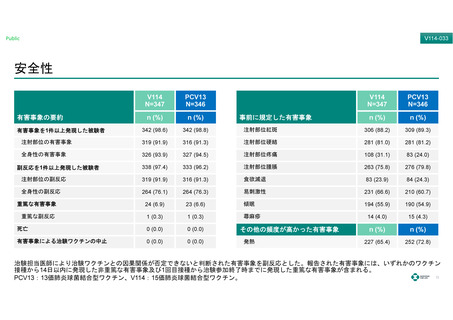
初期の開発製剤による乳児を対象とした臨床試験では、許容可能な安全性プロファイルを有していたが、15⾎清型のうち、
いくつかの⾎清型で免疫原性の基準を満たせなかった3)。
②免疫原性向上のための製剤変更
免疫原性を向上させるために、キャリアタンパク質の結合法を変更するなど改良と検討を重ねた4)。
③免疫原性の向上
健康乳児(2〜6カ⽉)を対象とした国内第Ⅲ相試験(033試験)において、
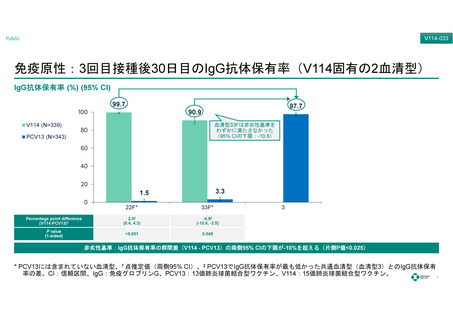
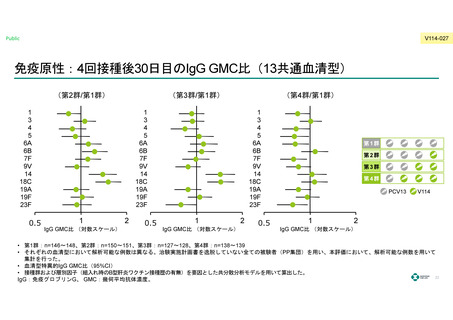
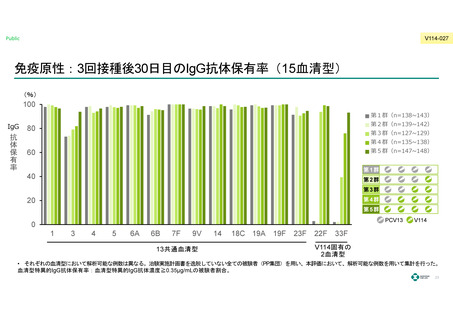
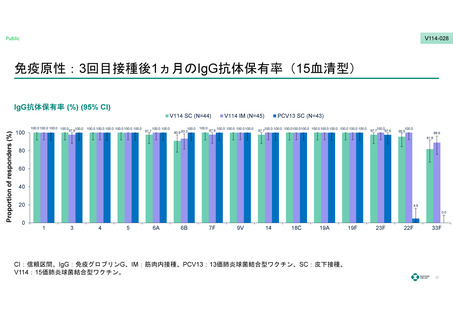
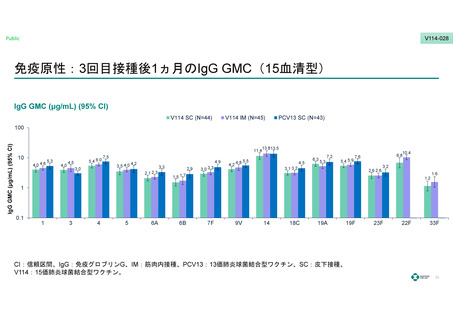
V114群の3回接種後30⽇⽬のPCV13と共通する13⾎清型の⾎清型特異的IgG抗体保有率
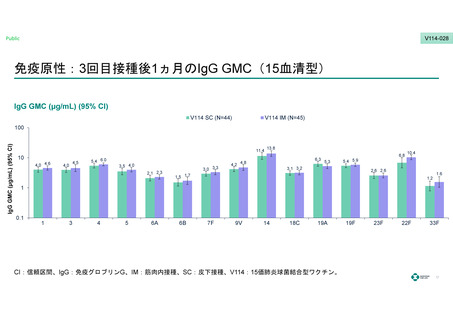
および⾎清型特異的IgG GMCはPCV13群に対する⾮劣性を⽰した。
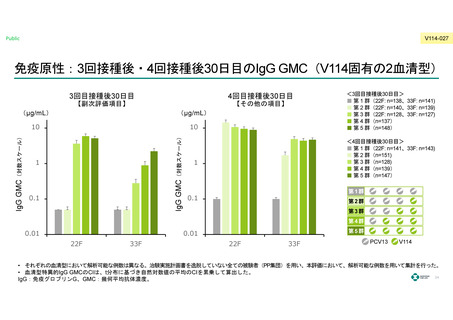
また、固有の2⾎清型においては、⾎清型特異的IgG抗体応答を⽰した5) 。
1)Klugman KP, et al. Plotkinʼs Vaccines. 7th; 2018: 773-815. 2)IASR Vol. 44 p3-5: 2023年1⽉号. 3)Greenberg D, et al. Vaccine. 2018; 36(45): 6883-6891.
4)Rupp R, et al. Hum Vaccin Immunother. 2019;15(3):549-559. 5)承認時評価資料: 国内第Ⅲ相試験(033試験)
4
多価の結合型ワクチンの開発における課題とV114の取り組み
多価の結合型ワクチンの開発の課題
多価にすることにより、キャリアタンパク質の量が多くなると、莢膜多糖体に対する免疫誘導を損なう可能性があるため、
ワクチンに含有可能な⾎清型数には限りがある1,2)。
V114の製剤開発︓有効性の維持に係る免疫原性の追求
①初期製剤の開発
初期の開発製剤による乳児を対象とした臨床試験では、許容可能な安全性プロファイルを有していたが、15⾎清型のうち、
いくつかの⾎清型で免疫原性の基準を満たせなかった3)。
②免疫原性向上のための製剤変更
免疫原性を向上させるために、キャリアタンパク質の結合法を変更するなど改良と検討を重ねた4)。
③免疫原性の向上
健康乳児(2〜6カ⽉)を対象とした国内第Ⅲ相試験(033試験)において、
V114群の3回接種後30⽇⽬のPCV13と共通する13⾎清型の⾎清型特異的IgG抗体保有率
および⾎清型特異的IgG GMCはPCV13群に対する⾮劣性を⽰した。
また、固有の2⾎清型においては、⾎清型特異的IgG抗体応答を⽰した5) 。
1)Klugman KP, et al. Plotkinʼs Vaccines. 7th; 2018: 773-815. 2)IASR Vol. 44 p3-5: 2023年1⽉号. 3)Greenberg D, et al. Vaccine. 2018; 36(45): 6883-6891.
4)Rupp R, et al. Hum Vaccin Immunother. 2019;15(3):549-559. 5)承認時評価資料: 国内第Ⅲ相試験(033試験)
4