よむ、つかう、まなぶ。
資料4-2 ロミプロスチム(遺伝子組換え) (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00032.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第58回 3/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
資料 4‐2
医療上の必要性の高い未承認薬・適応外薬検討会議
公知申請への該当性に係る報告書(案)
ロミプロスチム(遺伝子組換え)
小児の慢性特発性血小板減少性紫斑病
1.要望内容の概略について
要 望 さ れ 一般名:ロミプロスチム(遺伝子組換え)
た医薬品
販売名:ロミプレート皮下注 250 g 調製用
会社名:協和キリン株式会社
要望者名
日本小児血液・がん学会
要望内容
効能・効果
慢性特発性血小板減少性紫斑病
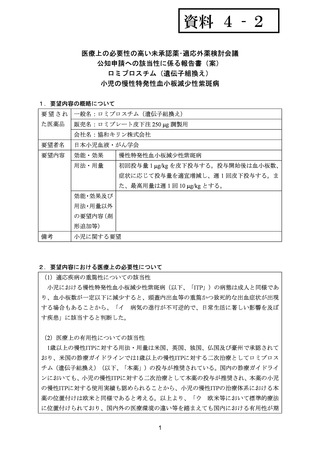
用法・用量
初回投与量 1 g/kg を皮下投与する。投与開始後は血小板数、
症状に応じて投与量を適宜増減し、週 1 回皮下投与する。ま
た、最高用量は週 1 回 10 g/kg とする。
効能・効果及び
用法・用量以外
の要望内容(剤
形追加等)
備考
小児に関する要望
2.要望内容における医療上の必要性について
(1)適応疾病の重篤性についての該当性
小児における慢性特発性血小板減少性紫斑病(以下、「ITP」)の病態は成人と同様であ
り、血小板数が一定以下に減少すると、頭蓋内出血等の重篤かつ致死的な出血症状が出現
する場合もあることから、「イ
病気の進行が不可逆的で、日常生活に著しい影響を及ぼ
す疾患」に該当すると判断した。
(2)医療上の有用性についての該当性
1歳以上の慢性ITPに対する用法・用量は米国、英国、独国、仏国及び豪州で承認されて
おり、米国の診療ガイドラインでは1歳以上の慢性ITPに対する二次治療としてロミプロス
チム(遺伝子組換え)(以下、「本薬」)の投与が推奨されている。国内の診療ガイドライ
ンにおいても、小児の慢性ITPに対する二次治療として本薬の投与が推奨され、本薬の小児
の慢性ITPに対する使用実績も認められることから、小児の慢性ITPの治療体系における本
薬の位置付けは欧米と同様であると考える。以上より、「ウ
欧米等において標準的療法
に位置付けられており、国内外の医療環境の違い等を踏まえても国内における有用性が期
1
54 / 213
医療上の必要性の高い未承認薬・適応外薬検討会議
公知申請への該当性に係る報告書(案)
ロミプロスチム(遺伝子組換え)
小児の慢性特発性血小板減少性紫斑病
1.要望内容の概略について
要 望 さ れ 一般名:ロミプロスチム(遺伝子組換え)
た医薬品
販売名:ロミプレート皮下注 250 g 調製用
会社名:協和キリン株式会社
要望者名
日本小児血液・がん学会
要望内容
効能・効果
慢性特発性血小板減少性紫斑病
用法・用量
初回投与量 1 g/kg を皮下投与する。投与開始後は血小板数、
症状に応じて投与量を適宜増減し、週 1 回皮下投与する。ま
た、最高用量は週 1 回 10 g/kg とする。
効能・効果及び
用法・用量以外
の要望内容(剤
形追加等)
備考
小児に関する要望
2.要望内容における医療上の必要性について
(1)適応疾病の重篤性についての該当性
小児における慢性特発性血小板減少性紫斑病(以下、「ITP」)の病態は成人と同様であ
り、血小板数が一定以下に減少すると、頭蓋内出血等の重篤かつ致死的な出血症状が出現
する場合もあることから、「イ
病気の進行が不可逆的で、日常生活に著しい影響を及ぼ
す疾患」に該当すると判断した。
(2)医療上の有用性についての該当性
1歳以上の慢性ITPに対する用法・用量は米国、英国、独国、仏国及び豪州で承認されて
おり、米国の診療ガイドラインでは1歳以上の慢性ITPに対する二次治療としてロミプロス
チム(遺伝子組換え)(以下、「本薬」)の投与が推奨されている。国内の診療ガイドライ
ンにおいても、小児の慢性ITPに対する二次治療として本薬の投与が推奨され、本薬の小児
の慢性ITPに対する使用実績も認められることから、小児の慢性ITPの治療体系における本
薬の位置付けは欧米と同様であると考える。以上より、「ウ
欧米等において標準的療法
に位置付けられており、国内外の医療環境の違い等を踏まえても国内における有用性が期
1
54 / 213