よむ、つかう、まなぶ。
資料2-2 ベポタスチンベシル酸塩のリスク区分について[5.2MB] (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42464.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会安全対策調査会(令和6年度第5回 8/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別紙(1)
調査結果の概要
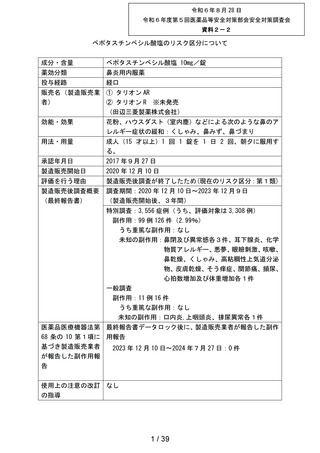
タリオン AR(以下、本剤)の本製造販売後安全性調査は 2020 年 12 月 10 日に開始され、当該調
査期間(最終報告:2020 年 12 月 10 日~2023 年 12 月 9 日)までの調査結果の概要は次のとおりで
ある。
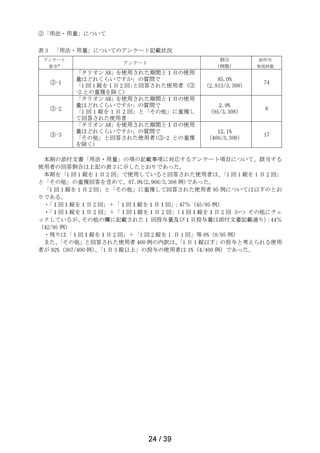
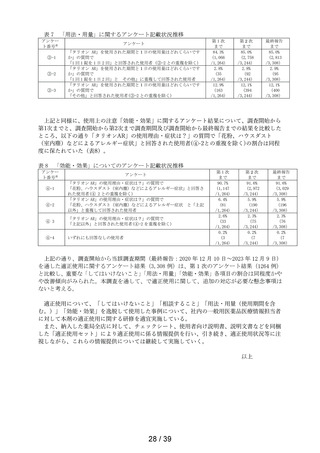
Ⅰ.副作用頻度調査(モニター店によるアンケート調査)
調査開始から当該調査期間(最終報告:2020 年 12 月 10 日~2023 年 12 月 9 日)までに 3,556 例
のアンケートを入手し、集計対象外症例(重複症例、情報源不明症例、未投与症例、有害事象判
定未実施症例)248 例を除いた 3,308 例(施設数:29 施設)を安全性集計対象症例とした。なお、
集計対象外症例 248 例において副作用の報告は 1 例 1 件(
「異食症」:「使用上の注意」から予測
できない・非重篤)であった。
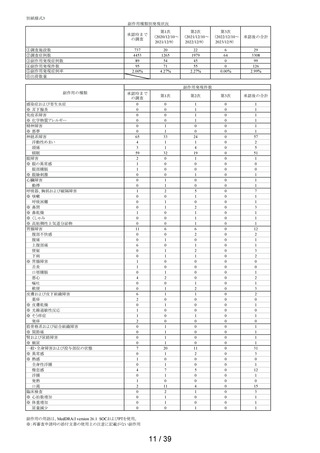
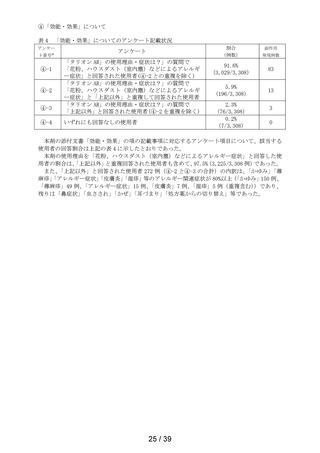
安全性集計対象症例中、副作用は 99 例 126 件であり、副作用発現症例率は 2.99 %(99/3,308
例)であった。
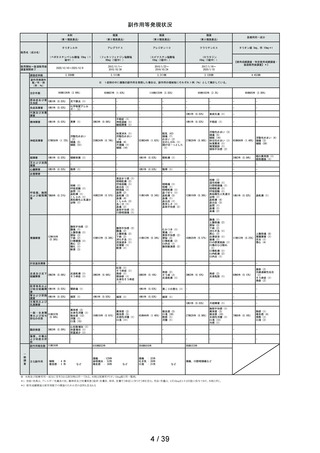
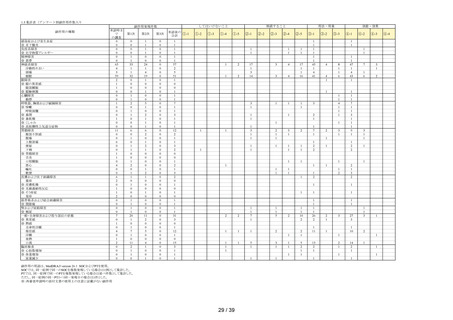
副作用の種類別内訳(MedDRA 基本語)では、
「使用上の注意」から予測できる副作用は「傾眠」
51 件、「口渇」15 件、
「倦怠感」12 件、
「頭痛」5 件、「便秘」「軟便」各 3 件、
「浮動性めまい」、
「腹部不快感」、
「下痢」、
「悪心」各 2 件、
「動悸」
「呼吸困難」「腹痛」
「口唇腫脹」「嘔吐」
「全身
性浮腫」「浮腫」
「尿量減少」「上腹部痛」各 1 件であった。
「使用上の注意」から予測できない副作用は、「鼻閉」「異常感」各 3 件、
「耳下腺炎」
「化学物
質アレルギー」
「悪夢」
「眼瞼刺激」
「咳嗽」
「鼻乾燥」
「くしゃみ」
「高粘稠性上気道分泌物」
「皮膚
乾燥」
「そう痒症」「関節痛」「頻尿」
「心拍数増加」
「体重増加」1 件であった。
「使用上の注意」から予測できる副作用および予測できない副作用ともに、重篤な副作用はな
かった。
Ⅱ.一般調査
本剤の調査開始から当該調査期間(最終報告:2020 年 12 月 10 日~2023 年 12 月 9 日)までに
副作用頻度調査以外の使用者あるいは薬剤師からの自発報告として 11 例 16 件の副作用報告があ
った。
副作用の種類別内訳(MedDRA 基本語)では、
「使用上の注意」から予測できる副作用は「傾眠」
4 件、
「倦怠感」3 件、
「下痢」
「感覚鈍麻」
「排尿回数減少」
「排尿困難」
「腹部不快感」
「腹痛」各 1
件であった。
「使用上の注意」から予測できない副作用は、
「口内炎」
「上咽頭炎」
「排尿異常」各 1 件であっ
た。
「使用上の注意」から予測できる副作用および予測できない副作用ともに、重篤な副作用はな
かった。
Ⅲ.その他
文献情報や外国措置等の情報で報告すべき事項はなかった。
10 / 39
調査結果の概要
タリオン AR(以下、本剤)の本製造販売後安全性調査は 2020 年 12 月 10 日に開始され、当該調
査期間(最終報告:2020 年 12 月 10 日~2023 年 12 月 9 日)までの調査結果の概要は次のとおりで
ある。
Ⅰ.副作用頻度調査(モニター店によるアンケート調査)
調査開始から当該調査期間(最終報告:2020 年 12 月 10 日~2023 年 12 月 9 日)までに 3,556 例
のアンケートを入手し、集計対象外症例(重複症例、情報源不明症例、未投与症例、有害事象判
定未実施症例)248 例を除いた 3,308 例(施設数:29 施設)を安全性集計対象症例とした。なお、
集計対象外症例 248 例において副作用の報告は 1 例 1 件(
「異食症」:「使用上の注意」から予測
できない・非重篤)であった。
安全性集計対象症例中、副作用は 99 例 126 件であり、副作用発現症例率は 2.99 %(99/3,308
例)であった。
副作用の種類別内訳(MedDRA 基本語)では、
「使用上の注意」から予測できる副作用は「傾眠」
51 件、「口渇」15 件、
「倦怠感」12 件、
「頭痛」5 件、「便秘」「軟便」各 3 件、
「浮動性めまい」、
「腹部不快感」、
「下痢」、
「悪心」各 2 件、
「動悸」
「呼吸困難」「腹痛」
「口唇腫脹」「嘔吐」
「全身
性浮腫」「浮腫」
「尿量減少」「上腹部痛」各 1 件であった。
「使用上の注意」から予測できない副作用は、「鼻閉」「異常感」各 3 件、
「耳下腺炎」
「化学物
質アレルギー」
「悪夢」
「眼瞼刺激」
「咳嗽」
「鼻乾燥」
「くしゃみ」
「高粘稠性上気道分泌物」
「皮膚
乾燥」
「そう痒症」「関節痛」「頻尿」
「心拍数増加」
「体重増加」1 件であった。
「使用上の注意」から予測できる副作用および予測できない副作用ともに、重篤な副作用はな
かった。
Ⅱ.一般調査
本剤の調査開始から当該調査期間(最終報告:2020 年 12 月 10 日~2023 年 12 月 9 日)までに
副作用頻度調査以外の使用者あるいは薬剤師からの自発報告として 11 例 16 件の副作用報告があ
った。
副作用の種類別内訳(MedDRA 基本語)では、
「使用上の注意」から予測できる副作用は「傾眠」
4 件、
「倦怠感」3 件、
「下痢」
「感覚鈍麻」
「排尿回数減少」
「排尿困難」
「腹部不快感」
「腹痛」各 1
件であった。
「使用上の注意」から予測できない副作用は、
「口内炎」
「上咽頭炎」
「排尿異常」各 1 件であっ
た。
「使用上の注意」から予測できる副作用および予測できない副作用ともに、重篤な副作用はな
かった。
Ⅲ.その他
文献情報や外国措置等の情報で報告すべき事項はなかった。
10 / 39