よむ、つかう、まなぶ。
03【資料1】新型コロナワクチンの接種について (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43697.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会(第58回 9/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
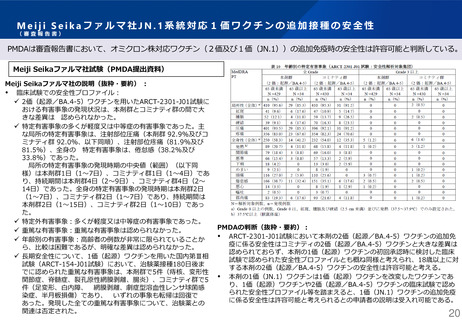
JN.1系統に対応したワクチンの開発状況
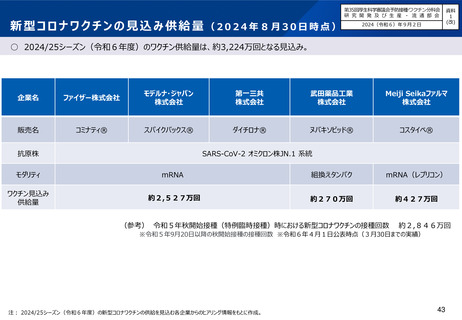
○ 現時点で、5社のワクチンが、JN.1系統対応1価ワクチンについての薬事承認を取得している。
○ ファイザー社、モデルナ社、第一三共社、武田薬品工業社の4社については、令和5年度までの臨時接種ですでに使用したワクチ
ンにおける、JN.1系統への対応である。
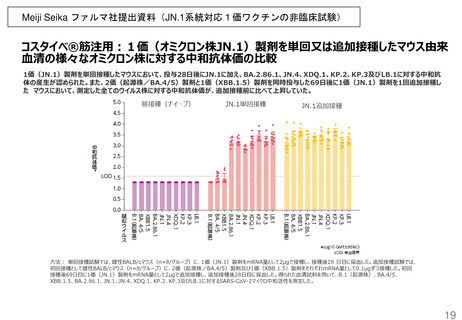
○ Meiji Seikaファルマ社のワクチンについては、令和5年度は従来株ワクチンについて薬事承認を取得していたが供給されず、臨時
接種では使用していない。今年度秋から、JN.1系統対応に係る承認事項一部変更を取得したワクチンが供給される見通しである。
新たに供給されるワクチンのJN.1
系統対応状況等
令和5年度までの臨時接種において使用したワクチンのJN.1系統対応状況等
企業名
ファイザー株式会社
モデルナ・ジャパン
株式会社
第一三共
株式会社
武田薬品工業
株式会社
Meiji Seikaファルマ
株式会社
販売名
コミナティ®
スパイクバックス®
ダイチロナ®
ヌバキソビッド®
コスタイベ®
種別
オミクロン株JN.1系統対応の1価ワクチン
モダリティ
薬事承認の
状況
mRNA
令和6年8月8日
一変承認*
令和6年8月23日
一変承認*
令和6年9月6日
一変承認*
有効性・安
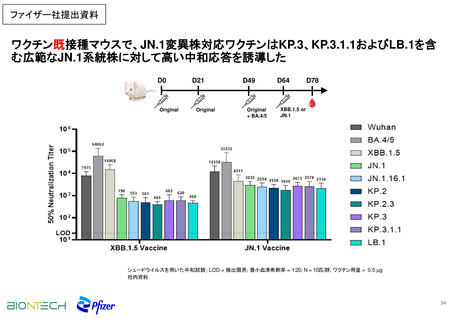
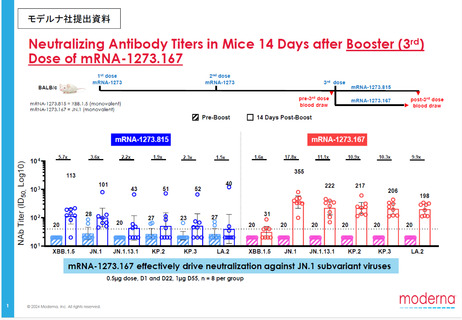
JN.1系統株に対する免疫原性(非臨床)【参考資料】
全性データ
組換えタンパク
mRNA(レプリコン)
令和6年9月5日
一変承認*
令和6年9月13日
一変承認*
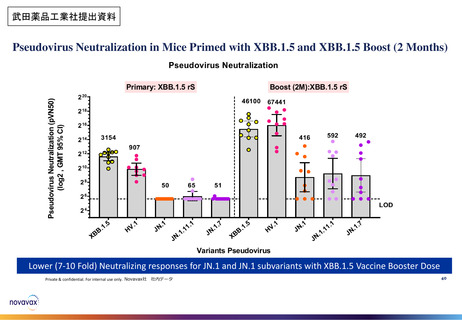
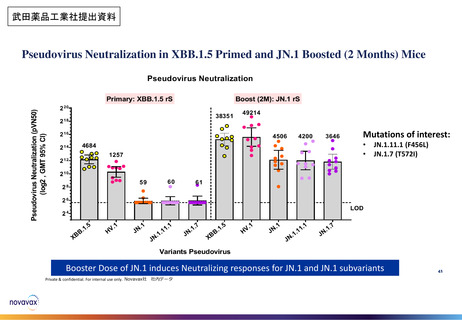
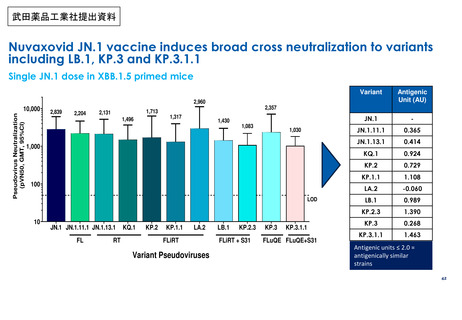
・JN.1系統株に対する免疫原性 (非臨床)
・オミクロン株BA.4/5系統対応ワクチンの免疫
原性・安全性(臨床)【参考資料】
・JN.1系統株に対する免疫原性(非臨床)
・オミクロン株BA.4/5系統対応ワクチンの
免疫原性・安全性(臨床)【p18-20】
(*)一変承認:製造販売承認事項一部変更の承認
〈参考〉変異株対応に関する薬事審査の方針
○「新型コロナウイルスワクチンの株の変更に関する取扱い等について」(令和6年5月23日付 医薬局医薬品審査管理課・監視指導・麻薬対策課長通知)
より抜粋、(注)と下線を追加
(2)一般的に新型コロナウイルスワクチンの抗原株を変更する際には、抗原株の変更前後のワクチンでの品質特性に関して分析・評価を行う必要があるこ
と。また、臨床試験成績により、標的とした新たな抗原株に対する免疫原性を有するとともに、安全性が変更前のワクチンと大きな相違がないことを明ら
かにする必要があること。
(3)前項の分析・評価及び臨床試験成績により抗原株変更が認められた本邦既承認のワクチンのうち、抗原株の変更によりその品質及び安全性が変更の影
響を受けない蓋然性が高く、免疫原性が非臨床試験によって予見できるワクチンについては、以下(4)から(12)に記載する対応(注:抗原性の免疫学
的特性に関する資料 (例:ワクチンの非臨床試験における免疫原性のデータ等) のPMDAへの提出等))を行うこと。
17
○ 現時点で、5社のワクチンが、JN.1系統対応1価ワクチンについての薬事承認を取得している。
○ ファイザー社、モデルナ社、第一三共社、武田薬品工業社の4社については、令和5年度までの臨時接種ですでに使用したワクチ
ンにおける、JN.1系統への対応である。
○ Meiji Seikaファルマ社のワクチンについては、令和5年度は従来株ワクチンについて薬事承認を取得していたが供給されず、臨時
接種では使用していない。今年度秋から、JN.1系統対応に係る承認事項一部変更を取得したワクチンが供給される見通しである。
新たに供給されるワクチンのJN.1
系統対応状況等
令和5年度までの臨時接種において使用したワクチンのJN.1系統対応状況等
企業名
ファイザー株式会社
モデルナ・ジャパン
株式会社
第一三共
株式会社
武田薬品工業
株式会社
Meiji Seikaファルマ
株式会社
販売名
コミナティ®
スパイクバックス®
ダイチロナ®
ヌバキソビッド®
コスタイベ®
種別
オミクロン株JN.1系統対応の1価ワクチン
モダリティ
薬事承認の
状況
mRNA
令和6年8月8日
一変承認*
令和6年8月23日
一変承認*
令和6年9月6日
一変承認*
有効性・安
JN.1系統株に対する免疫原性(非臨床)【参考資料】
全性データ
組換えタンパク
mRNA(レプリコン)
令和6年9月5日
一変承認*
令和6年9月13日
一変承認*
・JN.1系統株に対する免疫原性 (非臨床)
・オミクロン株BA.4/5系統対応ワクチンの免疫
原性・安全性(臨床)【参考資料】
・JN.1系統株に対する免疫原性(非臨床)
・オミクロン株BA.4/5系統対応ワクチンの
免疫原性・安全性(臨床)【p18-20】
(*)一変承認:製造販売承認事項一部変更の承認
〈参考〉変異株対応に関する薬事審査の方針
○「新型コロナウイルスワクチンの株の変更に関する取扱い等について」(令和6年5月23日付 医薬局医薬品審査管理課・監視指導・麻薬対策課長通知)
より抜粋、(注)と下線を追加
(2)一般的に新型コロナウイルスワクチンの抗原株を変更する際には、抗原株の変更前後のワクチンでの品質特性に関して分析・評価を行う必要があるこ
と。また、臨床試験成績により、標的とした新たな抗原株に対する免疫原性を有するとともに、安全性が変更前のワクチンと大きな相違がないことを明ら
かにする必要があること。
(3)前項の分析・評価及び臨床試験成績により抗原株変更が認められた本邦既承認のワクチンのうち、抗原株の変更によりその品質及び安全性が変更の影
響を受けない蓋然性が高く、免疫原性が非臨床試験によって予見できるワクチンについては、以下(4)から(12)に記載する対応(注:抗原性の免疫学
的特性に関する資料 (例:ワクチンの非臨床試験における免疫原性のデータ等) のPMDAへの提出等))を行うこと。
17