よむ、つかう、まなぶ。
総-2参考3 (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_46580.html |
| 出典情報 | 中央社会保険医療協議会 総会(第599回 12/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
活性化の徴候や症状の発現に注意すること。徴候や症状の発現が認められた場合には、患者に受診す
るよう説明し、本剤の投与を中断し速やかに適切な処置を行うこと。また、ヘルペスウイルス以外の
ウイルスの再活性化にも注意すること。
11) 本剤は免疫抑制作用を有することから、皮膚バリア機能が低下しているアトピー性皮膚炎患者への投
与に際しては十分な観察を行い、皮膚感染症の発現に注意すること。アトピー性皮膚炎患者を対象と
した臨床試験において重篤な皮膚感染症が報告されている。投与中に皮膚感染症が生じた場合は速や
かに適切な対処を考慮すること。
12) 本剤による B 型肝炎ウイルスの再活性化が報告されているので、投与に先立って B 型肝炎ウイルス
感染の有無を確認すること。感染が確認された場合には、関連するガイドライン等を踏まえて適切に
対処すること。
13) 感染症発現のリスクを否定できないので、本剤開始直前及び投与中の生ワクチン接種は行わないこと。
14) 非黒色腫皮膚癌を除く、悪性リンパ腫、固形癌の悪性腫瘍の発現が報告されている。本剤との因果関
係は明らかではないが、悪性腫瘍の発現には注意すること。
15) 皮膚有棘細胞癌、基底細胞癌等の非黒色腫皮膚癌があらわれることがあるので、定期的に皮膚の状態
を確認すること。また、皮膚の異常が認められた場合には、速やかに医療機関を受診するよう患者を
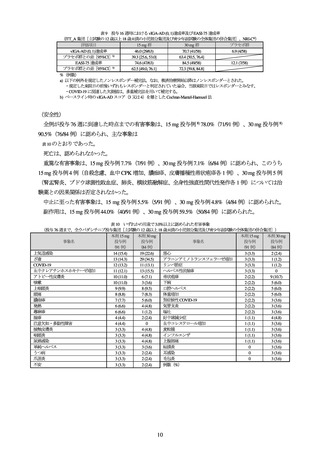
指導すること。臨床試験において本剤 15 mg と比較して本剤 30 mg で非黒色腫皮膚癌の発現率が高い
ことが報告されている。
16) 総コレステロール、LDL コレステロール、HDL コレステロール及びトリグリセリドの上昇等の脂質
検査値異常があらわれることがある。本剤投与開始後は定期的に脂質検査値を確認すること。臨床上
必要と認められた場合には、脂質異常症治療薬の投与等の適切な処置を考慮すること。
17) トランスアミナーゼ値の上昇があらわれることがあるので、ベースラインを測定するとともに、本剤
投与中は観察を十分に行うこと。トランスアミナーゼ値が基準値上限の 3 倍以上に上昇した症例も報
告されている。
18) 妊娠する可能性のある女性には、本剤投与中及び最終投与後 1 月経周期において避妊する必要性及び
適切な避妊法について説明すること。
19) 12 歳以上かつ体重 30 kg 以上 40 kg 未満の小児に投与する場合には、観察を十分に行い、慎重に投与
すること。12 歳未満、又は体重 40 kg 未満の小児等を対象とした臨床試験は実施されていない。
20) 添付文書に加え、製造販売業者が提供する資料等に基づき本剤の特性及び適正使用のために必要な情
報を十分理解してから使用すること。
21) 本剤の医薬品リスク管理計画書を熟読し、安全性検討事項を確認すること。
(参考文献)
アトピー性皮膚炎診療ガイドライン 2021(公益社団法人日本皮膚科学会/一般社団法人日本アレルギー学会 編)
16
るよう説明し、本剤の投与を中断し速やかに適切な処置を行うこと。また、ヘルペスウイルス以外の
ウイルスの再活性化にも注意すること。
11) 本剤は免疫抑制作用を有することから、皮膚バリア機能が低下しているアトピー性皮膚炎患者への投
与に際しては十分な観察を行い、皮膚感染症の発現に注意すること。アトピー性皮膚炎患者を対象と
した臨床試験において重篤な皮膚感染症が報告されている。投与中に皮膚感染症が生じた場合は速や
かに適切な対処を考慮すること。
12) 本剤による B 型肝炎ウイルスの再活性化が報告されているので、投与に先立って B 型肝炎ウイルス
感染の有無を確認すること。感染が確認された場合には、関連するガイドライン等を踏まえて適切に
対処すること。
13) 感染症発現のリスクを否定できないので、本剤開始直前及び投与中の生ワクチン接種は行わないこと。
14) 非黒色腫皮膚癌を除く、悪性リンパ腫、固形癌の悪性腫瘍の発現が報告されている。本剤との因果関
係は明らかではないが、悪性腫瘍の発現には注意すること。
15) 皮膚有棘細胞癌、基底細胞癌等の非黒色腫皮膚癌があらわれることがあるので、定期的に皮膚の状態
を確認すること。また、皮膚の異常が認められた場合には、速やかに医療機関を受診するよう患者を
指導すること。臨床試験において本剤 15 mg と比較して本剤 30 mg で非黒色腫皮膚癌の発現率が高い
ことが報告されている。
16) 総コレステロール、LDL コレステロール、HDL コレステロール及びトリグリセリドの上昇等の脂質
検査値異常があらわれることがある。本剤投与開始後は定期的に脂質検査値を確認すること。臨床上
必要と認められた場合には、脂質異常症治療薬の投与等の適切な処置を考慮すること。
17) トランスアミナーゼ値の上昇があらわれることがあるので、ベースラインを測定するとともに、本剤
投与中は観察を十分に行うこと。トランスアミナーゼ値が基準値上限の 3 倍以上に上昇した症例も報
告されている。
18) 妊娠する可能性のある女性には、本剤投与中及び最終投与後 1 月経周期において避妊する必要性及び
適切な避妊法について説明すること。
19) 12 歳以上かつ体重 30 kg 以上 40 kg 未満の小児に投与する場合には、観察を十分に行い、慎重に投与
すること。12 歳未満、又は体重 40 kg 未満の小児等を対象とした臨床試験は実施されていない。
20) 添付文書に加え、製造販売業者が提供する資料等に基づき本剤の特性及び適正使用のために必要な情
報を十分理解してから使用すること。
21) 本剤の医薬品リスク管理計画書を熟読し、安全性検討事項を確認すること。
(参考文献)
アトピー性皮膚炎診療ガイドライン 2021(公益社団法人日本皮膚科学会/一般社団法人日本アレルギー学会 編)
16