よむ、つかう、まなぶ。
参考資料5 (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000203222_00016.html |
| 出典情報 | 患者申出療養評価会議(第30回 1/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2.実施医療機関の追加について
○ 患者申出療養を実施できる医療機関は、以下のとおりとされている。
① 意見書を作成した臨床研究中核病院
② 患者申出療養評価会議で審議された際に、あらかじめ実施医療機関として実施計画に記載されてい
る医療機関
③ 意見書を作成した臨床研究中核病院が審査し、追加することが認められた医療機関
②については、臨床研究中核病院間の連携を図るため、意見書を作成した臨床研究中核病院以外
の臨床研究中核病院も、原則として実施医療機関となることとしてはどうか。
③については、臨床研究中核病院における審査に資するよう、当会議において審査する際に、 実
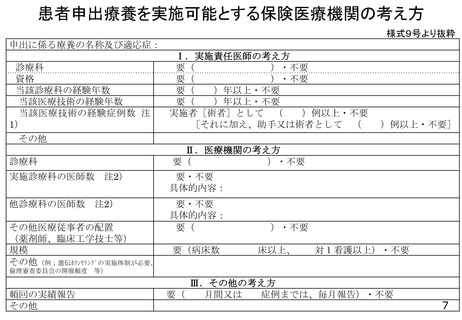
施医療機関追加の判断の参考として「実施可能な医療機関の考え方」を定めておくこととされている
ことから、意見書に含まれる「患者申出療養を実施可能とする保険医療機関の考え方」を元に定め
ることとしてはどうか。
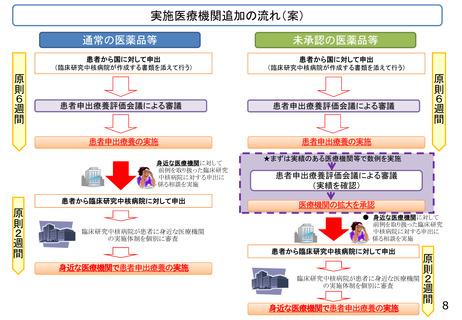
また、患者申出療養として使用される医薬品等の特性やリスク(特に海外・国内ともに未承認の医薬
品等を使用する場合)によっては、安全性等の観点から、実際に投与された結果を告示後に検証す
るなどのプロセスを経て実施医療機関を追加する場合もあると考えられることから、患者申出療養
評価会議における評価の際に、こうした考え方を示すものとして、「実施医療機関の追加に係る取
扱い」を定めておくこととされている。これを踏まえ、考え方を整理してはどうか。
国内未承認の医薬品等の場合は、以下の対象医療機関における患者申出療養としての実績(症例数は
個別に定める)を検証した上で、さらなる実施医療機関の追加の可否を判断することとする。
〔対象医療機関〕
① 臨床研究中核病院
② そのほか、既に使用実績を有していること等一定の水準を満たす医療機関
6
○ 患者申出療養を実施できる医療機関は、以下のとおりとされている。
① 意見書を作成した臨床研究中核病院
② 患者申出療養評価会議で審議された際に、あらかじめ実施医療機関として実施計画に記載されてい
る医療機関
③ 意見書を作成した臨床研究中核病院が審査し、追加することが認められた医療機関
②については、臨床研究中核病院間の連携を図るため、意見書を作成した臨床研究中核病院以外
の臨床研究中核病院も、原則として実施医療機関となることとしてはどうか。
③については、臨床研究中核病院における審査に資するよう、当会議において審査する際に、 実
施医療機関追加の判断の参考として「実施可能な医療機関の考え方」を定めておくこととされている
ことから、意見書に含まれる「患者申出療養を実施可能とする保険医療機関の考え方」を元に定め
ることとしてはどうか。
また、患者申出療養として使用される医薬品等の特性やリスク(特に海外・国内ともに未承認の医薬
品等を使用する場合)によっては、安全性等の観点から、実際に投与された結果を告示後に検証す
るなどのプロセスを経て実施医療機関を追加する場合もあると考えられることから、患者申出療養
評価会議における評価の際に、こうした考え方を示すものとして、「実施医療機関の追加に係る取
扱い」を定めておくこととされている。これを踏まえ、考え方を整理してはどうか。
国内未承認の医薬品等の場合は、以下の対象医療機関における患者申出療養としての実績(症例数は
個別に定める)を検証した上で、さらなる実施医療機関の追加の可否を判断することとする。
〔対象医療機関〕
① 臨床研究中核病院
② そのほか、既に使用実績を有していること等一定の水準を満たす医療機関
6