よむ、つかう、まなぶ。
03【資料1】新型コロナワクチンの接種について (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27963.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会(第37回 9/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2.本日の論点:【1】オミクロン株対応ワクチンの接種について
(1)有効性及び安全性について
ファイザー社製2価のオミクロン株対応ワクチンの安全性(審査報告書)
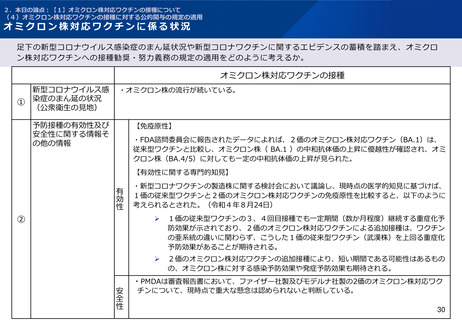
PMDAは審査報告書において、ファイザー社の2価のオミクロン株対応ワクチンの追加接種に係る安全性プロファイル
は従来型ワクチンと概ね同様であり、現時点で重大な懸念は認められていないと判断している。
※
抗原量は、従来型ワクチンでは30μg、2価のオミクロン株対応ワクチンでは、起源株15μg、オミクロン株15μg。
ファイザー社臨床試験(PMDA提出資料)
ファイザー社の説明(抜粋・要約) :
反応原性事象(局所反応及び全身反応):注射部位疼痛、疲労、頭痛等が多く認められ
たが、ほとんどがGrade 1又は2であり、Grade 3以上の事象の発現割合は低かった。
Grade 4の反応原性事象はいずれの接種群でも認められなかった。
有害事象:拡大コホートのいずれかの群で2例以上に認められた有害事象は、リンパ節
症、浮動性めまい及び発疹の他、反応原性事象として規定された事象であり、多くの事
象が治験薬との因果関係ありと判断された。
重篤な有害事象:C4591031試験サブ試験Eの拡大コホートではデータカットオフ日
(2022年5月16日)までに8例認められ、このうち脱水1例(OMI単価ワクチン30 µg
群)を除き、治験薬との因果関係は否定された。
死亡:いずれのサブ試験でもデータカットオフ日までに死亡や治験中止に至った有害事
象は報告されなかった。データカットオフ以降2022年8月4日までに、C4591031試験の
サブ試験E及びサブ試験Dコホート2において死亡例は3例(盲検下で試験継続中であり接
種群不明:心肺不全、壊疽、敗血症性ショック及び過量投与各1例(重複含む))に認め
られ、重篤な有害事象は21例に認められたが、すべて治験薬との因果関係は否定され
た。
心筋炎・心膜炎:C4591031試験のサブ試験E及びサブ試験Dコホート2において、デー
タカットオフ日までに心筋炎・心膜炎は報告されていない。
PMDAの判断(抜粋・要約):
現時点で得られているC4591031試験のサブ試験の結果から、オミクロン株BA.1系統を
含む2価ワクチンの追加接種に係る安全性プロファイルは親ワクチンの追加接種時と概ね
同様であることを確認し、現時点で重大な懸念は認められていないと判断した。ただ
し、変異株ワクチンでの評価例数は限られていることから、引き続き海外情報も含めて
情報収集し、得られた情報に基づき、適切な対応を検討する必要がある。
現時点までに親ワクチンで得られている知見から、心筋炎・心膜炎について、許容でき
ないリスクを示唆する情報は得られていないと考える。2価ワクチンにおいても、親ワク
チンと同様に注意喚起を行うとともに、引き続き情報収集し、得られた情報に基づき適
宜対応を検討する必要があると考える。
17
(1)有効性及び安全性について
ファイザー社製2価のオミクロン株対応ワクチンの安全性(審査報告書)
PMDAは審査報告書において、ファイザー社の2価のオミクロン株対応ワクチンの追加接種に係る安全性プロファイル
は従来型ワクチンと概ね同様であり、現時点で重大な懸念は認められていないと判断している。
※
抗原量は、従来型ワクチンでは30μg、2価のオミクロン株対応ワクチンでは、起源株15μg、オミクロン株15μg。
ファイザー社臨床試験(PMDA提出資料)
ファイザー社の説明(抜粋・要約) :
反応原性事象(局所反応及び全身反応):注射部位疼痛、疲労、頭痛等が多く認められ
たが、ほとんどがGrade 1又は2であり、Grade 3以上の事象の発現割合は低かった。
Grade 4の反応原性事象はいずれの接種群でも認められなかった。
有害事象:拡大コホートのいずれかの群で2例以上に認められた有害事象は、リンパ節
症、浮動性めまい及び発疹の他、反応原性事象として規定された事象であり、多くの事
象が治験薬との因果関係ありと判断された。
重篤な有害事象:C4591031試験サブ試験Eの拡大コホートではデータカットオフ日
(2022年5月16日)までに8例認められ、このうち脱水1例(OMI単価ワクチン30 µg
群)を除き、治験薬との因果関係は否定された。
死亡:いずれのサブ試験でもデータカットオフ日までに死亡や治験中止に至った有害事
象は報告されなかった。データカットオフ以降2022年8月4日までに、C4591031試験の
サブ試験E及びサブ試験Dコホート2において死亡例は3例(盲検下で試験継続中であり接
種群不明:心肺不全、壊疽、敗血症性ショック及び過量投与各1例(重複含む))に認め
られ、重篤な有害事象は21例に認められたが、すべて治験薬との因果関係は否定され
た。
心筋炎・心膜炎:C4591031試験のサブ試験E及びサブ試験Dコホート2において、デー
タカットオフ日までに心筋炎・心膜炎は報告されていない。
PMDAの判断(抜粋・要約):
現時点で得られているC4591031試験のサブ試験の結果から、オミクロン株BA.1系統を
含む2価ワクチンの追加接種に係る安全性プロファイルは親ワクチンの追加接種時と概ね
同様であることを確認し、現時点で重大な懸念は認められていないと判断した。ただ
し、変異株ワクチンでの評価例数は限られていることから、引き続き海外情報も含めて
情報収集し、得られた情報に基づき、適切な対応を検討する必要がある。
現時点までに親ワクチンで得られている知見から、心筋炎・心膜炎について、許容でき
ないリスクを示唆する情報は得られていないと考える。2価ワクチンにおいても、親ワク
チンと同様に注意喚起を行うとともに、引き続き情報収集し、得られた情報に基づき適
宜対応を検討する必要があると考える。
17