よむ、つかう、まなぶ。
別紙1○【先進医療合同会議】先進医療Bに係る新規技術の科学的評価等について (30 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00053.html |
| 出典情報 | 先進医療合同会議(第124回先進医療会議、第152回先進医療技術審査部会 9/7)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
【別添3】
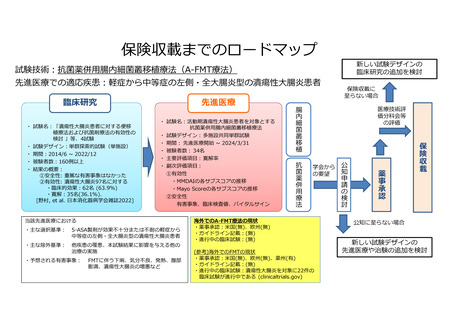
「抗菌薬併用腸内細菌叢移植療法(A-FMT 療法)」の被験者の適格基準
及び選定方法(申請書類より抜粋)
5.被験者の適格基準及び選定方法
<患者適格性基準>
下記の選択基準を全て満たし、かつ除外基準のいずれにも該当しない研究対象者を対象と
する。
患者選択基準
1)活動期の左側・全大腸炎型の潰瘍性大腸炎患者
2)5-ASA 製剤が効果不十分または不耐
3)適格性確認日前直近 3 日間における MMDAI※排便回数スコアの平均が 0~2 点の患者
4)適格性確認日前直近 3 日間における MMDAI※血便スコアの平均が 1~2 点かつすべての日
において 1 点以上の患者
5)適格性確認日の 2 週間前から適格性確認日までの間に実施した大腸内視鏡検査での MMDAI
※内視鏡所見スコアが 2 点と研究責任(分担)医師が判断した患者
6)適格性確認日において、潰瘍性大腸炎の診断から 12 週以上経過している患者
7)同意取得時の年齢が 16 歳以上
8)外来・入院:外来通院中の患者のみ
9)同意能力を有しており、本人の自由意思により文書同意の取得が可能な患者。なお、患者
の同意取得年齢が 18 歳未満の場合、代諾者からの同意も文書で得られる患者。
※Modified Mayo Disease Activity Index (MMDAI)
患者除外基準
1)本研究で使用する薬剤に対して重篤なアレルギーを有する患者
2)下記の薬物療法又は処置を、下記に示す期間内に実施した患者
・規定量を超える 5-ASA 製剤:適格性確認日前 4 週間
・ステロイド製剤(経口剤、注腸剤、坐剤、痔疾患治療剤、吸入剤、注射剤)
:適格性確認日
前 4 週間
・血球成分除去療法:適格性確認日前 4 週間
・免疫調節剤(シクロスポリン、タクロリムス、メトトレキサート、アザチオプリン、6-メ
ルカプトプリン):適格性確認日前 4 週間
・生物学的製剤:適格性確認日前 12 週間
・潰瘍性大腸炎治療目的の抗生物質、抗菌薬:適格性確認日前 3 カ月間
・止瀉剤:適格性確認日前 2 週間
・下痢型過敏性腸症候群治療剤:適格性確認日前 2 週間
・腸管洗浄剤(本研究のための大腸内視鏡検査の前処置での使用を除く)
:適格性確認日前 2
週間
・下剤(本研究のための大腸内視鏡検査の前処置での使用を除く):適格性確認日前 2 週間
・浣腸(本研究のための大腸内視鏡検査の前処置での使用を除く):適格性確認日前 2 週間
・生ワクチン:適格性確認日前 4 週間
30
「抗菌薬併用腸内細菌叢移植療法(A-FMT 療法)」の被験者の適格基準
及び選定方法(申請書類より抜粋)
5.被験者の適格基準及び選定方法
<患者適格性基準>
下記の選択基準を全て満たし、かつ除外基準のいずれにも該当しない研究対象者を対象と
する。
患者選択基準
1)活動期の左側・全大腸炎型の潰瘍性大腸炎患者
2)5-ASA 製剤が効果不十分または不耐
3)適格性確認日前直近 3 日間における MMDAI※排便回数スコアの平均が 0~2 点の患者
4)適格性確認日前直近 3 日間における MMDAI※血便スコアの平均が 1~2 点かつすべての日
において 1 点以上の患者
5)適格性確認日の 2 週間前から適格性確認日までの間に実施した大腸内視鏡検査での MMDAI
※内視鏡所見スコアが 2 点と研究責任(分担)医師が判断した患者
6)適格性確認日において、潰瘍性大腸炎の診断から 12 週以上経過している患者
7)同意取得時の年齢が 16 歳以上
8)外来・入院:外来通院中の患者のみ
9)同意能力を有しており、本人の自由意思により文書同意の取得が可能な患者。なお、患者
の同意取得年齢が 18 歳未満の場合、代諾者からの同意も文書で得られる患者。
※Modified Mayo Disease Activity Index (MMDAI)
患者除外基準
1)本研究で使用する薬剤に対して重篤なアレルギーを有する患者
2)下記の薬物療法又は処置を、下記に示す期間内に実施した患者
・規定量を超える 5-ASA 製剤:適格性確認日前 4 週間
・ステロイド製剤(経口剤、注腸剤、坐剤、痔疾患治療剤、吸入剤、注射剤)
:適格性確認日
前 4 週間
・血球成分除去療法:適格性確認日前 4 週間
・免疫調節剤(シクロスポリン、タクロリムス、メトトレキサート、アザチオプリン、6-メ
ルカプトプリン):適格性確認日前 4 週間
・生物学的製剤:適格性確認日前 12 週間
・潰瘍性大腸炎治療目的の抗生物質、抗菌薬:適格性確認日前 3 カ月間
・止瀉剤:適格性確認日前 2 週間
・下痢型過敏性腸症候群治療剤:適格性確認日前 2 週間
・腸管洗浄剤(本研究のための大腸内視鏡検査の前処置での使用を除く)
:適格性確認日前 2
週間
・下剤(本研究のための大腸内視鏡検査の前処置での使用を除く):適格性確認日前 2 週間
・浣腸(本研究のための大腸内視鏡検査の前処置での使用を除く):適格性確認日前 2 週間
・生ワクチン:適格性確認日前 4 週間
30