よむ、つかう、まなぶ。
薬-3○関係業界からの意見聴取について (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212451_00073.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第209回 9/20)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
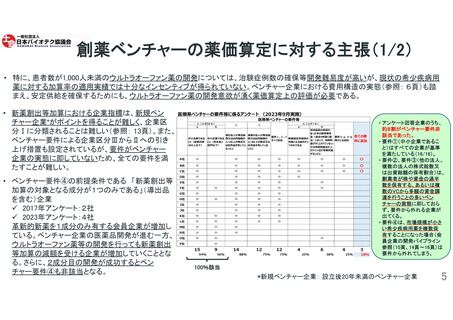
会員企業の海外開発の状況
国内市場だけでは投資コスト回収が期待できないため、海外先行開発を選択せざるを得な
い状況にある。薬価が期待できないことが一因である。
脳卒中後痙縮に対する筋弛緩薬貼付剤、がんに対す
るウイルスを用いた次世代治療薬、プリオン病治療薬、
根本的な治療法のない急性腎障害治療薬、etc.
行っている
9社
行っていない
6社
15社※
日本先行の開発品目が
ある
2社
海外先行の開発品目が
ある
7社
海外先行品目の日本での開発予定
あり
なし
3社(33%)4社(45%)
海外で先行開発を行う理由(サマリー)
日本での開発をためらう理由(サマリー)
薬価が期待できる。
製剤工夫等による付加価値が価格に反映されやすい。
海外であれば事業性が成立する患者数が見込める。
薬価水準の高い米国での開発を先行させ経営基盤の安
定化を図ることが合理的である。
• 臨床試験の質が高い。
• 市場性・事業性・先進性など。
• その他(薬価関連以外)
(参照: 12頁)
• 薬価がまったく期待できないこと。
• 製剤工夫による付加価値が価格に反映されにくい。
• 原価計算方式では低分子医薬品のようなものでは高薬
価になりにくい。
• 遺伝子治療などの新しい医薬品でも、既存の医薬品開
発と同様の治験と症例数が求められ、そのコストを十分に
償却できない薬価となった場合、開発コストの回収が見込
めず、承認申請に踏み切れないこともある。
• 日本での患者数では事業性が成立しない。
• 日本における臨床試験に係る課題。
• その他(薬価関連以外)
•
•
•
•
※会員企業で主に医薬品開発をおこなっている34社へのアンケートのうち、回答のあった15社
(参照: 12頁)
4
国内市場だけでは投資コスト回収が期待できないため、海外先行開発を選択せざるを得な
い状況にある。薬価が期待できないことが一因である。
脳卒中後痙縮に対する筋弛緩薬貼付剤、がんに対す
るウイルスを用いた次世代治療薬、プリオン病治療薬、
根本的な治療法のない急性腎障害治療薬、etc.
行っている
9社
行っていない
6社
15社※
日本先行の開発品目が
ある
2社
海外先行の開発品目が
ある
7社
海外先行品目の日本での開発予定
あり
なし
3社(33%)4社(45%)
海外で先行開発を行う理由(サマリー)
日本での開発をためらう理由(サマリー)
薬価が期待できる。
製剤工夫等による付加価値が価格に反映されやすい。
海外であれば事業性が成立する患者数が見込める。
薬価水準の高い米国での開発を先行させ経営基盤の安
定化を図ることが合理的である。
• 臨床試験の質が高い。
• 市場性・事業性・先進性など。
• その他(薬価関連以外)
(参照: 12頁)
• 薬価がまったく期待できないこと。
• 製剤工夫による付加価値が価格に反映されにくい。
• 原価計算方式では低分子医薬品のようなものでは高薬
価になりにくい。
• 遺伝子治療などの新しい医薬品でも、既存の医薬品開
発と同様の治験と症例数が求められ、そのコストを十分に
償却できない薬価となった場合、開発コストの回収が見込
めず、承認申請に踏み切れないこともある。
• 日本での患者数では事業性が成立しない。
• 日本における臨床試験に係る課題。
• その他(薬価関連以外)
•
•
•
•
※会員企業で主に医薬品開発をおこなっている34社へのアンケートのうち、回答のあった15社
(参照: 12頁)
4