よむ、つかう、まなぶ。
薬-3○関係業界からの意見聴取について (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212451_00073.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第209回 9/20)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
<具体的方策>
〇新規ベンチャー企業に対する評価
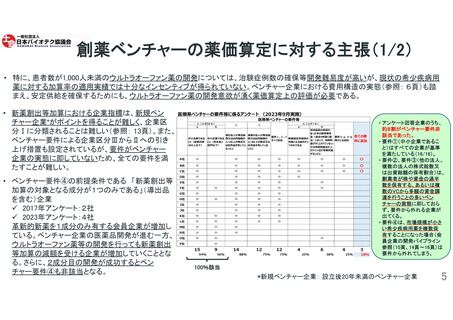
ベンチャー要件及び企業区分の見直し: ベンチャー要件につ
いて、実態に則さない要件②~④を撤廃し、要件①(中小企業
であること)のみを要件とする。また、新規ベンチャー企業が新
薬創出等加算の減額措置を受けないよう見直しを行う(参照:
5頁)。
ベンチャー体制整備補正(仮称)の新設: 大手製薬会社に比べて売上高研究開発費比率が高い創薬ベンチャーが承認取得をおこなっ
た医薬品で、原価計算方式が適用されるものについて、一般管理販売費比率をプラス補正する。(参照: 17~18頁)
〇開発難易度の高い品目に対する評価
ウルトラオーファン薬開発に対する評価: 大手製薬会社が手掛けない、希少疾病の中でも患者数が特に少ないウルトラオーファン(患者
数1,000人未満)の疾病に対する開発意欲が湧く薬価算定上の評価をする。(参照: 19頁)
〇その他の評価
医師主導治験等により効能追加した既収載品の加算対象の見直し: 難病・希少疾病用薬の開発に医師主導治験の果たす役割は大きく
(参照: 11頁)、資金的体力のないベンチャー企業は特に医師主導治験を活用しているが、現行ルールでは必ずしも加算が認められない
(参照: 20頁)。効能追加のイノベーション評価のために、企業の費用負担の程度に係わらず、加算要件を満たす追加効能の場合は加算
対象とする。
7
〇新規ベンチャー企業に対する評価
ベンチャー要件及び企業区分の見直し: ベンチャー要件につ
いて、実態に則さない要件②~④を撤廃し、要件①(中小企業
であること)のみを要件とする。また、新規ベンチャー企業が新
薬創出等加算の減額措置を受けないよう見直しを行う(参照:
5頁)。
ベンチャー体制整備補正(仮称)の新設: 大手製薬会社に比べて売上高研究開発費比率が高い創薬ベンチャーが承認取得をおこなっ
た医薬品で、原価計算方式が適用されるものについて、一般管理販売費比率をプラス補正する。(参照: 17~18頁)
〇開発難易度の高い品目に対する評価
ウルトラオーファン薬開発に対する評価: 大手製薬会社が手掛けない、希少疾病の中でも患者数が特に少ないウルトラオーファン(患者
数1,000人未満)の疾病に対する開発意欲が湧く薬価算定上の評価をする。(参照: 19頁)
〇その他の評価
医師主導治験等により効能追加した既収載品の加算対象の見直し: 難病・希少疾病用薬の開発に医師主導治験の果たす役割は大きく
(参照: 11頁)、資金的体力のないベンチャー企業は特に医師主導治験を活用しているが、現行ルールでは必ずしも加算が認められない
(参照: 20頁)。効能追加のイノベーション評価のために、企業の費用負担の程度に係わらず、加算要件を満たす追加効能の場合は加算
対象とする。
7