よむ、つかう、まなぶ。
○医薬品の新規薬価収載について 総-5-2 (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00223.html |
| 出典情報 | 中央社会保険医療協議会 総会(第564回 11/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
下痢
10.0(2)
2.6(1)
冠動脈狭窄
5.0(1)
2.6(1)
肝機能異常
5.0(1)
2.6(1)
咽頭炎
5.0(1)
2.6(1)
処置による疼痛
5.0(1)
2.6(1)
血中 CK 増加
5.0(1)
2.6(1)
2 型糖尿病
5.0(1)
2.6(1)
変形性関節症
5.0(1)
2.6(1)
そう痒症
5.0(1)
2.6(1)
不眠症
10.0(2)
0(0)
白内障
5.0(1)
0(0)
齲歯
5.0(1)
0(0)
注射部位疼痛
5.0(1)
0(0)
注射部位腫脹
5.0(1)
0(0)
造影剤アレルギー
5.0(1)
0(0)
扁桃炎
5.0(1)
0(0)
高カリウム血症
5.0(1)
0(0)
低血糖
5.0(1)
0(0)
関節炎
5.0(1)
0(0)
頭痛
5.0(1)
0(0)
喘息
5.0(1)
0(0)
汗疹
5.0(1)
0(0)
紫斑
5.0(1)
0(0)
%(例数)
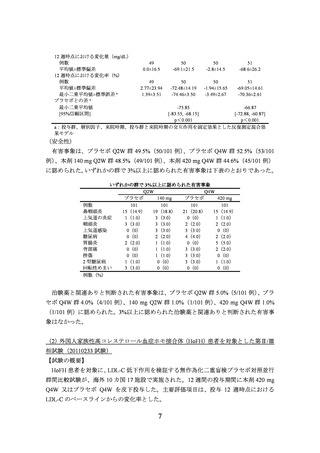
a:非盲検期は全ての群で本剤 140mgQ2W 又は本剤 420mgQ4W を投与
(4)心血管系疾患患者を対象とした心血管イベント抑制を評価した国際共同第Ⅲ相試
験(20110118 試験)
(添付文書改訂時に追記された試験成績)
【試験の概要】
スタチンで治療を受けている 40 歳以上 85 歳以下の心血管系疾患の既往を有する高
コレステロール血症患者を対象に、本剤の主要な心血管系イベント予防効果を検証する
ための無作為化二重盲検プラセボ対照並行群間比較試験が 1242(うち本邦 62)施設で
実施された。最大耐用量のスタチンとの併用にて、エボロクマブ 140mg を 2 週間に 1 回
若しくはエボロクマブ 420mg を 4 週間に 1 回、又はプラセボを 2 週間に 1 回若しくは
4 週間に 1 回投与した。主要評価項目は、心血管系疾患に起因する死亡、心筋梗塞、脳
卒中、冠動脈血行再建又は不安定狭心症による入院のいずれかが最初に発現するまでの
時間、重要な副次評価項目は、心血管系疾患に起因する死亡、心筋梗塞又は脳卒中のい
ずれかが最初に発現するまでの時間とした。
【結果】
有効性及び安全性の主要な解析対象集団は、プラセボ群 13780 例及び本剤群 13784 例
の計 27564 例であり、そのうち日本人はそれぞれ 225 例、204 例の計 429 例であった。
(有効性)
主要評価項目である、心血管系疾患に起因する死亡、心筋梗塞、脳卒中、冠動脈血行
12
10.0(2)
2.6(1)
冠動脈狭窄
5.0(1)
2.6(1)
肝機能異常
5.0(1)
2.6(1)
咽頭炎
5.0(1)
2.6(1)
処置による疼痛
5.0(1)
2.6(1)
血中 CK 増加
5.0(1)
2.6(1)
2 型糖尿病
5.0(1)
2.6(1)
変形性関節症
5.0(1)
2.6(1)
そう痒症
5.0(1)
2.6(1)
不眠症
10.0(2)
0(0)
白内障
5.0(1)
0(0)
齲歯
5.0(1)
0(0)
注射部位疼痛
5.0(1)
0(0)
注射部位腫脹
5.0(1)
0(0)
造影剤アレルギー
5.0(1)
0(0)
扁桃炎
5.0(1)
0(0)
高カリウム血症
5.0(1)
0(0)
低血糖
5.0(1)
0(0)
関節炎
5.0(1)
0(0)
頭痛
5.0(1)
0(0)
喘息
5.0(1)
0(0)
汗疹
5.0(1)
0(0)
紫斑
5.0(1)
0(0)
%(例数)
a:非盲検期は全ての群で本剤 140mgQ2W 又は本剤 420mgQ4W を投与
(4)心血管系疾患患者を対象とした心血管イベント抑制を評価した国際共同第Ⅲ相試
験(20110118 試験)
(添付文書改訂時に追記された試験成績)
【試験の概要】
スタチンで治療を受けている 40 歳以上 85 歳以下の心血管系疾患の既往を有する高
コレステロール血症患者を対象に、本剤の主要な心血管系イベント予防効果を検証する
ための無作為化二重盲検プラセボ対照並行群間比較試験が 1242(うち本邦 62)施設で
実施された。最大耐用量のスタチンとの併用にて、エボロクマブ 140mg を 2 週間に 1 回
若しくはエボロクマブ 420mg を 4 週間に 1 回、又はプラセボを 2 週間に 1 回若しくは
4 週間に 1 回投与した。主要評価項目は、心血管系疾患に起因する死亡、心筋梗塞、脳
卒中、冠動脈血行再建又は不安定狭心症による入院のいずれかが最初に発現するまでの
時間、重要な副次評価項目は、心血管系疾患に起因する死亡、心筋梗塞又は脳卒中のい
ずれかが最初に発現するまでの時間とした。
【結果】
有効性及び安全性の主要な解析対象集団は、プラセボ群 13780 例及び本剤群 13784 例
の計 27564 例であり、そのうち日本人はそれぞれ 225 例、204 例の計 429 例であった。
(有効性)
主要評価項目である、心血管系疾患に起因する死亡、心筋梗塞、脳卒中、冠動脈血行
12