よむ、つかう、まなぶ。
【参考資料5】海外で臨床開発が先行した医薬品の国際共同治験開始前の日本人での第Ⅰ相試験の実施に関する基本的考え方について (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_41120.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第16回 7/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
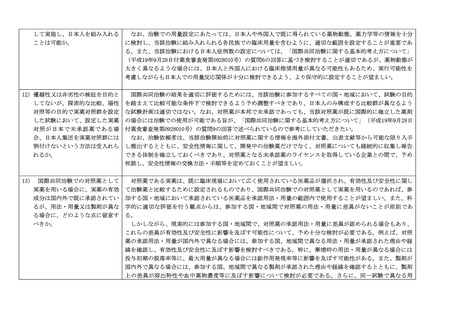
法・用量あるいは製剤を用いることによる盲検性担保への影響についても検討すべきである。
検討の結果から、対照薬の国内外での差異が有効性及び安全性に無視できない重大な影響を及ぼすと考えられ
る場合には、そのような薬剤を対照薬として設定することは避けるべきであり、本邦と同様の用法・用量及び製
剤で実施できる国・地域での治験を実施すること、あるいは別の薬剤を対照薬として設定すること等について検
討が必要である。
なお、国内での承認用法・用量とは異なるものの、国際的な教科書、診療ガイドライン等で既に用法・用量が
確立しており、国内の医療現場においても国際的な用法・用量が広く受け入れられている場合には、治験におけ
る用法・用量を国際的な用法・用量に合わせることが可能な場合もあると考えられる。個別のケースについて
は、対照薬の取り扱いも含めPMDAの対面助言で相談することが推奨される。
14) 治験薬と併用する既存薬の 効
国際共同治験は、様々な国・地域が参加して実施されるため、併用する既存薬の効能・効果や用法・用量が、
能・効果や用法・用量が国内外で
それぞれの国・地域における医療環境等により異なる可能性が想定される。したがって、併用する既存薬での差
異なる場合には、国際共同治験の
異が治験薬の有効性及び安全性に及ぼす影響について十分に検討した上で、国際共同治験を実施する国・地域を
実施は可能か。
適切に選択すべきである。
治験に参加する国・地域間で、併用する既存薬が治験薬の有効性又は安全性に影響を及ぼすことが明らかで、
治験薬の有効性及び安全性を評価するために、その既存薬の併用が必要であり、治験薬の使用時に効能・効果あ
るいは用法・用量等で併用薬についても明確に規定する必要がある場合(例:抗がん剤の併用療法等)には、併
用する既存薬の用法・用量について、国内外で統一することが望ましい。
一方で、治験に参加する国・地域間で併用する既存薬の効能・効果や用法・用量に差異があったとしても、必
ずしも治験薬との併用を前提としておらず、患者の状態によって適宜使用されるような場合(例:うつ病を対象
とした治験で併用される睡眠薬等)には、治験薬の有効性及び安全性の評価に大きな影響を及ぼさないことが科
学的根拠に基づき説明できることを前提とし、それらの国・地域において国際共同治験を実施することは可能と
考えられる。しかしながら、その場合にも、評価に与える影響を最小限とするため、治験中に併用する既存薬の
変更は不可とする等、可能な限り試験条件を統一すべきである。なお、治験実施後には、併用した既存薬での差
異が治験薬の有効性及び安全性にどのような影響を与えるのかについて、部分集団解析の実施が可能となるよ
う、治療内容、実施時期等の必要な情報を詳細に記録しておく必要がある。
検討の結果から、対照薬の国内外での差異が有効性及び安全性に無視できない重大な影響を及ぼすと考えられ
る場合には、そのような薬剤を対照薬として設定することは避けるべきであり、本邦と同様の用法・用量及び製
剤で実施できる国・地域での治験を実施すること、あるいは別の薬剤を対照薬として設定すること等について検
討が必要である。
なお、国内での承認用法・用量とは異なるものの、国際的な教科書、診療ガイドライン等で既に用法・用量が
確立しており、国内の医療現場においても国際的な用法・用量が広く受け入れられている場合には、治験におけ
る用法・用量を国際的な用法・用量に合わせることが可能な場合もあると考えられる。個別のケースについて
は、対照薬の取り扱いも含めPMDAの対面助言で相談することが推奨される。
14) 治験薬と併用する既存薬の 効
国際共同治験は、様々な国・地域が参加して実施されるため、併用する既存薬の効能・効果や用法・用量が、
能・効果や用法・用量が国内外で
それぞれの国・地域における医療環境等により異なる可能性が想定される。したがって、併用する既存薬での差
異なる場合には、国際共同治験の
異が治験薬の有効性及び安全性に及ぼす影響について十分に検討した上で、国際共同治験を実施する国・地域を
実施は可能か。
適切に選択すべきである。
治験に参加する国・地域間で、併用する既存薬が治験薬の有効性又は安全性に影響を及ぼすことが明らかで、
治験薬の有効性及び安全性を評価するために、その既存薬の併用が必要であり、治験薬の使用時に効能・効果あ
るいは用法・用量等で併用薬についても明確に規定する必要がある場合(例:抗がん剤の併用療法等)には、併
用する既存薬の用法・用量について、国内外で統一することが望ましい。
一方で、治験に参加する国・地域間で併用する既存薬の効能・効果や用法・用量に差異があったとしても、必
ずしも治験薬との併用を前提としておらず、患者の状態によって適宜使用されるような場合(例:うつ病を対象
とした治験で併用される睡眠薬等)には、治験薬の有効性及び安全性の評価に大きな影響を及ぼさないことが科
学的根拠に基づき説明できることを前提とし、それらの国・地域において国際共同治験を実施することは可能と
考えられる。しかしながら、その場合にも、評価に与える影響を最小限とするため、治験中に併用する既存薬の
変更は不可とする等、可能な限り試験条件を統一すべきである。なお、治験実施後には、併用した既存薬での差
異が治験薬の有効性及び安全性にどのような影響を与えるのかについて、部分集団解析の実施が可能となるよ
う、治療内容、実施時期等の必要な情報を詳細に記録しておく必要がある。