よむ、つかう、まなぶ。
【参考資料5】海外で臨床開発が先行した医薬品の国際共同治験開始前の日本人での第Ⅰ相試験の実施に関する基本的考え方について (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_41120.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第16回 7/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
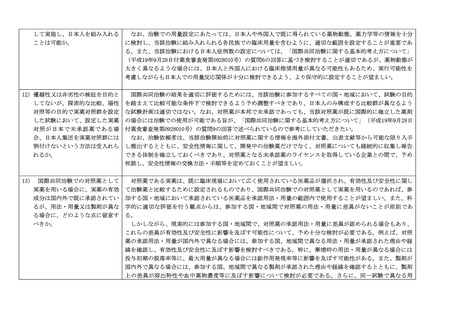
3.個別品目における判断の考え方
(1)希少疾患、難治性かつ重篤な疾患又は小児(成人開発の有無を問わな
い。)に用いる医薬品など、アンメットメディカルニーズが高く、日本で
の開発のために、実施予定又は実施中の国際共同治験への参加が望ましい
と考えられる場合は、適切なインフォームドコンセントを得た上で、日本
人第Ⅰ相試験を実施せずとも国際共同治験に参加できる。
(2)上記(1)以外の医薬品においても、例えば、非臨床データや海外で先
行する臨床試験における複数の人種での結果、類薬の情報を含めた既存の
知見、モデリング&シミュレーション等に基づき、薬物動態や反応(安全
性)が人種などの民族的要因の影響を受けやすいとは考えられないことな
どから、少なくとも日本人治験参加者の安全性が臨床的に許容・管理可能
であると判断できる場合には、日本人第Ⅰ相試験を実施せずとも国際共同
治験に参加できる。
一方、日本における患者数が多く、かつ、国際共同治験の実施までに日
本人第Ⅰ相試験を実施する時間が十分にあるなどの状況を踏まえ、日本人
第Ⅰ相試験の実施可能性があると治験依頼者が判断した場合には、日本人
第Ⅰ相試験の実施を検討すべきである。ただし、既存の情報から日本人に
おけるリスクが外国人におけるリスクを大きく上回らないと判断できる場
合やヒトでの安全域が広い場合は、この限りではない。
(3)上記(1)又は(2)のいずれの医薬品であっても、例えば抗がん剤な
どでみられるような、重篤な有害事象が高頻度に発現することが想定され、
安全域の狭い医薬品であり、かつ、年齢層や適応によらず日本人での投与
経験がない場合など安全性情報が限られている医薬品については、日本人
第Ⅰ相試験の要否についてより慎重に判断する必要がある。
4.その他
日本人第Ⅰ相試験の実施の有無にかかわらず、国際共同治験において日本
人の薬物動態・薬力学データを収集するなどして、承認申請までの間に、薬
物動態・薬力学の国内外差の検討を行うことが重要である。
日本人第Ⅰ相試験を実施しない場合であって、かつ治験依頼者が必要と判
断した場合には、国際共同治験において、日本人に対する追加の安全確保策
を設定する。
日本人第Ⅰ相試験の必要性及び国際共同治験における安全確保策の適切性
は、最終的には個別品目ごとに検討される必要があり、治験参加者の安全性
を確保する観点から PMDA が必要と判断した場合には、治験相談等において、
PMDA が日本人第Ⅰ相試験の必要性及び国際共同治験における日本人に対する
追加の安全確保策の実施又は変更等に係る指示又は助言を行う場合がある。
(1)希少疾患、難治性かつ重篤な疾患又は小児(成人開発の有無を問わな
い。)に用いる医薬品など、アンメットメディカルニーズが高く、日本で
の開発のために、実施予定又は実施中の国際共同治験への参加が望ましい
と考えられる場合は、適切なインフォームドコンセントを得た上で、日本
人第Ⅰ相試験を実施せずとも国際共同治験に参加できる。
(2)上記(1)以外の医薬品においても、例えば、非臨床データや海外で先
行する臨床試験における複数の人種での結果、類薬の情報を含めた既存の
知見、モデリング&シミュレーション等に基づき、薬物動態や反応(安全
性)が人種などの民族的要因の影響を受けやすいとは考えられないことな
どから、少なくとも日本人治験参加者の安全性が臨床的に許容・管理可能
であると判断できる場合には、日本人第Ⅰ相試験を実施せずとも国際共同
治験に参加できる。
一方、日本における患者数が多く、かつ、国際共同治験の実施までに日
本人第Ⅰ相試験を実施する時間が十分にあるなどの状況を踏まえ、日本人
第Ⅰ相試験の実施可能性があると治験依頼者が判断した場合には、日本人
第Ⅰ相試験の実施を検討すべきである。ただし、既存の情報から日本人に
おけるリスクが外国人におけるリスクを大きく上回らないと判断できる場
合やヒトでの安全域が広い場合は、この限りではない。
(3)上記(1)又は(2)のいずれの医薬品であっても、例えば抗がん剤な
どでみられるような、重篤な有害事象が高頻度に発現することが想定され、
安全域の狭い医薬品であり、かつ、年齢層や適応によらず日本人での投与
経験がない場合など安全性情報が限られている医薬品については、日本人
第Ⅰ相試験の要否についてより慎重に判断する必要がある。
4.その他
日本人第Ⅰ相試験の実施の有無にかかわらず、国際共同治験において日本
人の薬物動態・薬力学データを収集するなどして、承認申請までの間に、薬
物動態・薬力学の国内外差の検討を行うことが重要である。
日本人第Ⅰ相試験を実施しない場合であって、かつ治験依頼者が必要と判
断した場合には、国際共同治験において、日本人に対する追加の安全確保策
を設定する。
日本人第Ⅰ相試験の必要性及び国際共同治験における安全確保策の適切性
は、最終的には個別品目ごとに検討される必要があり、治験参加者の安全性
を確保する観点から PMDA が必要と判断した場合には、治験相談等において、
PMDA が日本人第Ⅰ相試験の必要性及び国際共同治験における日本人に対する
追加の安全確保策の実施又は変更等に係る指示又は助言を行う場合がある。