よむ、つかう、まなぶ。
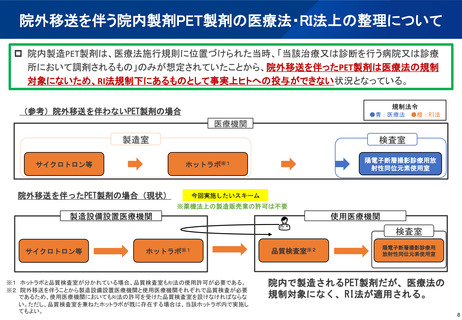
資料1 他の医療機関で製造されたPET製剤の使用に係る医療法上の取扱いについて (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53987.html |
| 出典情報 | 医療放射線の適正管理に関する検討会(第4回 3/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
既存の製造ガイドライン等の遵守・運搬時の品質管理
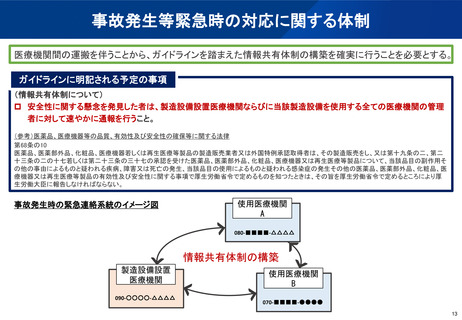
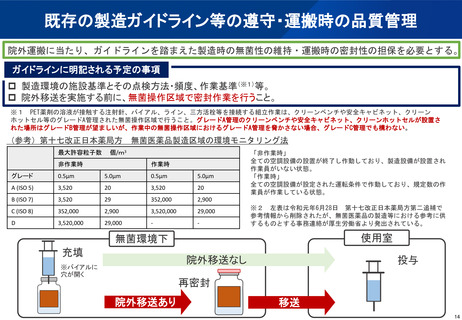
院外運搬に当たり、ガイドラインを踏まえた製造時の無菌性の維持・運搬時の密封性の担保を必要とする。
ガイドラインに明記される予定の事項
製造環境の施設基準とその点検方法・頻度、作業基準(※1)等。
院外移送を実施する前に、無菌操作区域で密封作業を行うこと。
※1 PET薬剤の溶液が接触する注射針、バイアル、ライン、三方活栓等を接続する組立作業は、クリーンベンチや安全キャビネット、クリーン
ホットセル等のグレードA管理された無菌操作区域で行うこと。グレードA管理のクリーンベンチや安全キャビネット、クリーンホットセルが設置さ
れた場所はグレードB管理が望ましいが、作業中の無菌操作区域におけるグレードA管理を脅かさない場合、グレードC管理でも構わない。
(参考)第十七改正日本薬局方 無菌医薬品製造区域の環境モニタリング法
最大許容粒子数
個/m3
非作業時
作業時
グレード
0.5µm
5.0µm
0.5µm
5.0µm
A (ISO 5)
3,520
20
3,520
20
B (ISO 7)
3,520
29
352,000
2,900
C (ISO 8)
352,000
2,900
3,520,000
29,000
D
3,520,000
29,000
-
-
「非作業時」
全ての空調設備の設置が終了し作動しており、製造設備が設置され
作業員がいない状態。
「作業時」
全ての空調設備が設定された運転条件で作動しており、規定数の作
業員が作業している状態。
※2 左表は令和元年6月28日 第十七改正日本薬局方第二追補で
参考情報から削除されたが、無菌医薬品の製造等における参考に供
するものとする事務連絡が厚生労働省より発出されている。
使用室
無菌環境下
充填
院外移送なし
※バイアルに
穴が開く
投与
再密封
院外移送あり
移送
14
院外運搬に当たり、ガイドラインを踏まえた製造時の無菌性の維持・運搬時の密封性の担保を必要とする。
ガイドラインに明記される予定の事項
製造環境の施設基準とその点検方法・頻度、作業基準(※1)等。
院外移送を実施する前に、無菌操作区域で密封作業を行うこと。
※1 PET薬剤の溶液が接触する注射針、バイアル、ライン、三方活栓等を接続する組立作業は、クリーンベンチや安全キャビネット、クリーン
ホットセル等のグレードA管理された無菌操作区域で行うこと。グレードA管理のクリーンベンチや安全キャビネット、クリーンホットセルが設置さ
れた場所はグレードB管理が望ましいが、作業中の無菌操作区域におけるグレードA管理を脅かさない場合、グレードC管理でも構わない。
(参考)第十七改正日本薬局方 無菌医薬品製造区域の環境モニタリング法
最大許容粒子数
個/m3
非作業時
作業時
グレード
0.5µm
5.0µm
0.5µm
5.0µm
A (ISO 5)
3,520
20
3,520
20
B (ISO 7)
3,520
29
352,000
2,900
C (ISO 8)
352,000
2,900
3,520,000
29,000
D
3,520,000
29,000
-
-
「非作業時」
全ての空調設備の設置が終了し作動しており、製造設備が設置され
作業員がいない状態。
「作業時」
全ての空調設備が設定された運転条件で作動しており、規定数の作
業員が作業している状態。
※2 左表は令和元年6月28日 第十七改正日本薬局方第二追補で
参考情報から削除されたが、無菌医薬品の製造等における参考に供
するものとする事務連絡が厚生労働省より発出されている。
使用室
無菌環境下
充填
院外移送なし
※バイアルに
穴が開く
投与
再密封
院外移送あり
移送
14