よむ、つかう、まなぶ。
資料1 他の医療機関で製造されたPET製剤の使用に係る医療法上の取扱いについて (19 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53987.html |
| 出典情報 | 医療放射線の適正管理に関する検討会(第4回 3/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
原子力規制委員会が指定する放射性同位元素等の規制に関する法律の適用を受けないもの
放射性同位元素等の規制に関する法律における未承認放射性医薬品等の取扱いについて(令和4年12月
23日付け医政地発1223第5号・薬生機審発1223第1号・原規放発第2212231号)(抄)
第1 改正の概要
1 RI法適用除外規定の構造の見直し
今後の医療分野における新たな放射線診療技術の開発・導入や、医療制度の枠組の変更等に応じ、迅速かつ適切に放射性同位元素等
の規制に関する法律(昭和32年法律第167号。以下「RI法」という。)の適用除外対象を変更することを可能とするため、放射性同
位元素等の規制に関する法律施行令(昭和35年政令第259号。以下「RI政令」という。)の規定の構造の見直しを行い、改正政令に
よる改正後のRI政令第1条第2号に規定する法律及びそれらに基づく命令によりRI法及びこれに基づく命令と同等の放射線防護に係
る規制を受けるものを、RI法の適用除外対象とし、その具体的な対象については、告示で指定することとする。これに伴い、「放
射性同位元素等の規制に関する法律施行令第1条第5号の医療機器を指定する告示」(平成17年文部科学省告示第76号)及び「放射性
同位元素等の規制に関する法律施行令第1条第4号の薬物を指定する告示」(平成17年文部科学省告示第140号)は廃止する。
2 未承認放射性医薬品等1に関する規制の合理化
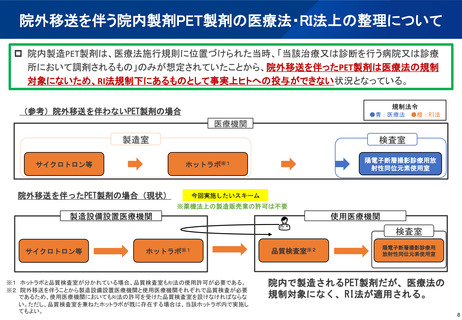
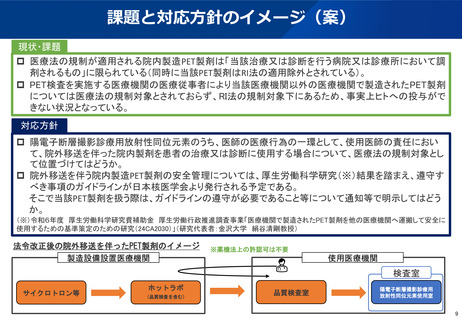
医療法施行規則の一部を改正する省令(平成31年厚生労働省令第21号)により、医療法(昭和23年法律第205号)第1条の5第1項に規
定する病院又は同条第2項に規定する診療所(以下「病院等」という。)に備えられた未承認放射性医薬品等について、医療法に基づ
く放射線防護に係る規制の対象となった。これを踏まえ、当該未承認放射性医薬品等については、RI法及びこれに基づく命令の規
定による規制と同等の規制を受けるものとして、RI法の適用を除外する。
3 体外診断用放射性医薬品の原料又は材料に関する規制の明確化
薬事法等の一部を改正する法律(平成25年法律第84号)2により、それまで製造業の許可の対象であった体外診断用医薬品は、新たに
設けられた登録制度により管理されることとなったところ、当該制度に係る登録製造所3に存する体外診断用放射性医薬品の原料又
は材料について、RI法の適用を除外する。
4 放射性治験薬の運搬に関する適用法令の明確化
放射性治験薬4の製造所から病院等までの運搬は、改正政令による改正後のRI政令第1条第2号に規定する法律及びそれらに基づく命
令によりRI法と同等の放射線防護に係る規制を受けているものではなく、RI法が適用されることを明確化する。
19
放射性同位元素等の規制に関する法律における未承認放射性医薬品等の取扱いについて(令和4年12月
23日付け医政地発1223第5号・薬生機審発1223第1号・原規放発第2212231号)(抄)
第1 改正の概要
1 RI法適用除外規定の構造の見直し
今後の医療分野における新たな放射線診療技術の開発・導入や、医療制度の枠組の変更等に応じ、迅速かつ適切に放射性同位元素等
の規制に関する法律(昭和32年法律第167号。以下「RI法」という。)の適用除外対象を変更することを可能とするため、放射性同
位元素等の規制に関する法律施行令(昭和35年政令第259号。以下「RI政令」という。)の規定の構造の見直しを行い、改正政令に
よる改正後のRI政令第1条第2号に規定する法律及びそれらに基づく命令によりRI法及びこれに基づく命令と同等の放射線防護に係
る規制を受けるものを、RI法の適用除外対象とし、その具体的な対象については、告示で指定することとする。これに伴い、「放
射性同位元素等の規制に関する法律施行令第1条第5号の医療機器を指定する告示」(平成17年文部科学省告示第76号)及び「放射性
同位元素等の規制に関する法律施行令第1条第4号の薬物を指定する告示」(平成17年文部科学省告示第140号)は廃止する。
2 未承認放射性医薬品等1に関する規制の合理化
医療法施行規則の一部を改正する省令(平成31年厚生労働省令第21号)により、医療法(昭和23年法律第205号)第1条の5第1項に規
定する病院又は同条第2項に規定する診療所(以下「病院等」という。)に備えられた未承認放射性医薬品等について、医療法に基づ
く放射線防護に係る規制の対象となった。これを踏まえ、当該未承認放射性医薬品等については、RI法及びこれに基づく命令の規
定による規制と同等の規制を受けるものとして、RI法の適用を除外する。
3 体外診断用放射性医薬品の原料又は材料に関する規制の明確化
薬事法等の一部を改正する法律(平成25年法律第84号)2により、それまで製造業の許可の対象であった体外診断用医薬品は、新たに
設けられた登録制度により管理されることとなったところ、当該制度に係る登録製造所3に存する体外診断用放射性医薬品の原料又
は材料について、RI法の適用を除外する。
4 放射性治験薬の運搬に関する適用法令の明確化
放射性治験薬4の製造所から病院等までの運搬は、改正政令による改正後のRI政令第1条第2号に規定する法律及びそれらに基づく命
令によりRI法と同等の放射線防護に係る規制を受けているものではなく、RI法が適用されることを明確化する。
19