よむ、つかう、まなぶ。
08 参考資料1-2 沈降ヘモフィルスb型ワクチンファクトシート[2.4MB] (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34803.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第20回 8/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
ワクチンの有効性
VaxemHib は ActHib と同程度の免疫原性をもつことが、
国内の臨床試験によって示されている。
VaxemHib 接種群、ActHib 接種群ともに、4 回のワクチン接種(初回免疫 3 回と追加免疫 1 回、
沈降百日咳ジフテリア破傷風混合ワクチンと同時接種)を受けた被験者の 99%以上が、抗 PRP IgG
抗体を Hib 感染症の長期防御レベルとされる 1.0μg/mL 以上の濃度で保有していた。VaxemHib
の免疫原性は中国、トルコ、タイ、南アフリカでの検討でも、他の Hib ワクチン製剤と同程度
であると報告されている。
ワクチン製剤の互換性
VaxemHib と ActHib の 2 製剤について交差接種を検討した論文報告はないが、世界保健機関
(World Health Organization: WHO)の事前承認審査 (prequalification)における VaxemHib の
添付文書(英語版)では「追加免疫」の項目に、「初回接種に VaxemHib を使用した者は、追加
接種として VaxemHib または他の Hib 結合体ワクチンが使用可能であり、同様に初回接種で他の
Hib ワクチンを接種した者には追加接種で VaxemHib の使用が可能」としている。また韓国では
VaxemHib、ActHib を含む 5 種類のワクチン製剤が使用されており、全接種件数の 14〜19%がこ
れら 5 種のワクチンの交差接種で行われている。
韓国で VaxemHib は 2009 年から使用されおり、
それ以降も韓国における Hib 感染症の動向には変化が認められていないため、他の Hib ワクチ
ンと VaxemHib の交差接種を行なっても Hib 感染症の防御効果には影響がないと考えられる。
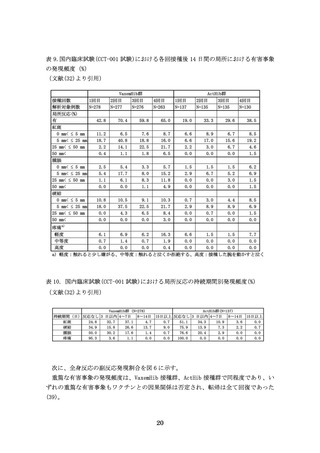
ワクチンの安全性について
国内第Ⅰ相臨床試験では、副反応の発現頻度は 94.3%(33/35 例)で、接種局所の発赤・硬結・
腫脹・疼痛、下痢、発疹、発熱、傾眠などがあった。ワクチンによる死亡等重篤な有害事象は
認められなかった。第Ⅲ相臨床試験では、国内ですでに承認され使用されている DPT ワクチン
を同時接種した際の副反応の発生頻度を ActHib と比較した。副反応の発現頻度は、VaxemHib 接
種群 82.4%(229/278 例)、ActHib 接種群 62.0%(84/137 例)と、VaxemHib の方が副反応の発
生頻度が高い傾向にあった。主な副反応は接種部位の紅斑・硬結・腫脹などであり、その発生
頻度について、VaxemHib は ActHib より高い傾向にあったものの、DPT ワクチン単独接種と比較
した場合、VaxemHib と DPT ワクチンはいずれも同程度だった。また、ワクチン接種後の重篤な
有害事象は認められなかった。
2
VaxemHib は ActHib と同程度の免疫原性をもつことが、
国内の臨床試験によって示されている。
VaxemHib 接種群、ActHib 接種群ともに、4 回のワクチン接種(初回免疫 3 回と追加免疫 1 回、
沈降百日咳ジフテリア破傷風混合ワクチンと同時接種)を受けた被験者の 99%以上が、抗 PRP IgG
抗体を Hib 感染症の長期防御レベルとされる 1.0μg/mL 以上の濃度で保有していた。VaxemHib
の免疫原性は中国、トルコ、タイ、南アフリカでの検討でも、他の Hib ワクチン製剤と同程度
であると報告されている。
ワクチン製剤の互換性
VaxemHib と ActHib の 2 製剤について交差接種を検討した論文報告はないが、世界保健機関
(World Health Organization: WHO)の事前承認審査 (prequalification)における VaxemHib の
添付文書(英語版)では「追加免疫」の項目に、「初回接種に VaxemHib を使用した者は、追加
接種として VaxemHib または他の Hib 結合体ワクチンが使用可能であり、同様に初回接種で他の
Hib ワクチンを接種した者には追加接種で VaxemHib の使用が可能」としている。また韓国では
VaxemHib、ActHib を含む 5 種類のワクチン製剤が使用されており、全接種件数の 14〜19%がこ
れら 5 種のワクチンの交差接種で行われている。
韓国で VaxemHib は 2009 年から使用されおり、
それ以降も韓国における Hib 感染症の動向には変化が認められていないため、他の Hib ワクチ
ンと VaxemHib の交差接種を行なっても Hib 感染症の防御効果には影響がないと考えられる。
ワクチンの安全性について
国内第Ⅰ相臨床試験では、副反応の発現頻度は 94.3%(33/35 例)で、接種局所の発赤・硬結・
腫脹・疼痛、下痢、発疹、発熱、傾眠などがあった。ワクチンによる死亡等重篤な有害事象は
認められなかった。第Ⅲ相臨床試験では、国内ですでに承認され使用されている DPT ワクチン
を同時接種した際の副反応の発生頻度を ActHib と比較した。副反応の発現頻度は、VaxemHib 接
種群 82.4%(229/278 例)、ActHib 接種群 62.0%(84/137 例)と、VaxemHib の方が副反応の発
生頻度が高い傾向にあった。主な副反応は接種部位の紅斑・硬結・腫脹などであり、その発生
頻度について、VaxemHib は ActHib より高い傾向にあったものの、DPT ワクチン単独接種と比較
した場合、VaxemHib と DPT ワクチンはいずれも同程度だった。また、ワクチン接種後の重篤な
有害事象は認められなかった。
2