よむ、つかう、まなぶ。
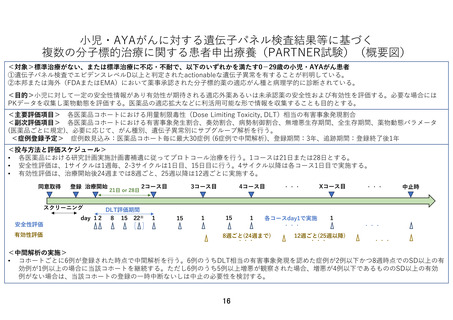
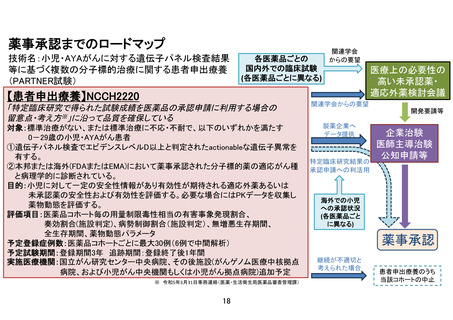
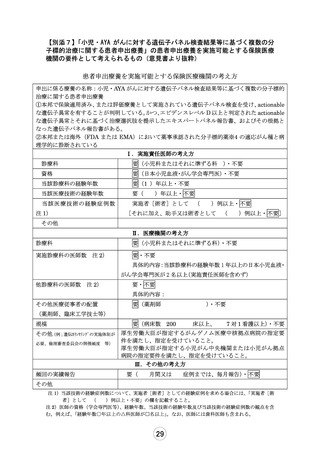
別紙1○「小児・AYAがんに対する遺伝子パネル検査結果等に基づく複数の分子標的治療に関する患者申出療養」の患者申出療養評価会議における事前評価等の取扱いについて (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000203222_00026.html |
| 出典情報 | 患者申出療養評価会議(第43回 9/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
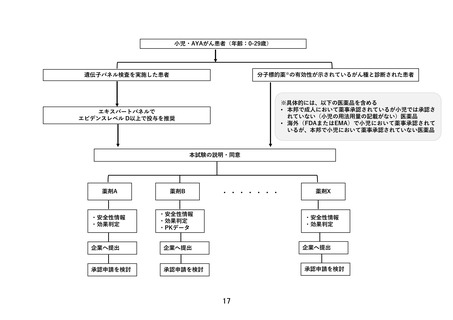
小児・AYAがん患者(年齢:0-29歳)
分子標的薬※の有効性が示されているがん種と診断された患者
遺伝子パネル検査を実施した患者
※具体的には、以下の医薬品を含める
• 本邦で成人において薬事承認されているが小児では承認さ
れていない(小児の用法用量の記載がない)医薬品
• 海外(FDAまたはEMA)で小児において薬事承認されて
いるが、本邦で小児において薬事承認されていない医薬品
エキスパートパネルで
エビデンスレベル D以上で投与を推奨
本試験の説明・同意
・・・・・・・
薬剤A
薬剤B
薬剤X
・安全性情報
・効果判定
・安全性情報
・効果判定
・PKデータ
企業へ提出
企業へ提出
企業へ提出
承認申請を検討
承認申請を検討
承認申請を検討
・安全性情報
・効果判定
17
分子標的薬※の有効性が示されているがん種と診断された患者
遺伝子パネル検査を実施した患者
※具体的には、以下の医薬品を含める
• 本邦で成人において薬事承認されているが小児では承認さ
れていない(小児の用法用量の記載がない)医薬品
• 海外(FDAまたはEMA)で小児において薬事承認されて
いるが、本邦で小児において薬事承認されていない医薬品
エキスパートパネルで
エビデンスレベル D以上で投与を推奨
本試験の説明・同意
・・・・・・・
薬剤A
薬剤B
薬剤X
・安全性情報
・効果判定
・安全性情報
・効果判定
・PKデータ
企業へ提出
企業へ提出
企業へ提出
承認申請を検討
承認申請を検討
承認申請を検討
・安全性情報
・効果判定
17