よむ、つかう、まなぶ。
【資料1】「後発医薬品の安定供給等の実現に向けた産業構造のあり方に関する検討会」を踏まえた本会議の検討事項について➂ (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40170.html |
| 出典情報 | 医療用医薬品の安定確保策に関する関係者会議(第13回 5/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
対策の方向性
3
3持続可能な産業構造
第12回「後発医薬品の安定供給等の実現に向
けた産業構造のあり方に関する検討会」資料
(報告書案)を抜粋したもの
持続可能な産業構造
(既収載品目の市場からの撤退のための薬価削除等プロセスの明確化・簡素化)
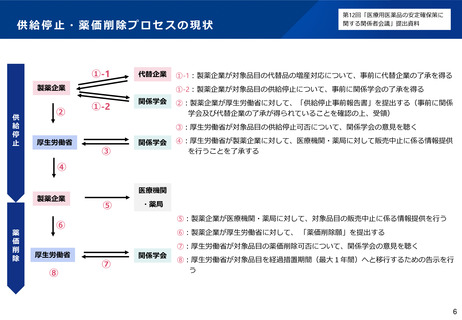
○ また、既収載品目を統合し、一方の品目が市場から撤退する際の供給停止や薬価削除については、製薬企業か
らの供給停止事前報告書の提出や医療現場における医療上の必要性の確認等のプロセスを経る必要がある。
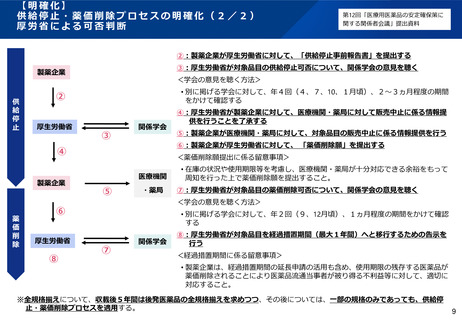
○ このため、関係学会や製薬企業双方の負担軽減も考慮し、供給停止・薬価削除プロセスについて、少量多品目
生産の適正化の観点からプロセスの明確化を図るとともに、一定の条件の下で簡素化するなどの方策について、
「医療用医薬品の安定確保策に関する関係者会議」において検討を行うべきである。
○ その際、供給停止・薬価削除プロセスの明確化・簡素化の具体策の検討に当たっては、代替品やシェアの状況
を踏まえた医療上の必要性や後発医薬品の流通に与える影響に留意すべきである。
(規格揃え原則の合理化)
○ 薬価基準への収載を希望する後発医薬品については、その承認に当たって標準製剤となった先発品(以下「標
準先発品」という。)が有する規格を、全て揃えて薬価基準収載することが求められている 。標準先発品が有す
る規格で、医療上必ずしも必要でないと考える規格がある場合には、製薬企業の報告に基づき個別に判断するこ
ととされている。
○ 規格揃え原則については、需要の少ない規格(非汎用規格)もあるが、製造技術上少量の生産が困難であるこ
とから、一定の廃棄数量分を含んだ製造がなされており、赤字品目となっている製品がある。
○ このため、後発医薬品の薬価収載時は全規格を取り揃えることを原則としつつ、安定供給が求められる収載後
5年間を経過した後は、医療現場での使用状況を踏まえ、医療上の必要性等に照らして全規格を取り揃えること
が必ずしも必要ではないと考えられる品目について、一部の規格のみであっても供給停止・薬価削除プロセスを
適用できるようにすることを検討すべきである。また、薬価収載後5年を待たず、薬価収載時に医療上必ずしも
必要でないと考える規格がある場合の取扱いを明確化することも検討すべきである。口腔崩壊錠(OD錠)につ
いてもこの中で検討するべきである。なお、全規格を取り揃える企業とそうでない企業が出てくることから、企
業ごとに有利不利が生じないよう配慮が必要であるとともに、規格が揃わないことにより医療現場での調剤に影
響が生じないようにすべきである。
4
3
3持続可能な産業構造
第12回「後発医薬品の安定供給等の実現に向
けた産業構造のあり方に関する検討会」資料
(報告書案)を抜粋したもの
持続可能な産業構造
(既収載品目の市場からの撤退のための薬価削除等プロセスの明確化・簡素化)
○ また、既収載品目を統合し、一方の品目が市場から撤退する際の供給停止や薬価削除については、製薬企業か
らの供給停止事前報告書の提出や医療現場における医療上の必要性の確認等のプロセスを経る必要がある。
○ このため、関係学会や製薬企業双方の負担軽減も考慮し、供給停止・薬価削除プロセスについて、少量多品目
生産の適正化の観点からプロセスの明確化を図るとともに、一定の条件の下で簡素化するなどの方策について、
「医療用医薬品の安定確保策に関する関係者会議」において検討を行うべきである。
○ その際、供給停止・薬価削除プロセスの明確化・簡素化の具体策の検討に当たっては、代替品やシェアの状況
を踏まえた医療上の必要性や後発医薬品の流通に与える影響に留意すべきである。
(規格揃え原則の合理化)
○ 薬価基準への収載を希望する後発医薬品については、その承認に当たって標準製剤となった先発品(以下「標
準先発品」という。)が有する規格を、全て揃えて薬価基準収載することが求められている 。標準先発品が有す
る規格で、医療上必ずしも必要でないと考える規格がある場合には、製薬企業の報告に基づき個別に判断するこ
ととされている。
○ 規格揃え原則については、需要の少ない規格(非汎用規格)もあるが、製造技術上少量の生産が困難であるこ
とから、一定の廃棄数量分を含んだ製造がなされており、赤字品目となっている製品がある。
○ このため、後発医薬品の薬価収載時は全規格を取り揃えることを原則としつつ、安定供給が求められる収載後
5年間を経過した後は、医療現場での使用状況を踏まえ、医療上の必要性等に照らして全規格を取り揃えること
が必ずしも必要ではないと考えられる品目について、一部の規格のみであっても供給停止・薬価削除プロセスを
適用できるようにすることを検討すべきである。また、薬価収載後5年を待たず、薬価収載時に医療上必ずしも
必要でないと考える規格がある場合の取扱いを明確化することも検討すべきである。口腔崩壊錠(OD錠)につ
いてもこの中で検討するべきである。なお、全規格を取り揃える企業とそうでない企業が出てくることから、企
業ごとに有利不利が生じないよう配慮が必要であるとともに、規格が揃わないことにより医療現場での調剤に影
響が生じないようにすべきである。
4