よむ、つかう、まなぶ。
資料1-2 オキシメタゾリン塩酸塩・クロルフェニラミンマレイン酸塩のリスク評価について[2.9MB] (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_42464.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会安全対策調査会(令和6年度第5回 8/28)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別紙(1)
調査結果の概要
本剤の当該調査期間(令和 3 年 9 月 13 日~令和 6 年 7 月 19 日)
における調査結果を以下の通り示す。
(1)副作用頻度調査
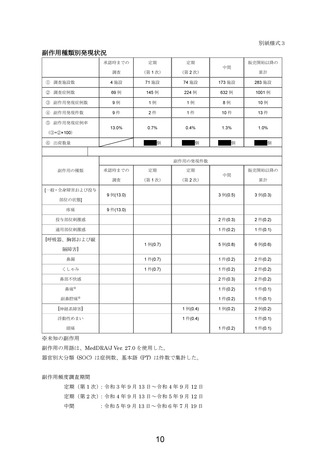
当該調査期間にモニター施設 283 施設から報告された 1001 症例において、副作用発現症例数
は 10 例(副作用発現症例率 1.0%)で、副作用発現件数は 13 件であった。内訳は、既知・非重
篤の副作用が「鼻漏」
(2 件)、
「くしゃみ」
(2 件)
、「鼻部不快感」
(2 件)、
「投与部位刺激感」
(2
件)、
「浮動性めまい」
(1 件)
、
「頭痛」
(1 件)、
「適用部位刺激感」
(1 件)
、未知・非重篤の副作用
が「副鼻腔痛」
(1 件)、
「鼻痛」(1 件)であった。重篤な副作用は認められなかった。
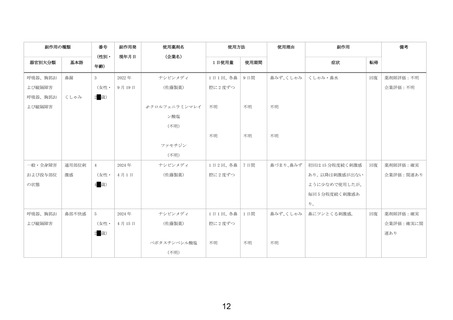
副作用の種類別発現状況は別紙様式3、4に示す通りである。
(2)一般調査
当該調査期間に報告された副作用発現症例はなかった。
(3)研究報告および外国での規制措置情報
当該調査期間に研究報告および外国措置報告の対象となるものはなかった。
(4)適正使用状況
使用目的について、本剤の効能・効果の範囲内で使用された症例は 944 例(94.3%)であった。
一方、本剤の効能・効果の範囲外で使用(鼻づまりの症状がない状態で使用)された症例が 57 例
(5.7%)であった。
薬剤師への追加で聴き取りを行った結果、上記 57 例中 43 例から回答が得られ、そのうち「販
売時に使用者に鼻づまりがあることを確認した」と回答したのは 40 例であった。一方、
「販売時
に使用者に鼻づまりがあることを確認しなかった」と回答したのは 3 例であった。
なお、鼻づまりがなく使用した症例の内、4 例に副作用が認められた。認められた事象は「鼻
漏」、
「くしゃみ」、
「鼻部不快感」、
「投与部位刺激感」
、
「頭痛」であり、いずれの副作用も既知・
非重篤であった。
使用期間について、用法・用量の範囲内で使用された症例は 915 例(91.4%)であった。一方、
1 週間を超えて使用された症例が 86 例(8.6%)であった。
86 例の具体的な使用期間は、8 日間(4 例)
、9 日間(2 例)
、10 日間(29 例)、12 日間(1 例)、
13 日間(2 例)
、14 日間(33 例)
、20 日間(7 例)
、21 日間(1 例)
、24 日間(1 例)
、25 日間(1
例)
、30 日間(4 例)
、1 カ月(1 例)であった。
薬剤師への聞き取りを追加で行った結果、理由・経緯について 86 例中 59 例から回答が得られ、
主な理由は以下の通りであった。
・ 毎日ではなく症状が出るたびに使用し、使用していなかった期間も含めて使用期間を記載し
たため、1 週間を超えてしまった(44 例)
。
8
調査結果の概要
本剤の当該調査期間(令和 3 年 9 月 13 日~令和 6 年 7 月 19 日)
における調査結果を以下の通り示す。
(1)副作用頻度調査
当該調査期間にモニター施設 283 施設から報告された 1001 症例において、副作用発現症例数
は 10 例(副作用発現症例率 1.0%)で、副作用発現件数は 13 件であった。内訳は、既知・非重
篤の副作用が「鼻漏」
(2 件)、
「くしゃみ」
(2 件)
、「鼻部不快感」
(2 件)、
「投与部位刺激感」
(2
件)、
「浮動性めまい」
(1 件)
、
「頭痛」
(1 件)、
「適用部位刺激感」
(1 件)
、未知・非重篤の副作用
が「副鼻腔痛」
(1 件)、
「鼻痛」(1 件)であった。重篤な副作用は認められなかった。
副作用の種類別発現状況は別紙様式3、4に示す通りである。
(2)一般調査
当該調査期間に報告された副作用発現症例はなかった。
(3)研究報告および外国での規制措置情報
当該調査期間に研究報告および外国措置報告の対象となるものはなかった。
(4)適正使用状況
使用目的について、本剤の効能・効果の範囲内で使用された症例は 944 例(94.3%)であった。
一方、本剤の効能・効果の範囲外で使用(鼻づまりの症状がない状態で使用)された症例が 57 例
(5.7%)であった。
薬剤師への追加で聴き取りを行った結果、上記 57 例中 43 例から回答が得られ、そのうち「販
売時に使用者に鼻づまりがあることを確認した」と回答したのは 40 例であった。一方、
「販売時
に使用者に鼻づまりがあることを確認しなかった」と回答したのは 3 例であった。
なお、鼻づまりがなく使用した症例の内、4 例に副作用が認められた。認められた事象は「鼻
漏」、
「くしゃみ」、
「鼻部不快感」、
「投与部位刺激感」
、
「頭痛」であり、いずれの副作用も既知・
非重篤であった。
使用期間について、用法・用量の範囲内で使用された症例は 915 例(91.4%)であった。一方、
1 週間を超えて使用された症例が 86 例(8.6%)であった。
86 例の具体的な使用期間は、8 日間(4 例)
、9 日間(2 例)
、10 日間(29 例)、12 日間(1 例)、
13 日間(2 例)
、14 日間(33 例)
、20 日間(7 例)
、21 日間(1 例)
、24 日間(1 例)
、25 日間(1
例)
、30 日間(4 例)
、1 カ月(1 例)であった。
薬剤師への聞き取りを追加で行った結果、理由・経緯について 86 例中 59 例から回答が得られ、
主な理由は以下の通りであった。
・ 毎日ではなく症状が出るたびに使用し、使用していなかった期間も含めて使用期間を記載し
たため、1 週間を超えてしまった(44 例)
。
8