よむ、つかう、まなぶ。
参考資料3:「創薬力の向上により国民に最新の医薬品を迅速に届けるための構想会議」中間とりまとめを踏まえた政策目標と工程表 (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43236.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第36回 9/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
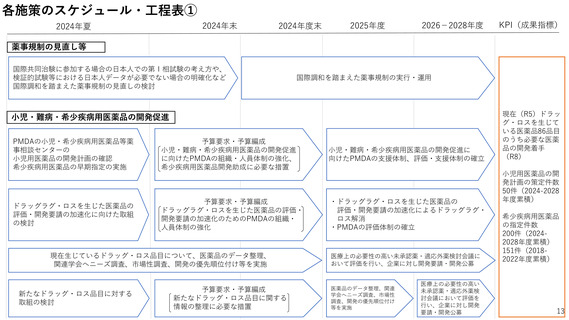
2ー2.小児・難病・希少疾病用医薬品の開発促進
<施策の目的>
成果指標・KPI
小児用医薬品や難病・希少疾病用医薬品は、医療ニーズが高いにもかかわらず、
市場規模が小さいこと等によりドラッグ・ロスが生じやすい。
企業による開発を促すため、薬事規制当局においても積極的な支援が必要。
<現状>
ドラッグロスを生
じている医薬品:
86品目(R5)
<目標>
左記品目のうち必要
な医薬品について開
発着手(R8まで)
<施策の内容>
採算性の乏しい小児用医薬品・難病・希少疾病用医薬品の開
発の促進
参考資料
PMDAに小児・希少疾病用医薬品等薬事相談センターを
令和6年度に設置し、以下の取組を進める。
企業が成人を対象とした医薬品の開発を行う場合、併
せて小児用医薬品の開発計画を策定し、PMDAの確認を
受ける仕組みを導入・運用。
すでに決定した希少疾病用医薬品の指定の早期化につ
いて、その確実な運用。
小児・希少疾病用医薬品等薬事相談センター
①希少疾病用医薬品
指定・指定見直し
の相談・審査
②小児用医薬品
開発計画の確認・
進捗管理
③未承認薬検討会議
評価の加速 (調査、
評価書作成等)
PMDA相談手数料を補助
対象:上記①・②に関して企業が支払う相談手数料。未承認薬等検討会
議での開発公募品や医師主導治験による開発品。
「医療上の必要性の高い未承認薬・適応外薬検討会議」
における評価、開発要請等の加速化。
33
<施策の目的>
成果指標・KPI
小児用医薬品や難病・希少疾病用医薬品は、医療ニーズが高いにもかかわらず、
市場規模が小さいこと等によりドラッグ・ロスが生じやすい。
企業による開発を促すため、薬事規制当局においても積極的な支援が必要。
<現状>
ドラッグロスを生
じている医薬品:
86品目(R5)
<目標>
左記品目のうち必要
な医薬品について開
発着手(R8まで)
<施策の内容>
採算性の乏しい小児用医薬品・難病・希少疾病用医薬品の開
発の促進
参考資料
PMDAに小児・希少疾病用医薬品等薬事相談センターを
令和6年度に設置し、以下の取組を進める。
企業が成人を対象とした医薬品の開発を行う場合、併
せて小児用医薬品の開発計画を策定し、PMDAの確認を
受ける仕組みを導入・運用。
すでに決定した希少疾病用医薬品の指定の早期化につ
いて、その確実な運用。
小児・希少疾病用医薬品等薬事相談センター
①希少疾病用医薬品
指定・指定見直し
の相談・審査
②小児用医薬品
開発計画の確認・
進捗管理
③未承認薬検討会議
評価の加速 (調査、
評価書作成等)
PMDA相談手数料を補助
対象:上記①・②に関して企業が支払う相談手数料。未承認薬等検討会
議での開発公募品や医師主導治験による開発品。
「医療上の必要性の高い未承認薬・適応外薬検討会議」
における評価、開発要請等の加速化。
33