よむ、つかう、まなぶ。
薬-1 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43714.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第227回 9/25)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
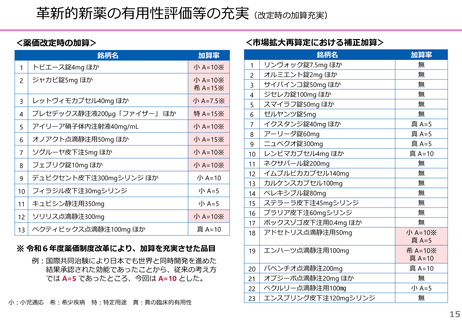
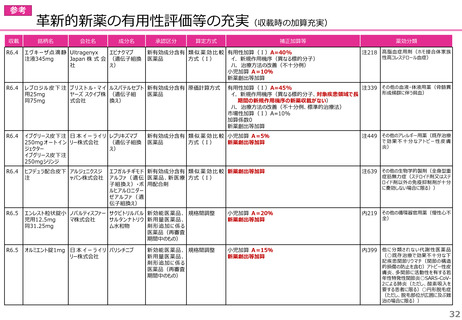
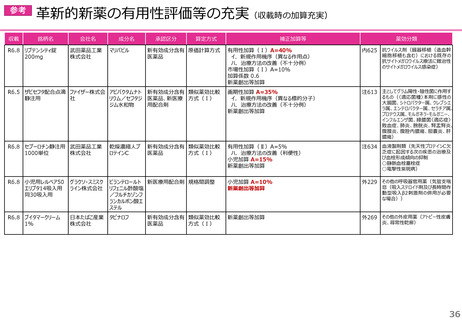
迅速導入加算の適用品目
※ 迅速導入加算以外の加算については省略
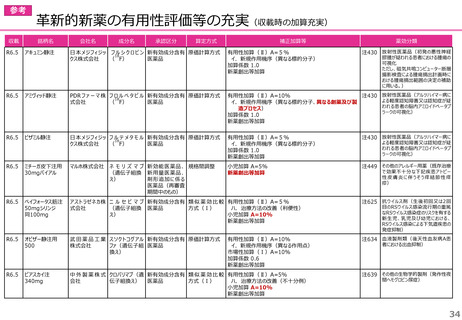
○ボイデヤ錠50mg
成分名:ダニコパン
効能・効果:発作性夜間ヘモグロビン尿症
迅速導入加算A=10%
理由:本剤は国際共同治験により開発され、優先審査の対象であり、かつ本邦における承認申請は欧米に
おいて最も早い承認申請から6か月以内及び承認は欧米より早いことから、加算の要件を満たす。
国際共同治験における日本人症例数が比較的多いことを踏まえ、加算率は10%が妥当である。
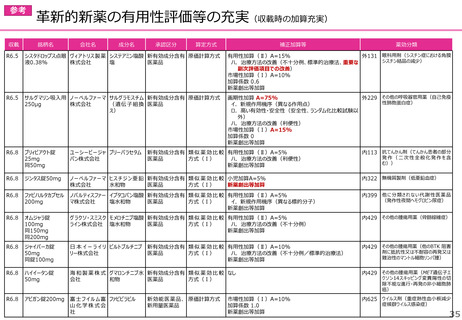
○アジンマ静注用1500
成分名:アパダムターゼ アルファ(遺伝子組換え)・シナキサダムターゼ アルファ(遺伝子組換え)混合物
効能・効果:先天性血栓性血小板減少性紫斑病
迅速導入加算A=5%
理由:本剤は国際共同治験により開発され、優先審査の対象であり、かつ本邦における承認申請及び承認
は欧米において最も早い承認申請及び承認から6か月以内であることから、加算の要件を満たす。
11
※ 迅速導入加算以外の加算については省略
○ボイデヤ錠50mg
成分名:ダニコパン
効能・効果:発作性夜間ヘモグロビン尿症
迅速導入加算A=10%
理由:本剤は国際共同治験により開発され、優先審査の対象であり、かつ本邦における承認申請は欧米に
おいて最も早い承認申請から6か月以内及び承認は欧米より早いことから、加算の要件を満たす。
国際共同治験における日本人症例数が比較的多いことを踏まえ、加算率は10%が妥当である。
○アジンマ静注用1500
成分名:アパダムターゼ アルファ(遺伝子組換え)・シナキサダムターゼ アルファ(遺伝子組換え)混合物
効能・効果:先天性血栓性血小板減少性紫斑病
迅速導入加算A=5%
理由:本剤は国際共同治験により開発され、優先審査の対象であり、かつ本邦における承認申請及び承認
は欧米において最も早い承認申請及び承認から6か月以内であることから、加算の要件を満たす。
11