よむ、つかう、まなぶ。
資料2 大学附属病院本院の現状等及び大学附属病院本院の特定機能病院としての取扱い上の論点等 (61 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43385.html |
| 出典情報 | 特定機能病院及び地域医療支援病院のあり方に関する検討会(第22回 11/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
臨床研究実施の流れ
研究責任医師が、実施計画・研究計画書等を認定臨床研究審査委員会に提出
認定臨床研究審査委員会が実施計画・研究計画書等を審査
厚生労働大臣に実施計画を提出(認定臨床研究審査委員会の意見書を添付)
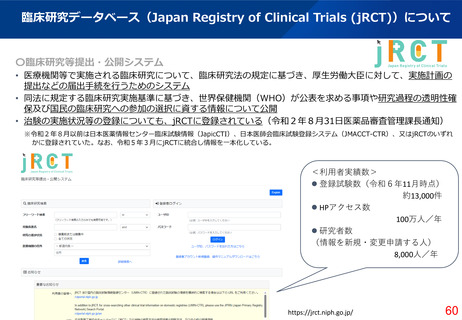
jRCT(Japan Registry of Clinical Trial)への登録・公開により行う
※
治験については、治験計画届書を届け出た場合、jRCTへ登録
研究責任医師が特定臨床研究を実施(国民へ公開)
⇒以下の事項について遵守することを義務付け
◎適切なインフォームド・コンセントの取得
◎臨床研究実施基準
・臨床研究の実施体制・構造設備に関する事項
・モニタリング・監査の実施に関する事項
・健康被害の補償・医療の提供に関する事項
・製薬企業等との利益相反管理に関する事項 等
◎記録の作成・保存
◎研究対象者の秘密の保持
<上記の手続に違反した場合の対応>
立
入
検
査
・
報
告
徴
収
改善命令
(保健衛生上の危害の発生又は拡大防止の
ために必要と認めるとき)
研究の全部又は
一部の停止命令
緊急命令
(研究の停止等)
罰
則
(検査の忌避・虚偽報告の場合)
61
研究責任医師が、実施計画・研究計画書等を認定臨床研究審査委員会に提出
認定臨床研究審査委員会が実施計画・研究計画書等を審査
厚生労働大臣に実施計画を提出(認定臨床研究審査委員会の意見書を添付)
jRCT(Japan Registry of Clinical Trial)への登録・公開により行う
※
治験については、治験計画届書を届け出た場合、jRCTへ登録
研究責任医師が特定臨床研究を実施(国民へ公開)
⇒以下の事項について遵守することを義務付け
◎適切なインフォームド・コンセントの取得
◎臨床研究実施基準
・臨床研究の実施体制・構造設備に関する事項
・モニタリング・監査の実施に関する事項
・健康被害の補償・医療の提供に関する事項
・製薬企業等との利益相反管理に関する事項 等
◎記録の作成・保存
◎研究対象者の秘密の保持
<上記の手続に違反した場合の対応>
立
入
検
査
・
報
告
徴
収
改善命令
(保健衛生上の危害の発生又は拡大防止の
ために必要と認めるとき)
研究の全部又は
一部の停止命令
緊急命令
(研究の停止等)
罰
則
(検査の忌避・虚偽報告の場合)
61