よむ、つかう、まなぶ。
資料5 ポリカルボフィルカルシウム (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198111_00021.html |
| 出典情報 | 医療用から要指導・一般用への転用に関する評価検討会議(第23回 12/26)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
審査報告
令和3年$月 13 日
1、申請品目
[販 売 名] 画是是証較 (申請時)
[一 般 名] ポリカルボフィルカルシツウ ム
[申 請 者] 小林製薬株式会社
[申請年月日] 令和元年 12 月 26 日
[成分・分基] 】 日量3錠中 ポリカルボフィルカルシウム 1300mg
[申請時の効能・効果] 過敏性腸症候群の次の諸症状の緩和:腹痛又は腹部不快感を伴い、
繰り返し又は交互にあらわれる下痢及び便秘 (以前に医師の診
断・治療を受けた人に限る)
[申請時の用法・用量] 成人 (15才以上) 1 回 1ー2 錠を、1 日 3 回、食後に水とともに
服用する。 ただし、 初回は最小基を用い、 便通の具合や状態をみ
ながら増基又は減量すること。
2. 提出された資料の概略及び審査の概格
本申請において、申請者が提出 した資料及び医薬品医療機器総合機構 (以下、『機構」と
いう。) における審査の概略は、以下のとおりである。なお、本剤については専門協議を実
施 し、 当該専門委員は、 本申請品目についての専門委員からの申し出等に基づき、「医薬品
医療機器総合機構における専円協議等の実施に関する達」 (平成 20 年 12 月 23 日付け 20 達
第 8 号) の規定により、指名 した。
イ. 起原又は発見の経緯及び外国における使用状況等に関する夏料
「ギュラック」 (以下、 「本剤」 という。) は、ポリカルボフィルカルシジウム (以下、 「本薬」
という。) を含有する医療用医薬品「ポリフル錠 S$00mg」 を要指導医薬品又は一般用医薬品
(以下、「要指導・一般用医薬品」という。) に転用するものである。本薬は要指導・一般用
医薬品として初めての成分であるため、 要指導 (一般用) 新有効成分含有医薬品として申請
された。
本薬は、北陸製薬株式会社 (現マイラン EPD 合同会社) で開発されたポリアクリル酸の
カルシウム塩である。 カルシウム脱離後、中性条件下で多量の水を吸収して膨潤・ゲル化す
ることで生体に吸収されずに消化管内容物の性状を正常化し、過敏性腸症候群 (以下、 HBS」
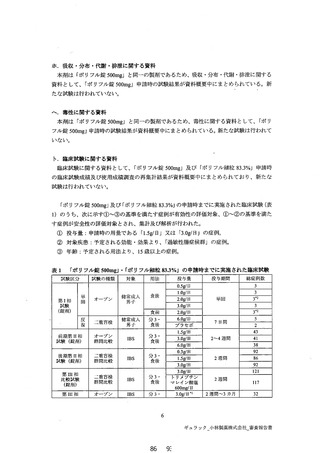
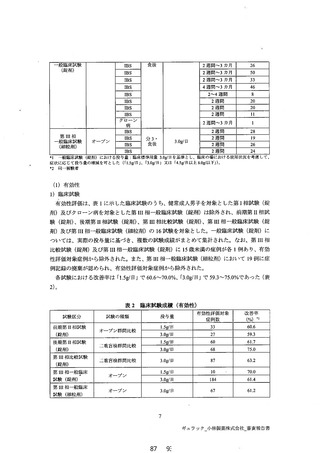
という。) の下弄及び便秘の両方に効果をボす。 本邦においては、!「ポリフル錠 300mg」 及び
剤形違い品目「ポリフル細粒 83.39%%」として、2000 年 7 月 3 日に過敏性腸症候群における
便通暴常 (下痢、 便秘) 及び消化器症状を適応症と して承認され、 再審査期間 6 年が指定 さ
れた。2009 年 3 月 30 日には、再審査結果が通知され、薬事法第 14 条第 2 項各号のいずれ
|
空テラック 小林製薬株式会社 審査報告書
63 けび
令和3年$月 13 日
1、申請品目
[販 売 名] 画是是証較 (申請時)
[一 般 名] ポリカルボフィルカルシツウ ム
[申 請 者] 小林製薬株式会社
[申請年月日] 令和元年 12 月 26 日
[成分・分基] 】 日量3錠中 ポリカルボフィルカルシウム 1300mg
[申請時の効能・効果] 過敏性腸症候群の次の諸症状の緩和:腹痛又は腹部不快感を伴い、
繰り返し又は交互にあらわれる下痢及び便秘 (以前に医師の診
断・治療を受けた人に限る)
[申請時の用法・用量] 成人 (15才以上) 1 回 1ー2 錠を、1 日 3 回、食後に水とともに
服用する。 ただし、 初回は最小基を用い、 便通の具合や状態をみ
ながら増基又は減量すること。
2. 提出された資料の概略及び審査の概格
本申請において、申請者が提出 した資料及び医薬品医療機器総合機構 (以下、『機構」と
いう。) における審査の概略は、以下のとおりである。なお、本剤については専門協議を実
施 し、 当該専門委員は、 本申請品目についての専門委員からの申し出等に基づき、「医薬品
医療機器総合機構における専円協議等の実施に関する達」 (平成 20 年 12 月 23 日付け 20 達
第 8 号) の規定により、指名 した。
イ. 起原又は発見の経緯及び外国における使用状況等に関する夏料
「ギュラック」 (以下、 「本剤」 という。) は、ポリカルボフィルカルシジウム (以下、 「本薬」
という。) を含有する医療用医薬品「ポリフル錠 S$00mg」 を要指導医薬品又は一般用医薬品
(以下、「要指導・一般用医薬品」という。) に転用するものである。本薬は要指導・一般用
医薬品として初めての成分であるため、 要指導 (一般用) 新有効成分含有医薬品として申請
された。
本薬は、北陸製薬株式会社 (現マイラン EPD 合同会社) で開発されたポリアクリル酸の
カルシウム塩である。 カルシウム脱離後、中性条件下で多量の水を吸収して膨潤・ゲル化す
ることで生体に吸収されずに消化管内容物の性状を正常化し、過敏性腸症候群 (以下、 HBS」
という。) の下弄及び便秘の両方に効果をボす。 本邦においては、!「ポリフル錠 300mg」 及び
剤形違い品目「ポリフル細粒 83.39%%」として、2000 年 7 月 3 日に過敏性腸症候群における
便通暴常 (下痢、 便秘) 及び消化器症状を適応症と して承認され、 再審査期間 6 年が指定 さ
れた。2009 年 3 月 30 日には、再審査結果が通知され、薬事法第 14 条第 2 項各号のいずれ
|
空テラック 小林製薬株式会社 審査報告書
63 けび