よむ、つかう、まなぶ。
資料1-1 厚生労働省 御提出資料 (14 ページ)
出典
| 公開元URL | https://www8.cao.go.jp/kisei-kaikaku/kisei/meeting/wg/2310_04medical/231211/medical03_agenda.html |
| 出典情報 | 規制改革推進会議 健康・医療・介護ワーキング・グループ(第3回 12/11)《内閣府》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
K P I ( ス イ ッ チ OTC の 総 審 査 期 間 ) の 具 体 的 内 容 と 管 理 状 況
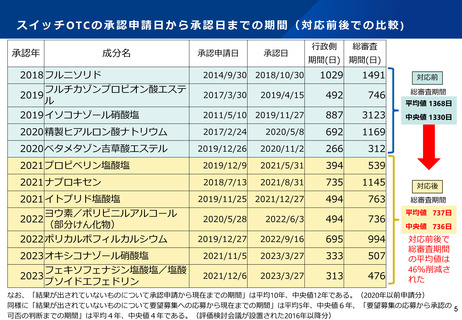
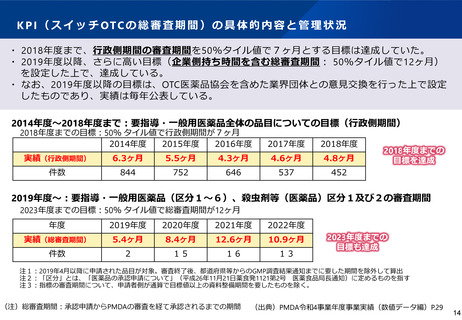
・ 2018年度まで、行政側期間の審査期間を50%タイル値で7ヶ月とする目標は達成していた。
・ 2019年度以降、さらに高い目標(企業側持ち時間を含む総審査期間: 50%タイル値で12ヶ月)
を設定した上で、達成している。
・ なお、2019年度以降の目標は、OTC医薬品協会を含めた業界団体との意見交換を行った上で設定
したものであり、実績は毎年公表している。
2014年度~2018年度まで:要指導・一般用医薬品全体の品目についての目標(行政側期間)
2018年度までの目標:50% タイル値で行政側期間が7ヶ月
2014年度
2015年度
2016年度
2017年度
2018年度
実績(行政側期間)
6.3ヶ月
5.5ヶ月
4.3ヶ月
4.6ヶ月
4.8ヶ月
件数
844
752
646
537
452
2018年度までの
目標を達成
2019年度~:要指導・一般用医薬品(区分1~6)、殺虫剤等(医薬品)区分1及び2の審査期間
2023年度までの目標:50% タイル値で総審査期間が12ヶ月
年度
2019年度
2020年度
2021年度
2022年度
実績(総審査期間)
5.4ヶ月
8.4ヶ月
12.6ヶ月
10.9ヶ月
件数
2
15
16
13
2023年度までの
目標も達成
注1:2019年4月以降に申請された品目が対象。審査終了後、都道府県等からのGMP調査結果通知までに要した期間を除外して算出
注2:「区分」とは、「医薬品の承認申請について」(平成26年11月21日薬食発1121第2号 医薬食品局長通知)に定めるものを指す
注3:指標の審査期間について、申請者側が通算で目標値以上の資料整備期間を要したものを除く。
(注)総審査期間:承認申請からPMDAの審査を経て承認されるまでの期間
(出典)PMDA令和4事業年度事業実績(数値データ編)P.29
14
・ 2018年度まで、行政側期間の審査期間を50%タイル値で7ヶ月とする目標は達成していた。
・ 2019年度以降、さらに高い目標(企業側持ち時間を含む総審査期間: 50%タイル値で12ヶ月)
を設定した上で、達成している。
・ なお、2019年度以降の目標は、OTC医薬品協会を含めた業界団体との意見交換を行った上で設定
したものであり、実績は毎年公表している。
2014年度~2018年度まで:要指導・一般用医薬品全体の品目についての目標(行政側期間)
2018年度までの目標:50% タイル値で行政側期間が7ヶ月
2014年度
2015年度
2016年度
2017年度
2018年度
実績(行政側期間)
6.3ヶ月
5.5ヶ月
4.3ヶ月
4.6ヶ月
4.8ヶ月
件数
844
752
646
537
452
2018年度までの
目標を達成
2019年度~:要指導・一般用医薬品(区分1~6)、殺虫剤等(医薬品)区分1及び2の審査期間
2023年度までの目標:50% タイル値で総審査期間が12ヶ月
年度
2019年度
2020年度
2021年度
2022年度
実績(総審査期間)
5.4ヶ月
8.4ヶ月
12.6ヶ月
10.9ヶ月
件数
2
15
16
13
2023年度までの
目標も達成
注1:2019年4月以降に申請された品目が対象。審査終了後、都道府県等からのGMP調査結果通知までに要した期間を除外して算出
注2:「区分」とは、「医薬品の承認申請について」(平成26年11月21日薬食発1121第2号 医薬食品局長通知)に定めるものを指す
注3:指標の審査期間について、申請者側が通算で目標値以上の資料整備期間を要したものを除く。
(注)総審査期間:承認申請からPMDAの審査を経て承認されるまでの期間
(出典)PMDA令和4事業年度事業実績(数値データ編)P.29
14