よむ、つかう、まなぶ。
資料4:臨床研究・治験推進に係る今後の方向性について (23 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43236.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第36回 9/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
臨床研究総合促進事業
臨床研究・治験従事者等研修プログラム
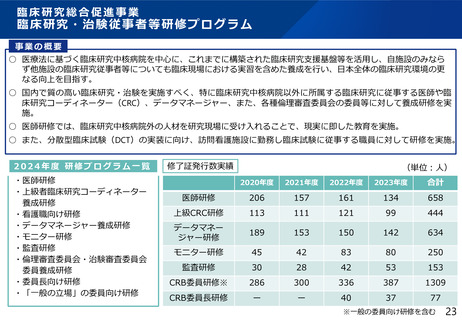
事業の概要
○ 医療法に基づく臨床研究中核病院を中心に、これまでに構築された臨床研究支援基盤等を活用し、自施設のみなら
ず他施設の臨床研究従事者等についても臨床現場における実習を含めた養成を行い、日本全体の臨床研究環境の更
なる向上を目指す。
○ 国内で質の高い臨床研究・治験を実施すべく、特に臨床研究中核病院以外に所属する臨床研究に従事する医師や臨
床研究コーディネーター(CRC)、データマネージャー、また、各種倫理審査委員会の委員等に対して養成研修を実
施。
○ 医師研修では、臨床研究中核病院外の人材を研究現場に受け入れることで、現実に即した教育を実施。
○ また、分散型臨床試験(DCT)の実装に向け、訪問看護施設に勤務し臨床試験に従事する職員に対して研修を実施。
2024年度 研修プログラム一覧
・医師研修
・上級者臨床研究コーディネーター
養成研修
・看護職向け研修
・データマネージャー養成研修
・モニター研修
・監査研修
・倫理審査委員会・治験審査委員会
委員養成研修
・委員長向け研修
・「一般の立場」の委員向け研修
修了証発行数実績
(単位:人)
2020年度
2021年度
2022年度
2023年度
合計
医師研修
206
157
161
134
658
上級CRC研修
113
111
121
99
444
データマネー
ジャー研修
189
153
150
142
634
モニター研修
45
42
83
80
250
監査研修
30
28
42
53
153
CRB委員研修※
286
300
336
387
1309
CRB委員長研修
ー
ー
40
37
77
※一般の委員向け研修を含む
23
臨床研究・治験従事者等研修プログラム
事業の概要
○ 医療法に基づく臨床研究中核病院を中心に、これまでに構築された臨床研究支援基盤等を活用し、自施設のみなら
ず他施設の臨床研究従事者等についても臨床現場における実習を含めた養成を行い、日本全体の臨床研究環境の更
なる向上を目指す。
○ 国内で質の高い臨床研究・治験を実施すべく、特に臨床研究中核病院以外に所属する臨床研究に従事する医師や臨
床研究コーディネーター(CRC)、データマネージャー、また、各種倫理審査委員会の委員等に対して養成研修を実
施。
○ 医師研修では、臨床研究中核病院外の人材を研究現場に受け入れることで、現実に即した教育を実施。
○ また、分散型臨床試験(DCT)の実装に向け、訪問看護施設に勤務し臨床試験に従事する職員に対して研修を実施。
2024年度 研修プログラム一覧
・医師研修
・上級者臨床研究コーディネーター
養成研修
・看護職向け研修
・データマネージャー養成研修
・モニター研修
・監査研修
・倫理審査委員会・治験審査委員会
委員養成研修
・委員長向け研修
・「一般の立場」の委員向け研修
修了証発行数実績
(単位:人)
2020年度
2021年度
2022年度
2023年度
合計
医師研修
206
157
161
134
658
上級CRC研修
113
111
121
99
444
データマネー
ジャー研修
189
153
150
142
634
モニター研修
45
42
83
80
250
監査研修
30
28
42
53
153
CRB委員研修※
286
300
336
387
1309
CRB委員長研修
ー
ー
40
37
77
※一般の委員向け研修を含む
23