よむ、つかう、まなぶ。
資料4:臨床研究・治験推進に係る今後の方向性について (32 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43236.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第36回 9/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
臨床研究データベースシステム
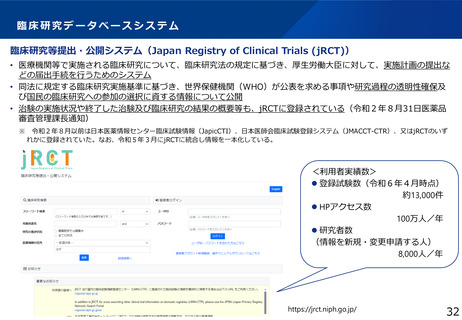
臨床研究等提出・公開システム(Japan Registry of Clinical Trials (jRCT))
• 医療機関等で実施される臨床研究について、臨床研究法の規定に基づき、厚生労働大臣に対して、実施計画の提出な
どの届出手続を行うためのシステム
• 同法に規定する臨床研究実施基準に基づき、世界保健機関(WHO)が公表を求める事項や研究過程の透明性確保及
び国民の臨床研究への参加の選択に資する情報について公開
• 治験の実施状況や終了した治験及び臨床研究の結果の概要等も、jRCTに登録されている(令和2年8月31日医薬品
審査管理課長通知)
※ 令和2年8月以前は日本医薬情報センター臨床試験情報(JapicCTI)、日本医師会臨床試験登録システム(JMACCT-CTR)、又はjRCTのいず
れかに登録されていた。なお、令和5年3月にjRCTに統合し情報を一本化している。
<利用者実績数>
⚫ 登録試験数(令和6年4月時点)
約13,000件
⚫ HPアクセス数
100万人/年
⚫ 研究者数
(情報を新規・変更申請する人)
8,000人/年
https://jrct.niph.go.jp/
32
臨床研究等提出・公開システム(Japan Registry of Clinical Trials (jRCT))
• 医療機関等で実施される臨床研究について、臨床研究法の規定に基づき、厚生労働大臣に対して、実施計画の提出な
どの届出手続を行うためのシステム
• 同法に規定する臨床研究実施基準に基づき、世界保健機関(WHO)が公表を求める事項や研究過程の透明性確保及
び国民の臨床研究への参加の選択に資する情報について公開
• 治験の実施状況や終了した治験及び臨床研究の結果の概要等も、jRCTに登録されている(令和2年8月31日医薬品
審査管理課長通知)
※ 令和2年8月以前は日本医薬情報センター臨床試験情報(JapicCTI)、日本医師会臨床試験登録システム(JMACCT-CTR)、又はjRCTのいず
れかに登録されていた。なお、令和5年3月にjRCTに統合し情報を一本化している。
<利用者実績数>
⚫ 登録試験数(令和6年4月時点)
約13,000件
⚫ HPアクセス数
100万人/年
⚫ 研究者数
(情報を新規・変更申請する人)
8,000人/年
https://jrct.niph.go.jp/
32