よむ、つかう、まなぶ。
資料4:臨床研究・治験推進に係る今後の方向性について (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43236.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第36回 9/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
「臨床研究・治験の推進に関する今後の方向性について
これまでの取組
2019年版とりまとめ」
Ⅳ.小児疾病・難病等の研究開発が進みにくい領域の取組
⚫ 小児疾病や難病等領域における取組の推進の観点から、
・AMEDを通じた臨床研究・医師主導治験の支援について、小児疾病領域においては別途公募枠
を設けた支援、希少疾病領域においては企業治験の支援を実施
・小児領域における医薬品開発を促進するため、開発支援リストの作成・更新や、企業への小児
用医薬品開発の要望、企業に対する治験実施のサポートを実施
・難病等のレジストリ保有者と開発企業とのマッチングを実施、企業の要望に応じたアカデミア
の疾患登録システムの改修を支援し、レジストリ利活用を促進
Ⅴ.国民・患者の理解や参画促進
⚫ 国民・患者への普及啓発の観点から、
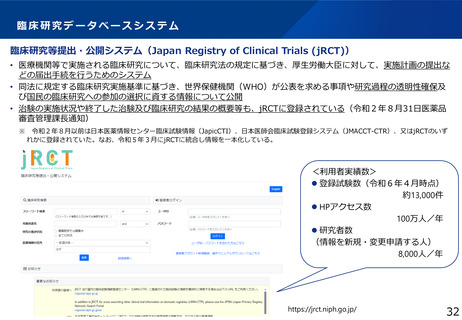
・臨床研究・治験情報へのアクセス向上に向けて、国内に複数存在していたデータベースについ
て順次jRCTへの統合を進め、検索機能の改善を実施
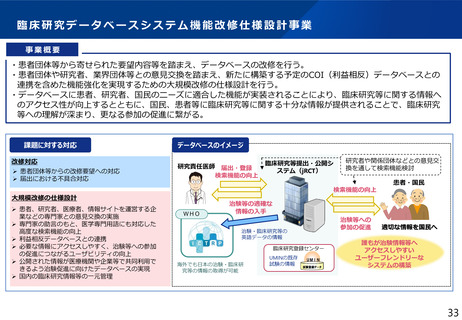
・患者団体や研究者、業界団体等との意見交換を踏まえ、国内の臨床研究データベースの在り方
を見直すべく、ユーザーフレンドリーなデータベースの実現に向けた大規模改修の検討を実施
・「臨床研究情報ポータルサイト」において、医療従事者だけでなく国民・患者向けの臨床研
究・治験について学ぶ本や教材を公表
6
これまでの取組
2019年版とりまとめ」
Ⅳ.小児疾病・難病等の研究開発が進みにくい領域の取組
⚫ 小児疾病や難病等領域における取組の推進の観点から、
・AMEDを通じた臨床研究・医師主導治験の支援について、小児疾病領域においては別途公募枠
を設けた支援、希少疾病領域においては企業治験の支援を実施
・小児領域における医薬品開発を促進するため、開発支援リストの作成・更新や、企業への小児
用医薬品開発の要望、企業に対する治験実施のサポートを実施
・難病等のレジストリ保有者と開発企業とのマッチングを実施、企業の要望に応じたアカデミア
の疾患登録システムの改修を支援し、レジストリ利活用を促進
Ⅴ.国民・患者の理解や参画促進
⚫ 国民・患者への普及啓発の観点から、
・臨床研究・治験情報へのアクセス向上に向けて、国内に複数存在していたデータベースについ
て順次jRCTへの統合を進め、検索機能の改善を実施
・患者団体や研究者、業界団体等との意見交換を踏まえ、国内の臨床研究データベースの在り方
を見直すべく、ユーザーフレンドリーなデータベースの実現に向けた大規模改修の検討を実施
・「臨床研究情報ポータルサイト」において、医療従事者だけでなく国民・患者向けの臨床研
究・治験について学ぶ本や教材を公表
6