資料2-2 医療機器基本計画に関する各省における取り組みの状況について (15 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_54795.html |
| 出典情報 | 国民が受ける医療の質の向上のための医療機器の研究開発及び普及の促進に関する検討会(第5回 3/17)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
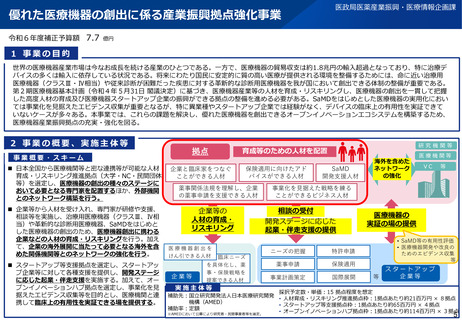
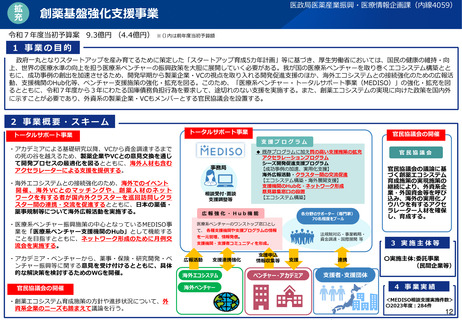
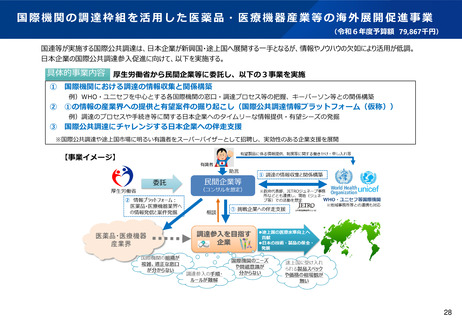
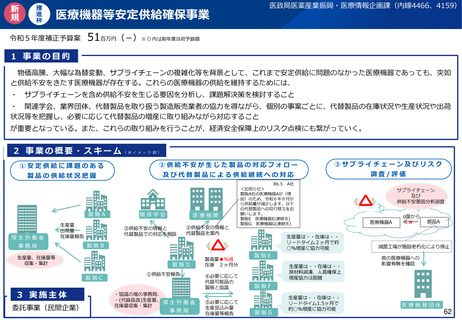
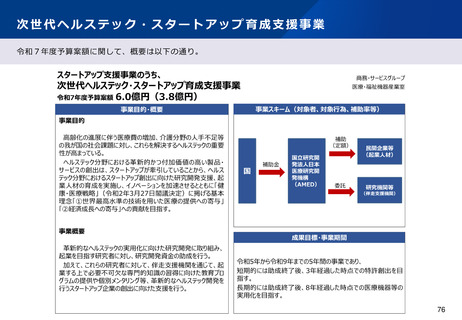
1 事業の目的
○ 小児・希少疾病に用いられる医療機器は、医療上の必要性は高いものの、国内外での対象患者数が少なく、市販後
の採算性の問題もあり、臨床試験の実施による製品開発が難しい。また、例えば小児患者においては、埋植型の医
療機器の場合、体格等の違いから成人用として承認取得した製品では代用ができず、小児患者にとって必要な医療
が提供できない状況がある。
○ 近年、医療機器の薬事申請においては、臨床試験データの代替又は補完となる根拠データとして、リアルワールド
エビデンスや非臨床データの利活用が着目されているが、実際に、小児疾患や希少疾病用医療機器の薬事申請にお
いてこれらのデータを利活用した経験は限定的である。
○ 小児疾患や希少疾病用医療機器の更なる早期承認に向けて、市販前後を通じ、臨床試験の代替又は補完となる根拠
データとして、国内レジストリ等により収集したリアルワールドエビデンスやin silico等による非臨床試験成績を
効率的に利活用するための具体的方法について提案する。また、将来的にガイドライン化することにより、小児疾
患や希少疾病用医療機器開発における臨床試験、リアルワールドエビデンス、非臨床試験等の有効的な活用手法を
明確化し、小児疾患や希少疾病用医療機器の早期実用化につなげる。
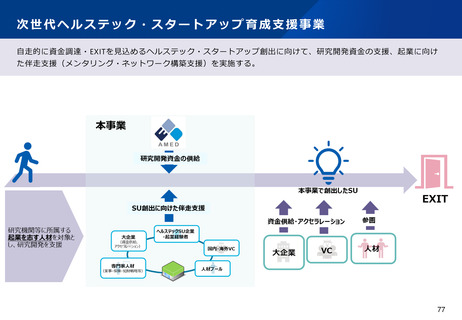
2 事業の概要・スキーム
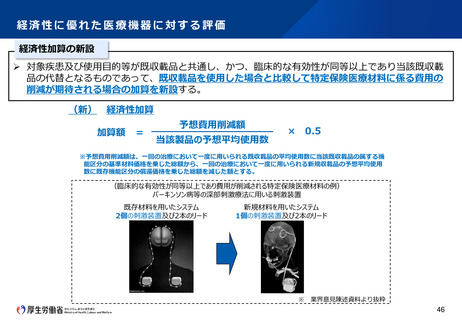
特定の小児疾患用医療機器開発において臨床試験データの代替又は補完として活用が期待される非臨床試験方法(令
和5年度研究)も参考に、様々な疾患領域における小児疾患や希少疾病用医療機器の更なる早期承認に向けて、市販
前後を通じて、臨床試験、リアルワールドエビデンス、非臨床試験等を効率的かつ有効的に利活用するための具体的
方法について提案する。
3 実施主体等
実施主体:国立医薬品食品衛生研究所
4 事業実績
ー
15