資料2-2 医療機器基本計画に関する各省における取り組みの状況について (34 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_54795.html |
| 出典情報 | 国民が受ける医療の質の向上のための医療機器の研究開発及び普及の促進に関する検討会(第5回 3/17)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
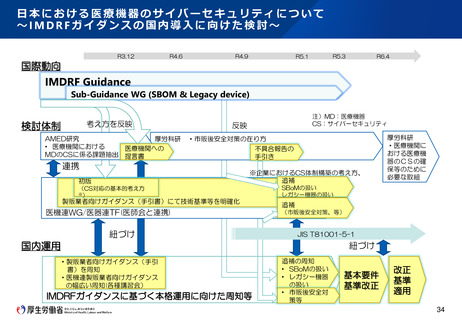
~IMDRFガイダンスの国内導入に向けた検討~
R3.12
R4.6
R4.9
R5.3
R5.1
R6.4
国際動向
IMDRF Guidance
Sub-Guidance WG (SBOM & Legacy device)
考え方を反映
検討体制
AMED研究
厚労科研
• 医療機関における
医療機関への
MDのCSに係る課題抽出 提言書
注)MD:医療機器
CS:サイバーセキュリティ
反映
・市販後安全対策の在り方
連携
不具合報告の
手引き
※企業におけるCS体制構築の考え方、
追補
等
初版
(CS対応の基本的考え方
※)
製販業者向けガイダンス(手引書)にて技術基準等を明確化
医機連WG/医器連TF(医師会と連携)
紐づけ
SBoMの扱い
レガシー機器の扱い
追補
(市販後安全対策、等)
JIS T81001-5-1
国内運用
・製販業者向けガイダンス(手引
書)を周知
・医機連製販業者向けガイダンス
の幅広い周知(各種講習会)
IMDRFガイダンスに基づく本格運用に向けた周知等
厚労科研
・医療機関に
おける医療機
器のCSの確
保等のために
必要な取組
紐づけ
追補の周知
• SBoMの扱い
• レガシー機器
の扱い
• 市販後安全対
策等
基本要件
基準改正
改正
基準
適用
34