よむ、つかう、まなぶ。
総-2-1○医薬品の新規薬価収載について (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00177.html |
| 出典情報 | 中央社会保険医療協議会 総会(第540回 3/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
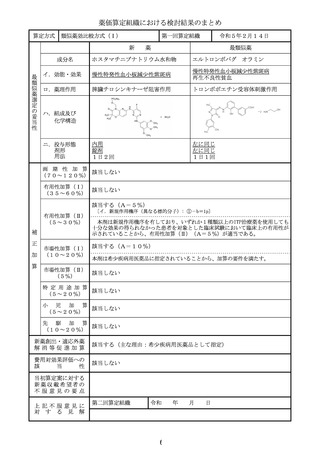
薬価算定組織における検討結果のまとめ
算定方式
原価計算方式
第一回算定組織
新
原
価
計
算
方
式
を
採
用
す
る
妥
当
性
令和5年2月14日
薬
類似薬がない根拠
ハ.組成及び
化学構造
薬価算定においては「承認を
受けた日の前日から起算して
急性白血病(慢性白血病の急性転化例を含
過去10年間に薬価収載され
たもの」を最類似薬とすること
む)、悪性リンパ腫
ただし、L-アスパラギナーゼ製剤に過敏症 が基本であるが、一定程度の類
似性のある大腸菌由来L-ア
を示した場合に限る。
スパラギナーゼ製剤であるロ
イナーゼは昭和46年の薬価
L-アスパラギン加水分解作用
収載品目であることから、本剤
327個のアミノ酸残基からなるサブユニッ の算定上の比較薬として用い
るには適当でないと判断した。
ト4分子から構成されるタンパク質である。
ニ.投与形態
剤形
用法
注射
注射剤
1日1回/週に3回
成分名
イ.効能・効果
ロ.薬理作用
クリサンタスパーゼ
画 期 性 加 算
該当しない
(70~120%)
有用性加算(Ⅰ)
該当しない
(35~60%)
該当する(A=5%)/該当しない
〔ハ.治療方法の改善(不十分例): ③-a=1p〕
補
正
加
算
有用性加算(Ⅱ)
既存の治療方法であるL-ASP製剤に対して過敏症を示し、同剤が使用できなく
(5~30%)
なった患者に対しての有効性が示されていること等から、有用性加算(Ⅱ)
(A=5%)
を適用することが適当と判断した。
市場性加算(Ⅰ)
該当しない
(10~20%)
市場性加算(Ⅱ)
該当しない
(5%)
特 定 用 途 加 算
該当しない
(5~20%)
該当する(A=5%)
小
児 加 算
本剤の効能・効果および用法・用量は小児と成人の区別がされておらず、小児と成人
(5~20%)
は明らかにされていないが、本剤は小児にも使用可能であること等から、加算の要件
に該当する。小児の試験組み入れ数等を踏まえ、加算率は5%が妥当である。
先 駆 加 算
該当しない
(10~20%)
新薬創出・適応外薬
解消等促進加算
該当する(主な理由:加算適用)
費用対効果評価への
該
当
性
該当しない
当初算定案に対する
新薬収載希望者の
不服意見の要点
上記不服意見に
対 す る 見 解
第二回算定組織
令和
16
年
月
日
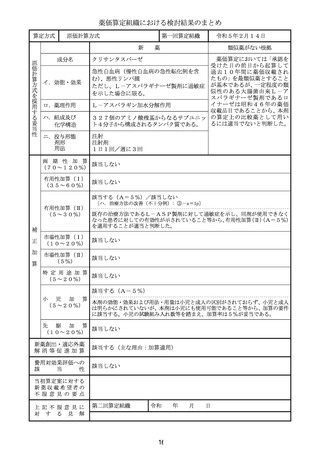
算定方式
原価計算方式
第一回算定組織
新
原
価
計
算
方
式
を
採
用
す
る
妥
当
性
令和5年2月14日
薬
類似薬がない根拠
ハ.組成及び
化学構造
薬価算定においては「承認を
受けた日の前日から起算して
急性白血病(慢性白血病の急性転化例を含
過去10年間に薬価収載され
たもの」を最類似薬とすること
む)、悪性リンパ腫
ただし、L-アスパラギナーゼ製剤に過敏症 が基本であるが、一定程度の類
似性のある大腸菌由来L-ア
を示した場合に限る。
スパラギナーゼ製剤であるロ
イナーゼは昭和46年の薬価
L-アスパラギン加水分解作用
収載品目であることから、本剤
327個のアミノ酸残基からなるサブユニッ の算定上の比較薬として用い
るには適当でないと判断した。
ト4分子から構成されるタンパク質である。
ニ.投与形態
剤形
用法
注射
注射剤
1日1回/週に3回
成分名
イ.効能・効果
ロ.薬理作用
クリサンタスパーゼ
画 期 性 加 算
該当しない
(70~120%)
有用性加算(Ⅰ)
該当しない
(35~60%)
該当する(A=5%)/該当しない
〔ハ.治療方法の改善(不十分例): ③-a=1p〕
補
正
加
算
有用性加算(Ⅱ)
既存の治療方法であるL-ASP製剤に対して過敏症を示し、同剤が使用できなく
(5~30%)
なった患者に対しての有効性が示されていること等から、有用性加算(Ⅱ)
(A=5%)
を適用することが適当と判断した。
市場性加算(Ⅰ)
該当しない
(10~20%)
市場性加算(Ⅱ)
該当しない
(5%)
特 定 用 途 加 算
該当しない
(5~20%)
該当する(A=5%)
小
児 加 算
本剤の効能・効果および用法・用量は小児と成人の区別がされておらず、小児と成人
(5~20%)
は明らかにされていないが、本剤は小児にも使用可能であること等から、加算の要件
に該当する。小児の試験組み入れ数等を踏まえ、加算率は5%が妥当である。
先 駆 加 算
該当しない
(10~20%)
新薬創出・適応外薬
解消等促進加算
該当する(主な理由:加算適用)
費用対効果評価への
該
当
性
該当しない
当初算定案に対する
新薬収載希望者の
不服意見の要点
上記不服意見に
対 す る 見 解
第二回算定組織
令和
16
年
月
日