よむ、つかう、まなぶ。
○令和6年度薬価改定について 薬-1 (28 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212451_00082.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第218回 11/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
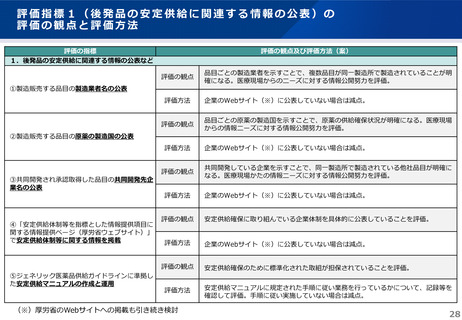
評価指標1(後発品の安定供給に関連する情報の公表)の
評価の観点と評価方法
評価の指標
1.後発品の安定供給に関連する情報の公表など
評価の観点及び評価方法(案)
評価の観点
品目ごとの製造業者を示すことで、複数品目が同一製造所で製造されていることが明
確になる。医療現場からのニーズに対する情報公開努力を評価。
評価方法
企業のWebサイト(※)に公表していない場合は減点。
評価の観点
品目ごとの原薬の製造国を示すことで、原薬の供給確保状況が明確になる。医療現場
からの情報ニーズに対する情報公開努力を評価。
評価方法
企業のWebサイト(※)に公表していない場合は減点。
評価の観点
共同開発している企業を示すことで、同一製造所で製造されている他社品目が明確に
なる。医療現場かたの情報ニーズに対する情報公開努力を評価。
評価方法
企業のWebサイト(※)に公表していない場合は減点。
評価の観点
安定供給確保に取り組んでいる企業体制を具体的に公表していることを評価。
評価方法
企業のWebサイト(※)に公表していない場合は減点。
評価の観点
安定供給確保のために標準化された取組が担保されていることを評価。
評価方法
安定供給マニュアルに規定された手順に従い業務を行っているかについて、記録等を
確認して評価。手順に従い実施していない場合は減点。
①製造販売する品目の製造業者名の公表
②製造販売する品目の原薬の製造国の公表
③共同開発され承認取得した品目の共同開発先企
業名の公表
④「安定供給体制等を指標とした情報提供項目に
関する情報提供ページ(厚労省ウェブサイト)」
で安定供給体制等に関する情報を掲載
⑤ジェネリック医薬品供給ガイドラインに準拠し
た安定供給マニュアルの作成と運用
(※)厚労省のWebサイトへの掲載も引き続き検討
28
評価の観点と評価方法
評価の指標
1.後発品の安定供給に関連する情報の公表など
評価の観点及び評価方法(案)
評価の観点
品目ごとの製造業者を示すことで、複数品目が同一製造所で製造されていることが明
確になる。医療現場からのニーズに対する情報公開努力を評価。
評価方法
企業のWebサイト(※)に公表していない場合は減点。
評価の観点
品目ごとの原薬の製造国を示すことで、原薬の供給確保状況が明確になる。医療現場
からの情報ニーズに対する情報公開努力を評価。
評価方法
企業のWebサイト(※)に公表していない場合は減点。
評価の観点
共同開発している企業を示すことで、同一製造所で製造されている他社品目が明確に
なる。医療現場かたの情報ニーズに対する情報公開努力を評価。
評価方法
企業のWebサイト(※)に公表していない場合は減点。
評価の観点
安定供給確保に取り組んでいる企業体制を具体的に公表していることを評価。
評価方法
企業のWebサイト(※)に公表していない場合は減点。
評価の観点
安定供給確保のために標準化された取組が担保されていることを評価。
評価方法
安定供給マニュアルに規定された手順に従い業務を行っているかについて、記録等を
確認して評価。手順に従い実施していない場合は減点。
①製造販売する品目の製造業者名の公表
②製造販売する品目の原薬の製造国の公表
③共同開発され承認取得した品目の共同開発先企
業名の公表
④「安定供給体制等を指標とした情報提供項目に
関する情報提供ページ(厚労省ウェブサイト)」
で安定供給体制等に関する情報を掲載
⑤ジェネリック医薬品供給ガイドラインに準拠し
た安定供給マニュアルの作成と運用
(※)厚労省のWebサイトへの掲載も引き続き検討
28