よむ、つかう、まなぶ。
参考資料4:総薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会報告書 (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43236.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第36回 9/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
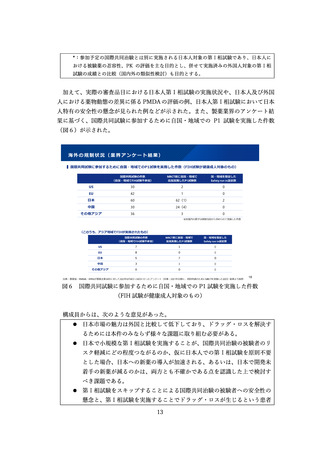
理科大学薬学部薬学科・鹿野真弓教授)から、小児がん及び小児希少難治性疾患に係
る医薬品開発の推進に資する調査研究の結果(海外制度の調査や国内関係者へのアン
ケート調査の結果)について報告された4。
特定用途医薬品指定制度
令和元年の薬機法改正に伴い新設(薬機法第77条の2第3項。令和2年9月施行)
特定用途医薬品の考え方
特定用途医薬品の運用
○ 制度の対象となる要件
•
当該用途に係る医薬品に対する需要が著しく充足されて
いないもの。
•
製造販売承認されれば、その用途に関し、特に優れた使
用価値を有するもの。
•
特定用途医薬品指定制度は、医療上の
ニーズが著しく充足されていない用途の
医薬品に注目した承認制度
•
「需要が著しく充足されていない用途」
を省令で指定し、その領域の医薬品につ
いて研究開発を促進
省令で以下の用途を指定
①小児用
②薬剤耐性菌(AMR)用
•
薬事・食品衛生審議会の意見を聴いて厚生
労働大臣が指定
- 医療上の必要性に基づき判断
•
優先審査の対象
•
4年以上6年未満の再審査期間の付与
•
その用途の対象者が5万人未満の医薬品の
開発については、研究開発費の助成と税制
優遇の対象
対象に想定される医薬品のイメージ
○含む
×含まない
• 患者数が多い医薬品の小児
用法・用量の追加
• 新薬開発における小児用
法・用量の検討
• 既存の医薬品の剤形の追加
で特に必要なもの
• 希少疾病用医薬品の対象と
なり得るもの(対象とする
必要がない)
図3 特定用途医薬品指定制度
4
https://www.mhlw.go.jp/content/11121000/001118957.pdf
8
る医薬品開発の推進に資する調査研究の結果(海外制度の調査や国内関係者へのアン
ケート調査の結果)について報告された4。
特定用途医薬品指定制度
令和元年の薬機法改正に伴い新設(薬機法第77条の2第3項。令和2年9月施行)
特定用途医薬品の考え方
特定用途医薬品の運用
○ 制度の対象となる要件
•
当該用途に係る医薬品に対する需要が著しく充足されて
いないもの。
•
製造販売承認されれば、その用途に関し、特に優れた使
用価値を有するもの。
•
特定用途医薬品指定制度は、医療上の
ニーズが著しく充足されていない用途の
医薬品に注目した承認制度
•
「需要が著しく充足されていない用途」
を省令で指定し、その領域の医薬品につ
いて研究開発を促進
省令で以下の用途を指定
①小児用
②薬剤耐性菌(AMR)用
•
薬事・食品衛生審議会の意見を聴いて厚生
労働大臣が指定
- 医療上の必要性に基づき判断
•
優先審査の対象
•
4年以上6年未満の再審査期間の付与
•
その用途の対象者が5万人未満の医薬品の
開発については、研究開発費の助成と税制
優遇の対象
対象に想定される医薬品のイメージ
○含む
×含まない
• 患者数が多い医薬品の小児
用法・用量の追加
• 新薬開発における小児用
法・用量の検討
• 既存の医薬品の剤形の追加
で特に必要なもの
• 希少疾病用医薬品の対象と
なり得るもの(対象とする
必要がない)
図3 特定用途医薬品指定制度
4
https://www.mhlw.go.jp/content/11121000/001118957.pdf
8