よむ、つかう、まなぶ。
資料2:臨床研究・治験推進に係る今後の方向性について (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44426.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第37回 10/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
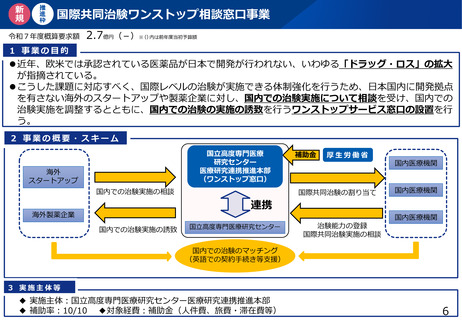
国際共同治験ワンストップ相談窓口事業
令和7年度概算要求額
2.7億円(-)※()内は前年度当初予算額
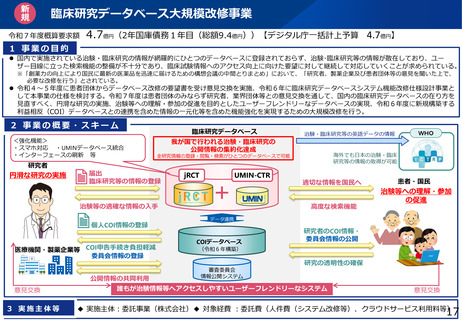
1 事業の目的
⚫ 近年、欧米では承認されている医薬品が日本で開発が行われない、いわゆる「ドラッグ・ロス」の拡大
が指摘されている。
⚫ こうした課題に対応すべく、国際レベルの治験が実施できる体制強化を行うため、日本国内に開発拠点
を有さない海外のスタートアップや製薬企業に対し、国内での治験実施について相談を受け、国内での
治験実施を調整するとともに、国内での治験の実施の誘致を行うワンストップサービス窓口の設置を行
う。
2 事業の概要・スキーム
国立高度専門医療
研究センター
医療研究連携推進本部
(ワンストップ窓口)
海外
スタートアップ
国内での治験実施の相談
補助金
厚生労働省
国際共同治験の割り当て
国内医療機関
国内医療機関
連携
海外製薬企業
国内での治験実施の誘致
国立高度専門医療研究センター
治験能力の登録
国際共同治験実施の相談
国内医療機関
国内での治験のマッチング
(英語での契約手続き等支援)
3 実施主体等
◆ 実施主体:国立高度専門医療研究センター医療研究連携推進本部
◆ 補助率:10/10 ◆対象経費:補助金(人件費、旅費・滞在費等)
6
令和7年度概算要求額
2.7億円(-)※()内は前年度当初予算額
1 事業の目的
⚫ 近年、欧米では承認されている医薬品が日本で開発が行われない、いわゆる「ドラッグ・ロス」の拡大
が指摘されている。
⚫ こうした課題に対応すべく、国際レベルの治験が実施できる体制強化を行うため、日本国内に開発拠点
を有さない海外のスタートアップや製薬企業に対し、国内での治験実施について相談を受け、国内での
治験実施を調整するとともに、国内での治験の実施の誘致を行うワンストップサービス窓口の設置を行
う。
2 事業の概要・スキーム
国立高度専門医療
研究センター
医療研究連携推進本部
(ワンストップ窓口)
海外
スタートアップ
国内での治験実施の相談
補助金
厚生労働省
国際共同治験の割り当て
国内医療機関
国内医療機関
連携
海外製薬企業
国内での治験実施の誘致
国立高度専門医療研究センター
治験能力の登録
国際共同治験実施の相談
国内医療機関
国内での治験のマッチング
(英語での契約手続き等支援)
3 実施主体等
◆ 実施主体:国立高度専門医療研究センター医療研究連携推進本部
◆ 補助率:10/10 ◆対象経費:補助金(人件費、旅費・滞在費等)
6