よむ、つかう、まなぶ。
資料2:臨床研究・治験推進に係る今後の方向性について (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44426.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第37回 10/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
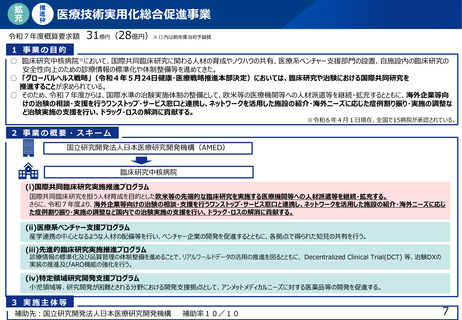
医療技術実用化総合促進事業
令和7年度概算要求額
31億円(28億円)※()内は前年度当初予算額
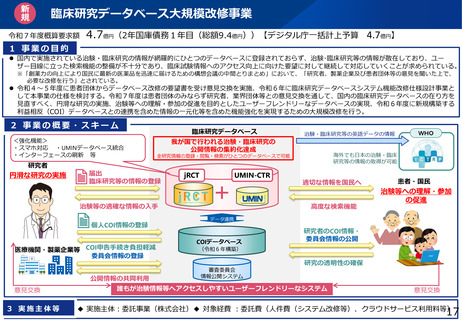
1 事業の目的
○ 臨床研究中核病院※において、国際共同臨床研究に関わる人材の育成やノウハウの共有、医療系ベンチャー支援部門の設置、自施設内の臨床研究の
安全性向上のための診療情報の標準化や体制整備等を進めてきた。
○ 「グローバルヘルス戦略」(令和4年5月24日健康・医療戦略推進本部決定)においては、臨床研究や治験における国際共同研究を
推進することが求められている。
○ そのため、令和7年度からは、国際水準の治験実施体制の整備として、欧米等の医療機関等への人材派遣等を継続・拡充するとともに、海外企業等向
けの治験の相談・支援を行うワンストップ・サービス窓口と連携し、ネットワークを活用した施設の紹介・海外ニーズに応じた症例割り振り・実施の調整な
ど治験実施の支援を行い、ドラッグ・ロスの解消に貢献する。
※令和6年4月1日現在、全国で15病院が承認されている。
2 事業の概要・スキーム
国立研究開発法人日本医療研究開発機構(AMED)
臨床研究中核病院
(i)国際共同臨床研究実施推進プログラム
国際共同臨床研究を担う人材育成を目的とした欧米等の先端的な臨床研究を実施する医療機関等への人材派遣等を継続・拡充する。
さらに、令和7年度より、海外企業等向けの治験の相談・支援を行うワンストップ・サービス窓口と連携し、ネットワークを活用した施設の紹介・海外ニーズに応じ
た症例割り振り・実施の調整など国内での治験実施の支援を行い、ドラッグ・ロスの解消に貢献する。
(ii)医療系ベンチャー支援プログラム
産学連携の中心となるような人材の配備等を行い、ベンチャー企業の開発を促進するとともに、各拠点で得られた知見の共有を行う。
(iii)先進的臨床研究実施推進プログラム
診療情報の標準化及び品質管理の体制整備を進めることで、リアルワールドデータの活用の推進を図るとともに、 Decentralized Clinical Trial(DCT) 等、治験DXの
実装の推進及びARO機能の強化を行う。
(iv)特定領域研究開発支援プログラム
小児領域等、研究開発が困難とされる分野における開発支援拠点として、アンメットメディカルニーズに対する医薬品等の開発を促進する。
3 実施主体等
補助先:国立研究開発法人日本医療研究開発機構
補助率10/10
7
令和7年度概算要求額
31億円(28億円)※()内は前年度当初予算額
1 事業の目的
○ 臨床研究中核病院※において、国際共同臨床研究に関わる人材の育成やノウハウの共有、医療系ベンチャー支援部門の設置、自施設内の臨床研究の
安全性向上のための診療情報の標準化や体制整備等を進めてきた。
○ 「グローバルヘルス戦略」(令和4年5月24日健康・医療戦略推進本部決定)においては、臨床研究や治験における国際共同研究を
推進することが求められている。
○ そのため、令和7年度からは、国際水準の治験実施体制の整備として、欧米等の医療機関等への人材派遣等を継続・拡充するとともに、海外企業等向
けの治験の相談・支援を行うワンストップ・サービス窓口と連携し、ネットワークを活用した施設の紹介・海外ニーズに応じた症例割り振り・実施の調整な
ど治験実施の支援を行い、ドラッグ・ロスの解消に貢献する。
※令和6年4月1日現在、全国で15病院が承認されている。
2 事業の概要・スキーム
国立研究開発法人日本医療研究開発機構(AMED)
臨床研究中核病院
(i)国際共同臨床研究実施推進プログラム
国際共同臨床研究を担う人材育成を目的とした欧米等の先端的な臨床研究を実施する医療機関等への人材派遣等を継続・拡充する。
さらに、令和7年度より、海外企業等向けの治験の相談・支援を行うワンストップ・サービス窓口と連携し、ネットワークを活用した施設の紹介・海外ニーズに応じ
た症例割り振り・実施の調整など国内での治験実施の支援を行い、ドラッグ・ロスの解消に貢献する。
(ii)医療系ベンチャー支援プログラム
産学連携の中心となるような人材の配備等を行い、ベンチャー企業の開発を促進するとともに、各拠点で得られた知見の共有を行う。
(iii)先進的臨床研究実施推進プログラム
診療情報の標準化及び品質管理の体制整備を進めることで、リアルワールドデータの活用の推進を図るとともに、 Decentralized Clinical Trial(DCT) 等、治験DXの
実装の推進及びARO機能の強化を行う。
(iv)特定領域研究開発支援プログラム
小児領域等、研究開発が困難とされる分野における開発支援拠点として、アンメットメディカルニーズに対する医薬品等の開発を促進する。
3 実施主体等
補助先:国立研究開発法人日本医療研究開発機構
補助率10/10
7