よむ、つかう、まなぶ。
資料1-2 MID-NET・NDB の行政利活用の調査実施状況について[894KB] (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別添資料3
MID-NET を用いた調査結果の概要
®
2025 年 3 月 5 日
Ⓡ
調査・研究 MID-NET を用いた GLP-1 受容体作動薬が処方された 2 型糖尿病患者における
の名称
肝機能障害の発現状況の評価
調 査 対 象 ◼ 以下の Glucagon-like peptide 1(以下、「GLP-1」)受容体作動薬
品目
デュラグルチド(遺伝子組換え)、リラグルチド(遺伝子組換え)、エキセナチド、
リキシセナチド、セマグルチド(遺伝子組換え)
◼
以下の GLP-1 受容体作動薬とインスリン製剤との配合剤
インスリン デグルデク(遺伝子組換え)・リラグルチド(遺伝子組換え)、イン
スリン グラルギン(遺伝子組換え)・リキシセナチド
調査背景
◼
本邦において、GLP-1 受容体作動薬及びそのインスリン製剤との配合剤は 2 型糖尿
病を効能・効果としている。
◼
このうちトルリシティ皮下注 0.75 mg アテオス(以下、「トルリシティ」)におけ
る肝機能障害関連の個別症例報告の集積状況、及び GLP-1 受容体作動薬の注意事項
等情報における肝機能障害関連の記載状況*1 に差異があること等を鑑みて、機構は、
医療情報データベースを活用した薬剤疫学調査を実施し、GLP-1 受容体作動薬処方
後の肝機能障害の発現状況を定量的に評価することとした。
*1 いずれの GLP-1 受容体作動薬も、使用上の注意において、「重大な副作用」の項に肝機能障害関連事象が
記載されているものはなかった。なお、使用上の注意の「その他の副作用」の項に肝機能障害関連事象が
記載されているのは以下の製剤であった。なお、2022 年 3 月 16 日時点の情報であり、2025 年 3 月 4 日時
点まで変更はなかった。
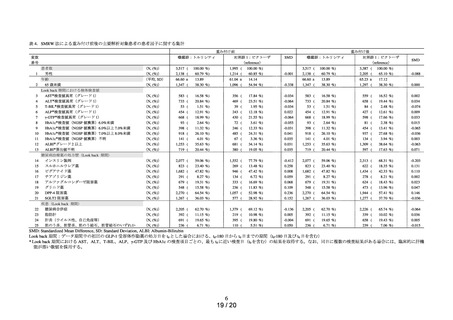
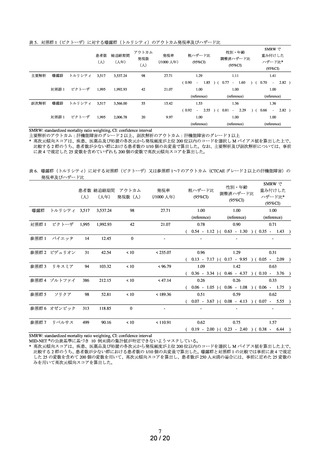
ビクトーザ皮下注 18 mg(リラグルチド(遺伝子組換え))(以下、「ビクトーザ」)は、肝胆道系
障害に、肝機能異常(0.2~1%)及び臨床検査(AST、ALT 増加)(0.2~1%)
バイエッタ皮下注 5μg ペン 300 及び同 10 μg ペン 300(エキセナチド)は、肝胆道系障害に肝機
能異常(1%未満)
ビデュリオン皮下注用 2 mg ペン及び同皮下注用 2 mg(エキセナチド)は、肝胆道系障害に肝機能
異常(1%未満)
ゾルトファイ配合注フレックスタッチ(インスリン デグルデク(遺伝子組換え)・リラグルチド
(遺伝子組換え))は、肝胆道系障害に肝機能異常(AST、ALT の上昇等)(頻度不明)
AST:アスパラギン酸アミノトランスフェラーゼ、ALT:アラニンアミノトランスフェラーゼ
調査目的
MID-NETⓇを用いて、GLP-1 受容体作動薬が処方された 2 型糖尿病患者において、トル
リシティ処方患者とその他の GLP-1 受容体作動薬処方患者の肝機能障害の発現状況を
比較する。
MID-NET 選定理由
:臨床検査値を指標とした評価を実施するために選択
の 選 定 理 データ期間 :2009 年 1 月 1 日~2022 年 3 月 31 日
由とデー
データ期間に利用可能であった MID-NET®協力医療機関(10 拠点 22 病
タ期間
院)のデータを利用
調 査 方 法 ◼ 調査デザイン:New User Cohort デザイン
の概略
◼ 調査対象集団:GLP-1 受容体作動薬が新規で処方された患者
®
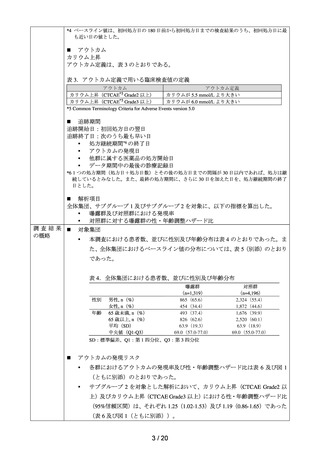
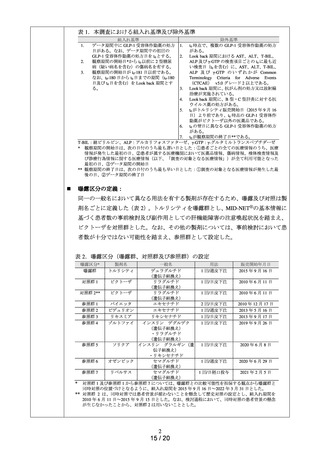
本調査は、GLP-1 受容体作動薬の効能・効果である 2 型糖尿病の患者を対象として、
表 1 の全ての組入れ基準を満たし、いずれの除外基準も満たさない患者を調査対象
集団に設定した。
1
14 / 20
MID-NET を用いた調査結果の概要
®
2025 年 3 月 5 日
Ⓡ
調査・研究 MID-NET を用いた GLP-1 受容体作動薬が処方された 2 型糖尿病患者における
の名称
肝機能障害の発現状況の評価
調 査 対 象 ◼ 以下の Glucagon-like peptide 1(以下、「GLP-1」)受容体作動薬
品目
デュラグルチド(遺伝子組換え)、リラグルチド(遺伝子組換え)、エキセナチド、
リキシセナチド、セマグルチド(遺伝子組換え)
◼
以下の GLP-1 受容体作動薬とインスリン製剤との配合剤
インスリン デグルデク(遺伝子組換え)・リラグルチド(遺伝子組換え)、イン
スリン グラルギン(遺伝子組換え)・リキシセナチド
調査背景
◼
本邦において、GLP-1 受容体作動薬及びそのインスリン製剤との配合剤は 2 型糖尿
病を効能・効果としている。
◼
このうちトルリシティ皮下注 0.75 mg アテオス(以下、「トルリシティ」)におけ
る肝機能障害関連の個別症例報告の集積状況、及び GLP-1 受容体作動薬の注意事項
等情報における肝機能障害関連の記載状況*1 に差異があること等を鑑みて、機構は、
医療情報データベースを活用した薬剤疫学調査を実施し、GLP-1 受容体作動薬処方
後の肝機能障害の発現状況を定量的に評価することとした。
*1 いずれの GLP-1 受容体作動薬も、使用上の注意において、「重大な副作用」の項に肝機能障害関連事象が
記載されているものはなかった。なお、使用上の注意の「その他の副作用」の項に肝機能障害関連事象が
記載されているのは以下の製剤であった。なお、2022 年 3 月 16 日時点の情報であり、2025 年 3 月 4 日時
点まで変更はなかった。
ビクトーザ皮下注 18 mg(リラグルチド(遺伝子組換え))(以下、「ビクトーザ」)は、肝胆道系
障害に、肝機能異常(0.2~1%)及び臨床検査(AST、ALT 増加)(0.2~1%)
バイエッタ皮下注 5μg ペン 300 及び同 10 μg ペン 300(エキセナチド)は、肝胆道系障害に肝機
能異常(1%未満)
ビデュリオン皮下注用 2 mg ペン及び同皮下注用 2 mg(エキセナチド)は、肝胆道系障害に肝機能
異常(1%未満)
ゾルトファイ配合注フレックスタッチ(インスリン デグルデク(遺伝子組換え)・リラグルチド
(遺伝子組換え))は、肝胆道系障害に肝機能異常(AST、ALT の上昇等)(頻度不明)
AST:アスパラギン酸アミノトランスフェラーゼ、ALT:アラニンアミノトランスフェラーゼ
調査目的
MID-NETⓇを用いて、GLP-1 受容体作動薬が処方された 2 型糖尿病患者において、トル
リシティ処方患者とその他の GLP-1 受容体作動薬処方患者の肝機能障害の発現状況を
比較する。
MID-NET 選定理由
:臨床検査値を指標とした評価を実施するために選択
の 選 定 理 データ期間 :2009 年 1 月 1 日~2022 年 3 月 31 日
由とデー
データ期間に利用可能であった MID-NET®協力医療機関(10 拠点 22 病
タ期間
院)のデータを利用
調 査 方 法 ◼ 調査デザイン:New User Cohort デザイン
の概略
◼ 調査対象集団:GLP-1 受容体作動薬が新規で処方された患者
®
本調査は、GLP-1 受容体作動薬の効能・効果である 2 型糖尿病の患者を対象として、
表 1 の全ての組入れ基準を満たし、いずれの除外基準も満たさない患者を調査対象
集団に設定した。
1
14 / 20