よむ、つかう、まなぶ。
資料1-2 MID-NET・NDB の行政利活用の調査実施状況について[894KB] (15 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
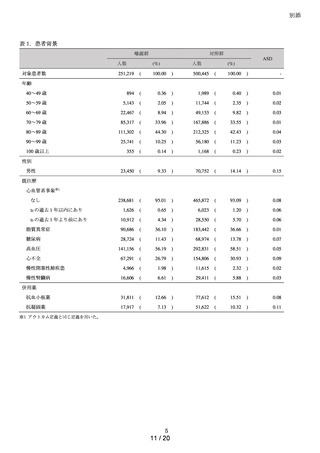
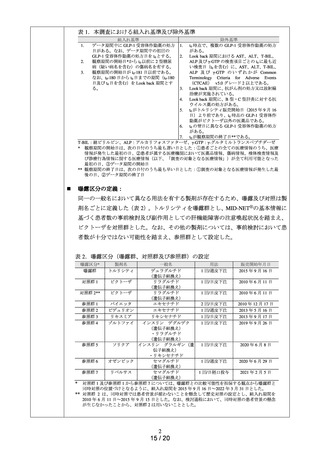
表 1.本調査における組入れ基準及び除外基準
除外基準
t0 時点で、複数の GLP-1 受容体作動薬の処方
がある。
2. Look back 期間における AST、ALT、T-BIL、
2.
ALP 及び γ-GTP の検査項目ごとの t0 に最も近
い検査日(t0 を含む)に、AST、ALT、T-BIL、
3.
ALP 及 び γ-GTP の い ず れ か が Common
Terminology Criteria for Adverse Events
(CTCAE) v5.0 グレード 2 以上である。
3. Look back 期間に、抗がん剤の処方又は放射線
治療が実施されている。
4. Look back 期間に、B 型・C 型肝炎に対する抗
ウイルス薬の処方がある。
5. t0 がトルリシティ販売開始日(2015 年 9 月 16
日)より前であり、t0 時点の GLP-1 受容体作
動薬がビクトーザ以外の医薬品である。
6. t0 の翌日に異なる GLP-1 受容体作動薬の処方
がある。
7. t0 が観察期間の終了日**である。
T-BIL:総ビリルビン、ALP:アルカリフォスファターゼ、γ-GTP:γ-グルタミルトランスペプチダーゼ
* 観察期間の開始日は、次の日付のうち最も遅い日とした:①患者ごとの全ての医療情報のうち、医療
情報が発生した最初の日、②患者が属する医療機関において医薬品情報、傷病情報、検体検査情報及
び診療行為情報に関する医療情報(以下、「調査の対象となる医療情報」)が全て利用可能となった
最初の日、③データ期間の開始日
** 観察期間の終了日は、次の日付のうち最も早い日とした:①調査の対象となる医療情報が発生した最
後の日、②データ期間の終了日
1.
◼
組入れ基準
データ期間中に GLP-1 受容体作動薬の処方
日がある。なお、データ期間中の初回の
GLP-1 受容体作動薬の処方日を t0 とする。
観察期間の開始日*から t0 以前に 2 型糖尿
病(疑い病名を含む)の傷病名を有する。
観察期間の開始日が t0-181 日以前である。
なお、t0-180 日から t0 日までの期間(t0-180
日及び t0 日を含む)を Look back 期間とす
る。
1.
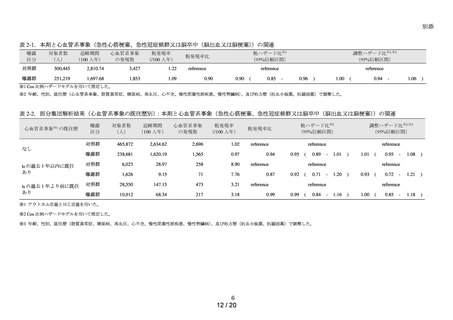
曝露区分の定義:
同一の一般名において異なる用法を有する製剤が存在するため、曝露及び対照は製
剤名ごとに定義した(表 2)。トルリシティを曝露群とし、MID-NETⓇの基本情報に
基づく患者数の事前検討及び副作用としての肝機能障害の注意喚起状況を踏まえ、
ビクトーザを対照群とした。なお、その他の製剤については、事前検討において患
者数が十分ではない可能性を踏まえ、参照群として設定した。
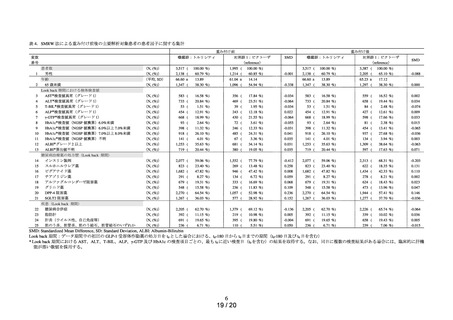
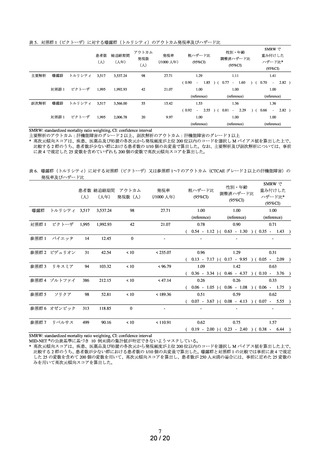
表 2.曝露区分(曝露群、対照群及び参照群)の設定
曝露区分*
曝露群
製剤名
トルリシティ
一般名
用法
販売開始年月日
デュラグルチド
1 回/週皮下注
2015 年 9 月 16 日
(遺伝子組換え)
対照群 1
ビクトーザ
リラグルチド
1 回/日皮下注
2010 年 6 月 11 日
(遺伝子組換え)
対照群 2**
ビクトーザ
リラグルチド
1 回/日皮下注
2010 年 6 月 11 日
(遺伝子組換え)
参照群 1
バイエッタ
エキセナチド
2 回/日皮下注
2010 年 12 月 17 日
参照群 2
ビデュリオン
エキセナチド
1 回/週皮下注
2013 年 5 月 16 日
参照群 3
リキスミア
リキシセナチド
1 回/日皮下注
2013 年 9 月 17 日
参照群 4
ゾルトファイ
インスリン デグルデク
1 回/日皮下注
2019 年 9 月 26 日
(遺伝子組換え)
・リラグルチド
(遺伝子組換え)
参照群 5
ソリクア
インスリン グラルギン(遺
1 回/日皮下注
2020 年 6 月 8 日
伝子組換え)
・リキシセナチド
参照群 6
オゼンピック
セマグルチド
1 回/週皮下注
2020 年 6 月 29 日
(遺伝子組換え)
参照群 7
リベルサス
セマグルチド
1 回/日経口投与
2021 年 2 月 5 日
(遺伝子組換え)
* 対照群 1 及び参照群 1 から参照群 7 については、曝露群との比較可能性を担保する観点から曝露群と
同時対照の位置づけとなるように、組入れ期間を 2015 年 9 月 16 日~2022 年 3 月 31 日とした。
** 対照群 2 は、同時対照では患者背景が揃わないことを懸念して歴史対照の設定とし、組入れ期間を
2010 年 6 月 11 日~2015 年 9 月 15 日とした。なお、検討過程において、同時対照の患者背景の懸念
が生じなかったことから、対照群 2 は用いないこととした。
2
15 / 20
除外基準
t0 時点で、複数の GLP-1 受容体作動薬の処方
がある。
2. Look back 期間における AST、ALT、T-BIL、
2.
ALP 及び γ-GTP の検査項目ごとの t0 に最も近
い検査日(t0 を含む)に、AST、ALT、T-BIL、
3.
ALP 及 び γ-GTP の い ず れ か が Common
Terminology Criteria for Adverse Events
(CTCAE) v5.0 グレード 2 以上である。
3. Look back 期間に、抗がん剤の処方又は放射線
治療が実施されている。
4. Look back 期間に、B 型・C 型肝炎に対する抗
ウイルス薬の処方がある。
5. t0 がトルリシティ販売開始日(2015 年 9 月 16
日)より前であり、t0 時点の GLP-1 受容体作
動薬がビクトーザ以外の医薬品である。
6. t0 の翌日に異なる GLP-1 受容体作動薬の処方
がある。
7. t0 が観察期間の終了日**である。
T-BIL:総ビリルビン、ALP:アルカリフォスファターゼ、γ-GTP:γ-グルタミルトランスペプチダーゼ
* 観察期間の開始日は、次の日付のうち最も遅い日とした:①患者ごとの全ての医療情報のうち、医療
情報が発生した最初の日、②患者が属する医療機関において医薬品情報、傷病情報、検体検査情報及
び診療行為情報に関する医療情報(以下、「調査の対象となる医療情報」)が全て利用可能となった
最初の日、③データ期間の開始日
** 観察期間の終了日は、次の日付のうち最も早い日とした:①調査の対象となる医療情報が発生した最
後の日、②データ期間の終了日
1.
◼
組入れ基準
データ期間中に GLP-1 受容体作動薬の処方
日がある。なお、データ期間中の初回の
GLP-1 受容体作動薬の処方日を t0 とする。
観察期間の開始日*から t0 以前に 2 型糖尿
病(疑い病名を含む)の傷病名を有する。
観察期間の開始日が t0-181 日以前である。
なお、t0-180 日から t0 日までの期間(t0-180
日及び t0 日を含む)を Look back 期間とす
る。
1.
曝露区分の定義:
同一の一般名において異なる用法を有する製剤が存在するため、曝露及び対照は製
剤名ごとに定義した(表 2)。トルリシティを曝露群とし、MID-NETⓇの基本情報に
基づく患者数の事前検討及び副作用としての肝機能障害の注意喚起状況を踏まえ、
ビクトーザを対照群とした。なお、その他の製剤については、事前検討において患
者数が十分ではない可能性を踏まえ、参照群として設定した。
表 2.曝露区分(曝露群、対照群及び参照群)の設定
曝露区分*
曝露群
製剤名
トルリシティ
一般名
用法
販売開始年月日
デュラグルチド
1 回/週皮下注
2015 年 9 月 16 日
(遺伝子組換え)
対照群 1
ビクトーザ
リラグルチド
1 回/日皮下注
2010 年 6 月 11 日
(遺伝子組換え)
対照群 2**
ビクトーザ
リラグルチド
1 回/日皮下注
2010 年 6 月 11 日
(遺伝子組換え)
参照群 1
バイエッタ
エキセナチド
2 回/日皮下注
2010 年 12 月 17 日
参照群 2
ビデュリオン
エキセナチド
1 回/週皮下注
2013 年 5 月 16 日
参照群 3
リキスミア
リキシセナチド
1 回/日皮下注
2013 年 9 月 17 日
参照群 4
ゾルトファイ
インスリン デグルデク
1 回/日皮下注
2019 年 9 月 26 日
(遺伝子組換え)
・リラグルチド
(遺伝子組換え)
参照群 5
ソリクア
インスリン グラルギン(遺
1 回/日皮下注
2020 年 6 月 8 日
伝子組換え)
・リキシセナチド
参照群 6
オゼンピック
セマグルチド
1 回/週皮下注
2020 年 6 月 29 日
(遺伝子組換え)
参照群 7
リベルサス
セマグルチド
1 回/日経口投与
2021 年 2 月 5 日
(遺伝子組換え)
* 対照群 1 及び参照群 1 から参照群 7 については、曝露群との比較可能性を担保する観点から曝露群と
同時対照の位置づけとなるように、組入れ期間を 2015 年 9 月 16 日~2022 年 3 月 31 日とした。
** 対照群 2 は、同時対照では患者背景が揃わないことを懸念して歴史対照の設定とし、組入れ期間を
2010 年 6 月 11 日~2015 年 9 月 15 日とした。なお、検討過程において、同時対照の患者背景の懸念
が生じなかったことから、対照群 2 は用いないこととした。
2
15 / 20