よむ、つかう、まなぶ。
参考資料8 「定期の予防接種等による副反応疑いの報告等の取扱いについて」の一部改正について(令和4年3月18日付け健発0318第19号・薬生発0318第13号厚生労働省健康局長及び医薬・生活衛生局長連名通知) (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00053.html |
| 出典情報 | 第87回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第16回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
品質、有効性及び安全性の確保等に関する法律第 68 条の 10 第2項の規定による
報告をする必要はないこと。
(5)患者に対して予防接種を行った医師等以外が、(1)の報告をする場合において
は、記載が困難な事項については、記載する必要はないこと。
(6)厚生労働省、国立感染症研究所又は機構が(1)の報告に関する調査を行うこと
があるので、医療機関の関係者等は、予防接種法第 13 条第4項の規定に基づき、
厚生労働省等から副反応疑い報告に関する情報収集等の協力依頼がなされた際に
は、これに協力すること。
(7)(1)の報告の内容については、厚生労働省、国立感染症研究所又は機構におい
て調査等を実施した後、個人情報に十分配慮した上で、公開の場で検討すること
とするものであること。
(8)厚生労働大臣が(1)の報告に関して検討を加えた結果については、都道府県を
通じて市町村に通知することがあるので、その際には、都道府県は、市町村に対
して、速やかに管内の関係機関へ周知するよう依頼すること。
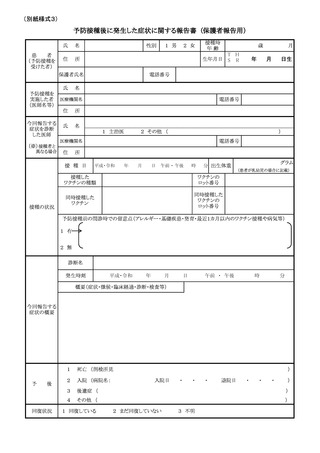
(9)市町村が被接種者又は保護者(以下「保護者等」という。)からの定期の予防接
種等後に発生した健康被害に関し相談を受けた場合等には、必要に応じて、別紙
様式3に必要事項を記入するよう促すとともに、それを都道府県を通じて、厚生
労働省健康局健康課へ電子メール(メールアドレス:yoboseshu@mhlw.go.jp)に
て報告すること。
この場合において、市町村は当該健康被害を診断した医師等に対し、(1)の
報告の提出を促すとともに、医師等が報告基準に該当せず因果関係もないと判断
しているなどの理由により、報告をしない場合には、その理由も添えて厚生労働
省へ報告すること。
2 任意接種における健康被害の報告
都道府県及び市町村は、定期の予防接種以外の予防接種(以下「任意接種」とい
う。)のみを行う医療機関に対しても、別紙様式1及び全種調査票を配布並びに別紙
様式2を周知し、当該報告への協力を求めること。任意接種における健康被害につい
ては、「医薬関係者からの医薬品、医療機器、再生医療等製品、医薬部外品及び化粧
品の副作用、感染症及び不具合報告の実施要領について」(令和4年3月 18 日付け薬
生発 0318 第1号)の別添「医薬品・医療機器等安全性情報報告制度」実施要領の
「(2)報告対象となる情報」に該当する疾病、障害若しくは死亡の発生又は感染症
の発生であり、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律
第 68 条の 10 第2項の規定に基づき、薬局開設者、病院若しくは診療所の開設者又は
医師、歯科医師、薬剤師その他医薬関係者は、保健衛生上の危害の発生又は拡大を防
止するため必要があると認めるとき(別記①~⑨参照)は、1(1)と同様に、別紙
様式1又は2を用い、
速 や か に 機 構 へ FAX( FAX 番 号 : 0120-176-146) 又 は 電 子 報 告 シ ス テ ム
報告をする必要はないこと。
(5)患者に対して予防接種を行った医師等以外が、(1)の報告をする場合において
は、記載が困難な事項については、記載する必要はないこと。
(6)厚生労働省、国立感染症研究所又は機構が(1)の報告に関する調査を行うこと
があるので、医療機関の関係者等は、予防接種法第 13 条第4項の規定に基づき、
厚生労働省等から副反応疑い報告に関する情報収集等の協力依頼がなされた際に
は、これに協力すること。
(7)(1)の報告の内容については、厚生労働省、国立感染症研究所又は機構におい
て調査等を実施した後、個人情報に十分配慮した上で、公開の場で検討すること
とするものであること。
(8)厚生労働大臣が(1)の報告に関して検討を加えた結果については、都道府県を
通じて市町村に通知することがあるので、その際には、都道府県は、市町村に対
して、速やかに管内の関係機関へ周知するよう依頼すること。
(9)市町村が被接種者又は保護者(以下「保護者等」という。)からの定期の予防接
種等後に発生した健康被害に関し相談を受けた場合等には、必要に応じて、別紙
様式3に必要事項を記入するよう促すとともに、それを都道府県を通じて、厚生
労働省健康局健康課へ電子メール(メールアドレス:yoboseshu@mhlw.go.jp)に
て報告すること。
この場合において、市町村は当該健康被害を診断した医師等に対し、(1)の
報告の提出を促すとともに、医師等が報告基準に該当せず因果関係もないと判断
しているなどの理由により、報告をしない場合には、その理由も添えて厚生労働
省へ報告すること。
2 任意接種における健康被害の報告
都道府県及び市町村は、定期の予防接種以外の予防接種(以下「任意接種」とい
う。)のみを行う医療機関に対しても、別紙様式1及び全種調査票を配布並びに別紙
様式2を周知し、当該報告への協力を求めること。任意接種における健康被害につい
ては、「医薬関係者からの医薬品、医療機器、再生医療等製品、医薬部外品及び化粧
品の副作用、感染症及び不具合報告の実施要領について」(令和4年3月 18 日付け薬
生発 0318 第1号)の別添「医薬品・医療機器等安全性情報報告制度」実施要領の
「(2)報告対象となる情報」に該当する疾病、障害若しくは死亡の発生又は感染症
の発生であり、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律
第 68 条の 10 第2項の規定に基づき、薬局開設者、病院若しくは診療所の開設者又は
医師、歯科医師、薬剤師その他医薬関係者は、保健衛生上の危害の発生又は拡大を防
止するため必要があると認めるとき(別記①~⑨参照)は、1(1)と同様に、別紙
様式1又は2を用い、
速 や か に 機 構 へ FAX( FAX 番 号 : 0120-176-146) 又 は 電 子 報 告 シ ス テ ム