よむ、つかう、まなぶ。
【資料5-1】医薬品等行政評価・監視委員会における海外調査(個別医薬品の欧米での承認状況) (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_30030.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第10回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
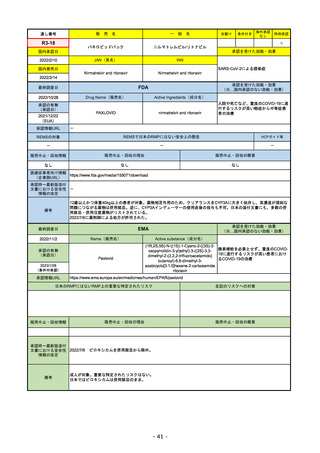
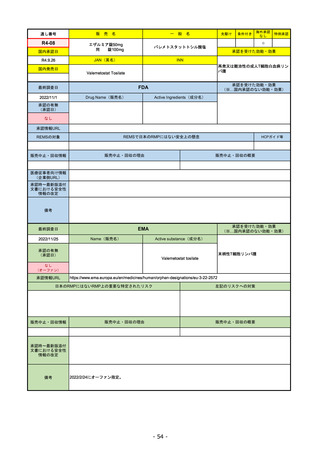
販
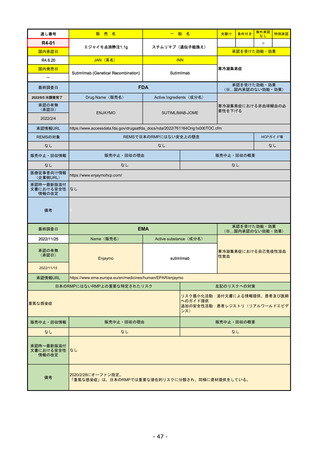
通し番号
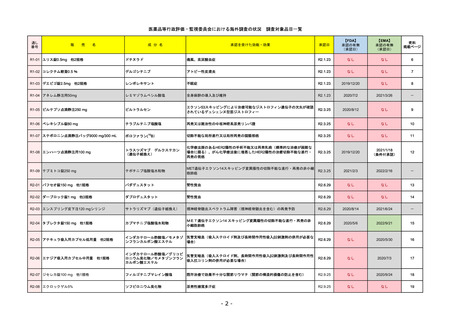
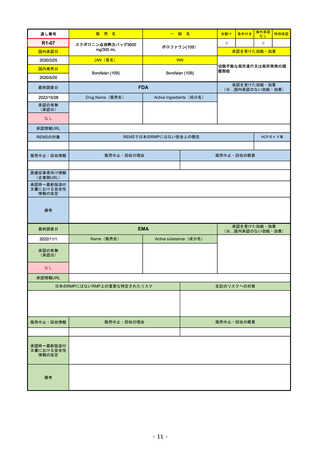
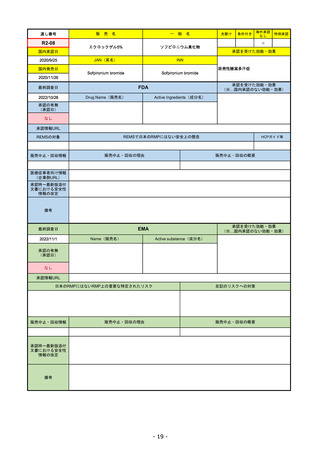
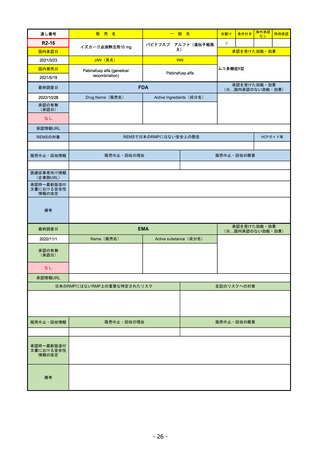
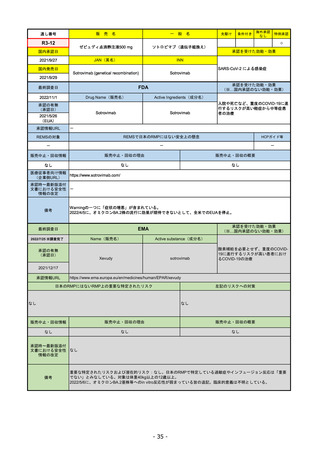
R2-07
売
名
一
般
名
フィルゴチニブマレイン酸塩
国内承認日
ジセレカ錠100 mg
同 錠200 mg
2020/9/25
JAN(英名)
INN
Filgotinib maleate
Filgotinib
国内発売日
先駆け
条件付き
海外承認
なし
特例承認
0
0
○
0
承認を受けた効能・効果
既存治療で効果不十分な関節リウマチ
(関節の構造的損傷の防止を含む)
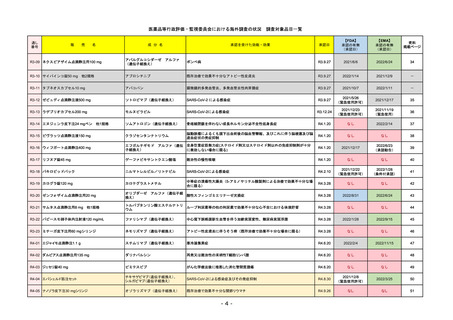
2020/11/18
承認を受けた効能・効果
(※…国内承認のない効能・効果)
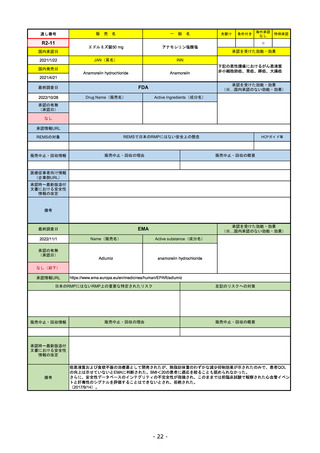
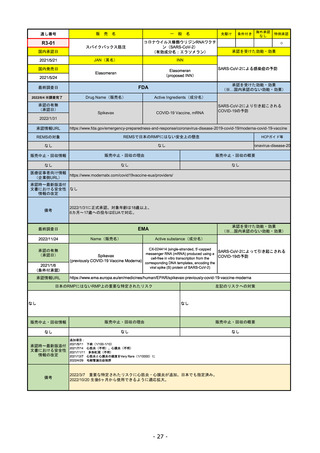
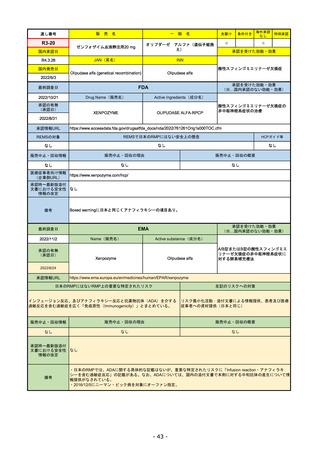
FDA
最終調査日
2022/10/28
承認の有無
(承認日)
Drug Name(販売名)
Active Ingredients(成分名)
0
0
0
なし
承認情報URL
0
REMSの対象
REMSで日本のRMPにはない安全上の懸念
HCPガイド等
0
0
0
販売中止・回収情報
販売中止・回収の理由
販売中止・回収の概要
0
0
0
医療従事者向け情報
(企業側URL)
承認時~最新版添付
文書における安全性 0
情報の改定
0
備考
2022/7/22 ※調査完了
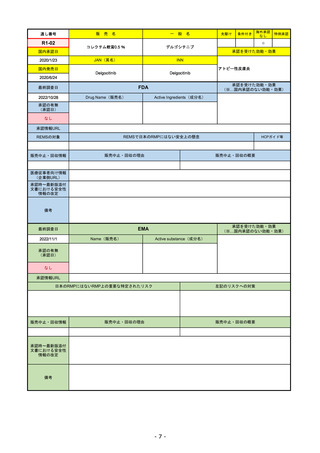
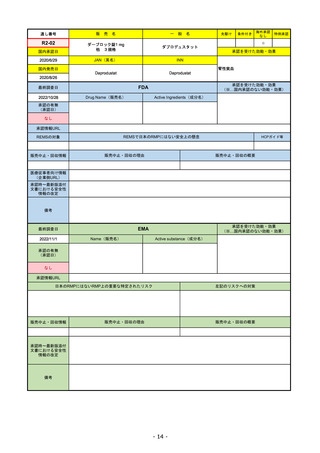
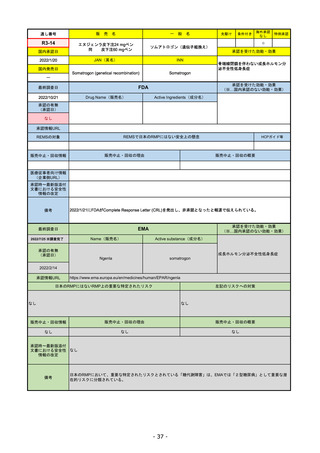
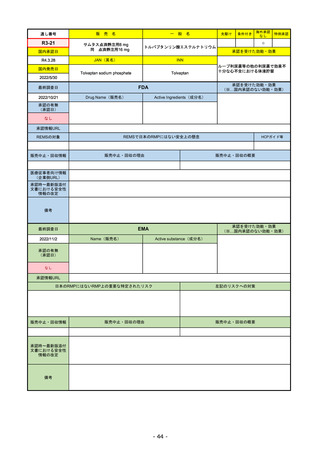
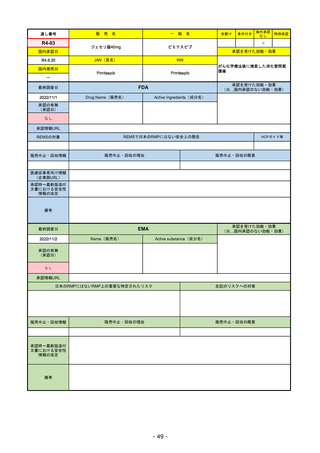
承認の有無
(承認日)
承認を受けた効能・効果
(※…国内承認のない効能・効果)
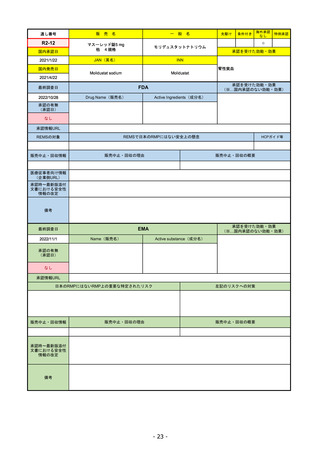
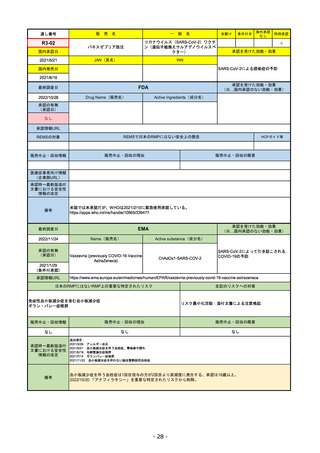
EMA
最終調査日
Name(販売名)
Active substance(成分名)
Jyseleca
filgotinib maleate
2020/9/24
承認情報URL
1つまたは複数の疾患修飾性抗リウマチ
薬への反応性が不十分であるかまたは
不耐性の、中等度から重度の活動性関
節リウマチ
※既存の治療が有効でない中等度から
重度の活動性潰瘍性大腸炎
https://www.ema.europa.eu/en/medicines/human/EPAR/jyseleca
日本のRMPにはないRMP上の重要な特定されたリスク
左記のリスクへの対策
なし
なし
販売中止・回収情報
販売中止・回収の理由
販売中止・回収の概要
なし
なし
なし
承認時~最新版添付 2021/11/16 関節リウマチ(RA)に潰瘍性大腸炎(UC)の適応が加わったため、RMPもRAとUCを適宜分けて表記するよ
文書における安全性
うに記載ぶりを変更。UCに特異的な安全性上の懸念はないが、承認後の観察研究を追加。
情報の改定
備考
重要な特定されたリスクは「日和見感染症」と「帯状疱疹」で、いずれも日本のRMPに記載されている。
2021/11/12に活動性潰瘍性大腸炎の適応が追加。
- 18 -
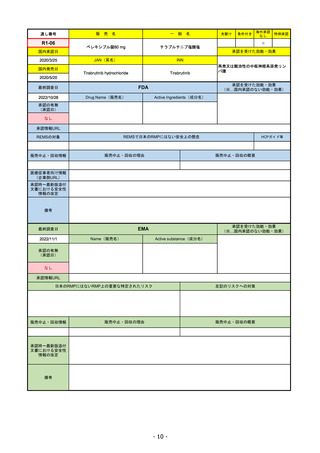
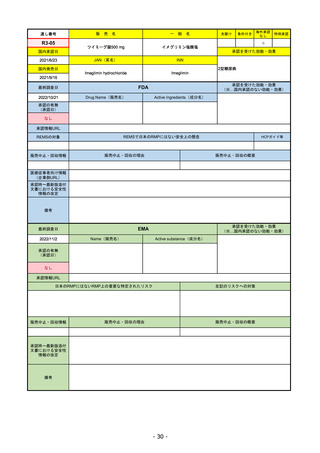
通し番号
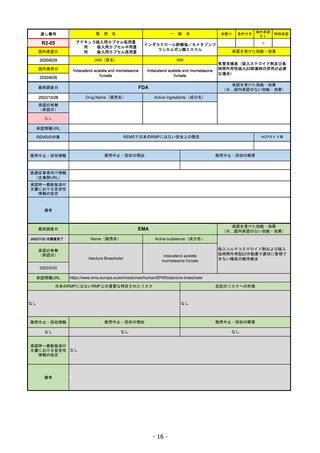
R2-07
売
名
一
般
名
フィルゴチニブマレイン酸塩
国内承認日
ジセレカ錠100 mg
同 錠200 mg
2020/9/25
JAN(英名)
INN
Filgotinib maleate
Filgotinib
国内発売日
先駆け
条件付き
海外承認
なし
特例承認
0
0
○
0
承認を受けた効能・効果
既存治療で効果不十分な関節リウマチ
(関節の構造的損傷の防止を含む)
2020/11/18
承認を受けた効能・効果
(※…国内承認のない効能・効果)
FDA
最終調査日
2022/10/28
承認の有無
(承認日)
Drug Name(販売名)
Active Ingredients(成分名)
0
0
0
なし
承認情報URL
0
REMSの対象
REMSで日本のRMPにはない安全上の懸念
HCPガイド等
0
0
0
販売中止・回収情報
販売中止・回収の理由
販売中止・回収の概要
0
0
0
医療従事者向け情報
(企業側URL)
承認時~最新版添付
文書における安全性 0
情報の改定
0
備考
2022/7/22 ※調査完了
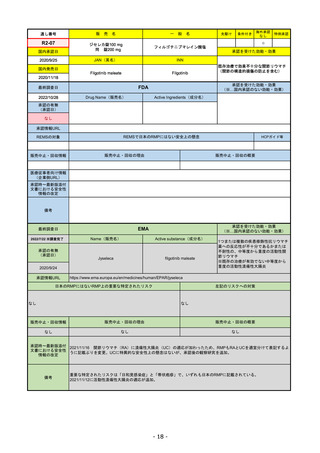
承認の有無
(承認日)
承認を受けた効能・効果
(※…国内承認のない効能・効果)
EMA
最終調査日
Name(販売名)
Active substance(成分名)
Jyseleca
filgotinib maleate
2020/9/24
承認情報URL
1つまたは複数の疾患修飾性抗リウマチ
薬への反応性が不十分であるかまたは
不耐性の、中等度から重度の活動性関
節リウマチ
※既存の治療が有効でない中等度から
重度の活動性潰瘍性大腸炎
https://www.ema.europa.eu/en/medicines/human/EPAR/jyseleca
日本のRMPにはないRMP上の重要な特定されたリスク
左記のリスクへの対策
なし
なし
販売中止・回収情報
販売中止・回収の理由
販売中止・回収の概要
なし
なし
なし
承認時~最新版添付 2021/11/16 関節リウマチ(RA)に潰瘍性大腸炎(UC)の適応が加わったため、RMPもRAとUCを適宜分けて表記するよ
文書における安全性
うに記載ぶりを変更。UCに特異的な安全性上の懸念はないが、承認後の観察研究を追加。
情報の改定
備考
重要な特定されたリスクは「日和見感染症」と「帯状疱疹」で、いずれも日本のRMPに記載されている。
2021/11/12に活動性潰瘍性大腸炎の適応が追加。
- 18 -