よむ、つかう、まなぶ。
【資料4】医薬品等行政評価・監視委員会における海外調査 (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_33889.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第12回 6/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
販
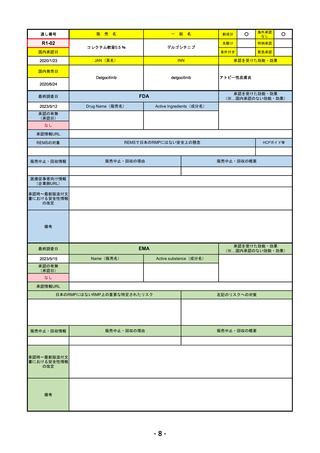
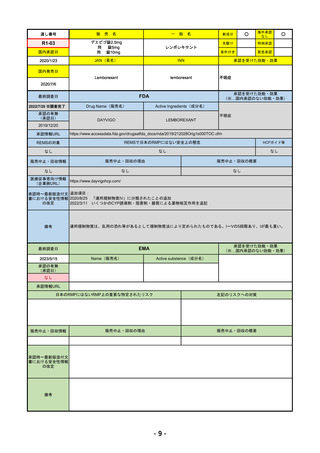
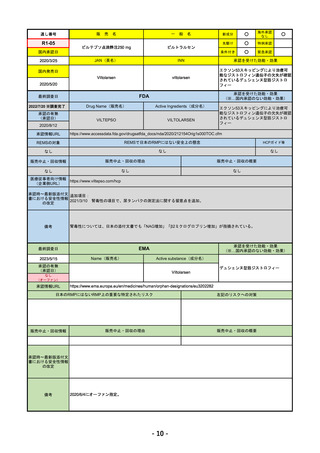
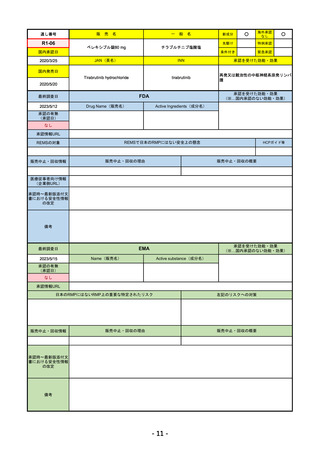
通し番号
R4-04
売
名
一
国内承認日
○
海外承認
なし
0
先駆け
0
特例承認
○
条件付き
0
緊急承認
0
INN
承認を受けた効能・効果
Tixagevimab (genetical recombination)
and cilgavimab (genetical recombination)
0
SARS-CoV-2による感染症及びその発症
抑制
承認を受けた効能・効果
(※…国内承認のない効能・効果)
FDA
最終調査日
2023/5/15
Drug Name(販売名)
Active Ingredients(成分名)
承認の有無
(承認日)
EVUSHELD
TIXAGEVIMAB CO-PACKAGED WITH
CILGAVIMAB
2021/12/8
(EUA)
承認情報URL
新成分
JAN(英名)
2022/8/30
2022/8/31
名
チキサゲビマブ(遺伝子組換え)、シル
ガビマブ(遺伝子組換え)
エバシェルド筋注セット
国内発売日
般
SARS-CoV-2に感染しておらず、感染者との最近の
接触歴もない下記の者における感染の曝露前予防
1)中等度~重度の免疫不全によりワクチンの効果
が期待できない
2)重篤な副作用履歴のため予定通りのワクチン投
与ができない
-
REMSの対象
REMSで日本のRMPにはない安全上の懸念
HCPガイド等
-
-
-
販売中止・回収情報
販売中止・回収の理由
販売中止・回収の概要
なし
なし
なし
医療従事者向け情報
https://www.evusheld.com/en/hcp
(企業側URL)
承認時~最新版添付文
書における安全性情報 -
の改定
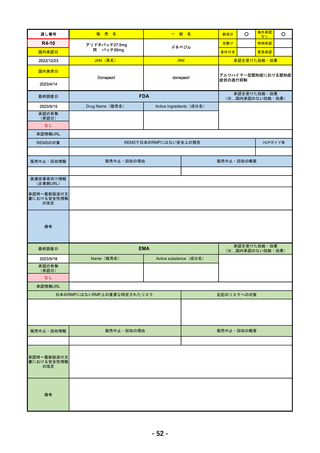
国内承認には「SARS-CoV-2による感染」の適応が含まれるが、EUAの対象は「曝露前予防」のみ。
2023/1/26 本剤非感受性株の割合が高いうちはEUAを一旦停止することとされた。但し、政府は将来的に本剤によって中和
される変異株が流行する場合に備えて、医療機関や関係企業において本剤を保持しておくことを推奨している。
備考
承認を受けた効能・効果
(※…国内承認のない効能・効果)
EMA
最終調査日
2022/12/3 ※調査完了
Name(販売名)
Active substance(成分名)
承認の有無
(承認日)
Evusheld
Tixagevimab and cilgavimab
COVID-19の曝露前予防
酸素補充療法を必要とせず重症化のリス
クが高い患者におけるCOVID-19の治療
2022/3/25
承認情報URL
https://www.ema.europa.eu/en/medicines/human/EPAR/evusheld
日本のRMPにはないRMP上の重要な特定されたリスク
なし
左記のリスクへの対策
なし
販売中止・回収情報
販売中止・回収の理由
販売中止・回収の概要
なし
なし
なし
承認時~最新版添付文 なし
書における安全性情報
(治療の適応が後から追加されたが、その安全性プロファイルは予防の治験で得られたものと同様)
の改定
備考
重要な特定されたリスクは「なし」。日本のRMPで挙げられる「アナフィラキシー等の重篤な過敏症」については、臨床試
験において重篤な有害事象が報告されていないこと等をもって、安全上の懸念事項には含めない旨積極的に判断されてい
る。
2022/9/16 治療に関する適応を取得。
- 46 -
通し番号
R4-04
売
名
一
国内承認日
○
海外承認
なし
0
先駆け
0
特例承認
○
条件付き
0
緊急承認
0
INN
承認を受けた効能・効果
Tixagevimab (genetical recombination)
and cilgavimab (genetical recombination)
0
SARS-CoV-2による感染症及びその発症
抑制
承認を受けた効能・効果
(※…国内承認のない効能・効果)
FDA
最終調査日
2023/5/15
Drug Name(販売名)
Active Ingredients(成分名)
承認の有無
(承認日)
EVUSHELD
TIXAGEVIMAB CO-PACKAGED WITH
CILGAVIMAB
2021/12/8
(EUA)
承認情報URL
新成分
JAN(英名)
2022/8/30
2022/8/31
名
チキサゲビマブ(遺伝子組換え)、シル
ガビマブ(遺伝子組換え)
エバシェルド筋注セット
国内発売日
般
SARS-CoV-2に感染しておらず、感染者との最近の
接触歴もない下記の者における感染の曝露前予防
1)中等度~重度の免疫不全によりワクチンの効果
が期待できない
2)重篤な副作用履歴のため予定通りのワクチン投
与ができない
-
REMSの対象
REMSで日本のRMPにはない安全上の懸念
HCPガイド等
-
-
-
販売中止・回収情報
販売中止・回収の理由
販売中止・回収の概要
なし
なし
なし
医療従事者向け情報
https://www.evusheld.com/en/hcp
(企業側URL)
承認時~最新版添付文
書における安全性情報 -
の改定
国内承認には「SARS-CoV-2による感染」の適応が含まれるが、EUAの対象は「曝露前予防」のみ。
2023/1/26 本剤非感受性株の割合が高いうちはEUAを一旦停止することとされた。但し、政府は将来的に本剤によって中和
される変異株が流行する場合に備えて、医療機関や関係企業において本剤を保持しておくことを推奨している。
備考
承認を受けた効能・効果
(※…国内承認のない効能・効果)
EMA
最終調査日
2022/12/3 ※調査完了
Name(販売名)
Active substance(成分名)
承認の有無
(承認日)
Evusheld
Tixagevimab and cilgavimab
COVID-19の曝露前予防
酸素補充療法を必要とせず重症化のリス
クが高い患者におけるCOVID-19の治療
2022/3/25
承認情報URL
https://www.ema.europa.eu/en/medicines/human/EPAR/evusheld
日本のRMPにはないRMP上の重要な特定されたリスク
なし
左記のリスクへの対策
なし
販売中止・回収情報
販売中止・回収の理由
販売中止・回収の概要
なし
なし
なし
承認時~最新版添付文 なし
書における安全性情報
(治療の適応が後から追加されたが、その安全性プロファイルは予防の治験で得られたものと同様)
の改定
備考
重要な特定されたリスクは「なし」。日本のRMPで挙げられる「アナフィラキシー等の重篤な過敏症」については、臨床試
験において重篤な有害事象が報告されていないこと等をもって、安全上の懸念事項には含めない旨積極的に判断されてい
る。
2022/9/16 治療に関する適応を取得。
- 46 -