よむ、つかう、まなぶ。
資料2-2 MID-NET・NDBの行政利活用の調査実施状況について[1.4MB] (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(以下、「CTCAE」)Grade 3 以上相当)を好中球数減少と定義した。
追跡期間
アウトカムの発生を確認する追跡期間は、新規処方日を起点として、①アウトカム
の発現日、②処方継続期間*4 の終了日、③新規処方日に処方された医薬品と異なる
群の医薬品、インフリキシマブ(遺伝子組換え)又はセルトリズマブ
ペゴル(遺
伝子組換え)の処方日、④がん化学療法剤又はクロザピンの処方日、⑤最終の医療
記録発生日又は⑥データ期間の終了日のうち、最も早い日までの期間とした。
*4 注射剤(アプレミラスト以外の医薬品)については、先行する処方期間の終了日と後続の処方期間の開始
日が 30 日(以下、「Gap period」)未満の場合に、処方が継続しているとみなして連結した期間とし、アプ
レミラストについては飲み残しの可能性を考慮して処方が継続しているとみなして連結した期間に 28 日
(以下、「Grace period」)を加えた期間とした。なお、注射剤のうち自己投与が認められていない医薬品
については、用法及び用法で定められた維持期における処方間隔を基に処方期間を設定し、注射剤のうち
自己投与が認められている医薬品については維持期における処方間隔及び処方された製剤数を基に処方期
間を設定した。
解析項目及び方法
<主解析>
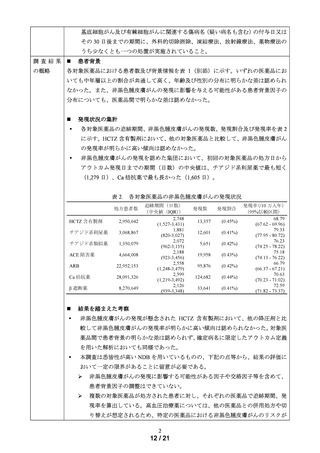
9 つの曝露群について、Cox 比例ハザードモデルを用いてアダリムマブ群に対する
粗ハザード比及び傾向スコアの逆数で重み付けを行った調整ハザード比を推定し
た。なお、傾向スコアは、各曝露群及び対照群それぞれの組合せに対して、ロジス
ティック回帰モデルを用いて推定した。
<副次解析>
Cox 比例ハザードモデルを用いて抗 IL-17 抗体製剤群及びアプレミラスト群に対す
る抗 IL-23 抗体製剤群の粗ハザード比及び傾向スコアの逆数で重み付けを行った調
整ハザード比をそれぞれ推定した。
<感度解析>
主解析及び副次解析の頑健性を確認する目的で、主解析及び副次解析について以下
のとおり条件を変更した場合における調整ハザード比を推定した。
感度解析①:アウトカム定義を好中球数 500/µL 未満(CTCAE Grade 4 相当)に
変更した場合
感度解析②:アウトカム定義を好中球数 1,500/µL 未満(CTCAE Grade 2 以上相
当)に変更した場合
感度解析③:調査対象集団を新規処方日の 90 日前から新規処方日の前日まで
の好中球数が基準範囲内 2,000/µL~7,500/µL にある患者に限定した場合
感度解析④:調査対象集団を新規処方日の 90 日前から新規処方日の前日まで
の好中球数が基準範囲内 2,000/µL~7,500/µL にある患者に限定、及びアウトカ
ム定義を好中球数 1,500/µL 未満に変更した場合
感度解析⑤:Gap period 及び Grace period を主解析の条件の 2 倍に変更した場合
<追加解析>
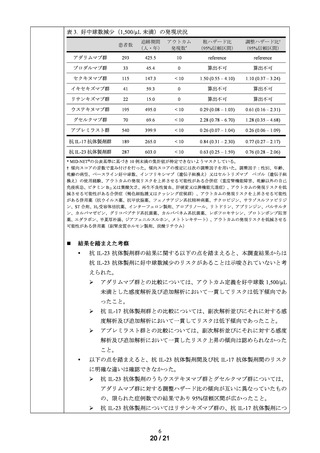
主解析(アウトカム定義:好中球数 1,000/µL 未満)における対照群のアウトカム発
現数が 0 であったことから、好中球数減少のリスクを多角的に検討する目的で、好
中球数 1,500/µL 未満のアウトカム定義に対して、Gap period 及び Grace period を 2
3
17 / 21
追跡期間
アウトカムの発生を確認する追跡期間は、新規処方日を起点として、①アウトカム
の発現日、②処方継続期間*4 の終了日、③新規処方日に処方された医薬品と異なる
群の医薬品、インフリキシマブ(遺伝子組換え)又はセルトリズマブ
ペゴル(遺
伝子組換え)の処方日、④がん化学療法剤又はクロザピンの処方日、⑤最終の医療
記録発生日又は⑥データ期間の終了日のうち、最も早い日までの期間とした。
*4 注射剤(アプレミラスト以外の医薬品)については、先行する処方期間の終了日と後続の処方期間の開始
日が 30 日(以下、「Gap period」)未満の場合に、処方が継続しているとみなして連結した期間とし、アプ
レミラストについては飲み残しの可能性を考慮して処方が継続しているとみなして連結した期間に 28 日
(以下、「Grace period」)を加えた期間とした。なお、注射剤のうち自己投与が認められていない医薬品
については、用法及び用法で定められた維持期における処方間隔を基に処方期間を設定し、注射剤のうち
自己投与が認められている医薬品については維持期における処方間隔及び処方された製剤数を基に処方期
間を設定した。
解析項目及び方法
<主解析>
9 つの曝露群について、Cox 比例ハザードモデルを用いてアダリムマブ群に対する
粗ハザード比及び傾向スコアの逆数で重み付けを行った調整ハザード比を推定し
た。なお、傾向スコアは、各曝露群及び対照群それぞれの組合せに対して、ロジス
ティック回帰モデルを用いて推定した。
<副次解析>
Cox 比例ハザードモデルを用いて抗 IL-17 抗体製剤群及びアプレミラスト群に対す
る抗 IL-23 抗体製剤群の粗ハザード比及び傾向スコアの逆数で重み付けを行った調
整ハザード比をそれぞれ推定した。
<感度解析>
主解析及び副次解析の頑健性を確認する目的で、主解析及び副次解析について以下
のとおり条件を変更した場合における調整ハザード比を推定した。
感度解析①:アウトカム定義を好中球数 500/µL 未満(CTCAE Grade 4 相当)に
変更した場合
感度解析②:アウトカム定義を好中球数 1,500/µL 未満(CTCAE Grade 2 以上相
当)に変更した場合
感度解析③:調査対象集団を新規処方日の 90 日前から新規処方日の前日まで
の好中球数が基準範囲内 2,000/µL~7,500/µL にある患者に限定した場合
感度解析④:調査対象集団を新規処方日の 90 日前から新規処方日の前日まで
の好中球数が基準範囲内 2,000/µL~7,500/µL にある患者に限定、及びアウトカ
ム定義を好中球数 1,500/µL 未満に変更した場合
感度解析⑤:Gap period 及び Grace period を主解析の条件の 2 倍に変更した場合
<追加解析>
主解析(アウトカム定義:好中球数 1,000/µL 未満)における対照群のアウトカム発
現数が 0 であったことから、好中球数減少のリスクを多角的に検討する目的で、好
中球数 1,500/µL 未満のアウトカム定義に対して、Gap period 及び Grace period を 2
3
17 / 21