よむ、つかう、まなぶ。
04【資料1-2】ファイザー株式会社提出資料 (41 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40343.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第25回 5/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
主要目的
B7471014
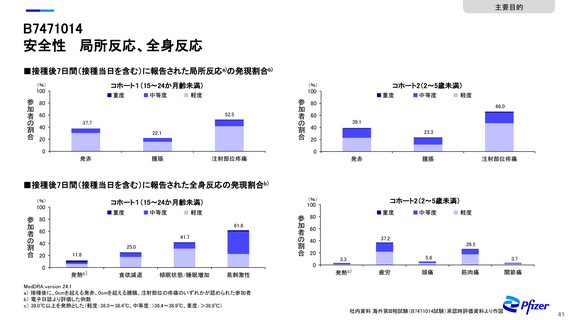
安全性 局所反応、全身反応
■接種後7日間(接種当日を含む)に報告された局所反応a)の発現割合b)
コホート1(15~24か月齢未満)
(%)
100
参
加
者
の
割
合
重度
中等度
軽度
参
加
者
の
割
合
80
52.5
60
37.7
40
コホート2(2~5歳未満)
(%)
100
22.1
20
0
重度
中等度
軽度
80
66.0
60
39.1
40
23.3
20
0
発赤
腫脹
注射部位疼痛
発赤
腫脹
注射部位疼痛
■接種後7日間(接種当日を含む)に報告された全身反応の発現割合b)
(%)
100
参
加
者
の
割
合
(%)
コホート1(15~24か月齢未満)
重度
中等度
軽度
80
61.8
60
41.7
40
20
0
コホート2(2~5歳未満)
100
25.0
11.8
参
加
者
の
割
合
重度
80
中等度
軽度
60
37.2
40
26.5
20
5.6
3.3
3.7
0
発熱c)
食欲減退
傾眠状態/睡眠増加
易刺激性
発熱c)
発熱c)
疲労
頭痛
筋肉痛
関節痛
MedDRA version 24.1
a) 接種後に、0cmを超える発赤、0cmを超える腫脹、注射部位の疼痛のいずれかが認められた参加者
b) 電子日誌より評価した例数
c) 38.0℃以上を発熱とした(軽度:38.0~38.4℃、中等度:>38.4~38.9℃、重度:>38.9℃)
社内資料 海外第III相試験(B7471014試験)承認時評価資料より作図
41
B7471014
安全性 局所反応、全身反応
■接種後7日間(接種当日を含む)に報告された局所反応a)の発現割合b)
コホート1(15~24か月齢未満)
(%)
100
参
加
者
の
割
合
重度
中等度
軽度
参
加
者
の
割
合
80
52.5
60
37.7
40
コホート2(2~5歳未満)
(%)
100
22.1
20
0
重度
中等度
軽度
80
66.0
60
39.1
40
23.3
20
0
発赤
腫脹
注射部位疼痛
発赤
腫脹
注射部位疼痛
■接種後7日間(接種当日を含む)に報告された全身反応の発現割合b)
(%)
100
参
加
者
の
割
合
(%)
コホート1(15~24か月齢未満)
重度
中等度
軽度
80
61.8
60
41.7
40
20
0
コホート2(2~5歳未満)
100
25.0
11.8
参
加
者
の
割
合
重度
80
中等度
軽度
60
37.2
40
26.5
20
5.6
3.3
3.7
0
発熱c)
食欲減退
傾眠状態/睡眠増加
易刺激性
発熱c)
発熱c)
疲労
頭痛
筋肉痛
関節痛
MedDRA version 24.1
a) 接種後に、0cmを超える発赤、0cmを超える腫脹、注射部位の疼痛のいずれかが認められた参加者
b) 電子日誌より評価した例数
c) 38.0℃以上を発熱とした(軽度:38.0~38.4℃、中等度:>38.4~38.9℃、重度:>38.9℃)
社内資料 海外第III相試験(B7471014試験)承認時評価資料より作図
41