よむ、つかう、まなぶ。
参考資料 2 血漿分画製剤のウイルスに対する安全性確保に関するガイドラインの一部改正について(令和6年3月 29 日付け医薬発 0329 第 16 号厚生労働省医薬局長通知) (21 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40647.html |
| 出典情報 | 薬事審議会 血液事業部会運営委員会(令和6年度第1回 6/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
ある。
1.2 対象
本ガイドラインは国内で使用される全ての原血漿、中間原料、及び製品に適用し、安全性確保対策の対
象とするウイルスは、「生物由来原料基準」(平成 15 年厚生労働省告示第 210 号)の「第2 血液製剤総
則」の「2 血漿分画製剤総則」において検査対象とされているB型肝炎ウイルス(HBV)
、C 型肝炎ウイ
ルス(HCV)及びヒト免疫不全ウイルス(HIV)に加え、健康被害をもたらす可能性が指摘され血液に混入
リスクのあるその他のウイルスも含むものとする。
1.2 対象
本ガイドラインは国内で使用されるすべての原料血漿及び製品に適用し、安全性確保対策の対象とする
ウイルスは、当分の間、ヒト免疫不全ウイルス(HIV)、C 型肝炎ウイルス(HCV)及び B 型肝炎ウイルス(HBV)
とする。
1.3 感染性因子
1.3 感染性因子
血漿分画製剤はヒトの血液を原料として製造されることから、血液を介して伝播するウイルスに対する
血漿分画製剤は人間の血液を原料として製造されることから、血液を介して伝播するウイルスに対する
十分な対策を講じなければならない。現在、HBV、HCV 及び HIV 等に係る高い感度のスクリーニング検査や 十分な対策を講じなければならない。現在ではスクリーニング検査、ウイルス除去及び不活化処理が実施
製造工程でのウイルス除去及び不活化処理が実施されており、血漿分画製剤の安全性は格段に向上してい されており、血漿分画製剤の安全性は格段に向上しているが、血液を介したウイルス感染の歴史的経過を
る。一方、血液を介したウイルス感染の歴史的経過を顧みると、ウイルス肝炎についての報告や 1980 年代 顧みると、ウイルス肝炎についての報告もあり、また、1980 年代の血漿分画製剤による HIV 感染も記憶に
の血漿分画製剤による HIV や HCV 感染があったことに加え、その後も国内外で複数の新興・再興感染症の 新しいところである。感染性ウイルスで現在までに明らかになっているものにはヒト免疫不全ウイルス
発症が報告されている。血漿分画製剤の安全性確保の上で問題になりうる主なウイルスとして、B 型肝炎 (HIV)、A 型肝炎ウイルス(HAV)、B 型肝炎ウイルス(HBV)、C 型肝炎ウイルス(HCV)、そしてパルボウイルス
ウイルス(HBV)、C 型肝炎ウイルス(HCV)
、ヒト免疫不全ウイルス(HIV)のほか、A 型肝炎ウイルス(HAV)、 B19 などがある。血漿分画製剤は、多くの人の血漿をプールして製造されるため、十分に検出ができない
E 型肝炎ウイルス(HEV)
、ヒトパルボウイルス B19 などが挙げられる。さらに血漿分画製剤は、多くのヒ ウイルスや未知のウイルスなどが潜在している可能性があり、安全対策を徹底して実施する必要がある。
トの血漿をプールして製造されるため、検査対象とされていないウイルスや未知のウイルスなどが潜在し さらに、原料血液以外の材料、例えば、製造工程で使用する酵素やモノクローナル抗体を用いて製造する
ている可能性があり、安全対策を徹底して実施する必要がある。例えば、新興感染症として新たなウイル 場合における動物由来のウイルス汚染の可能性や製造環境からのウイルス汚染の可能性も推定されるこ
スが出現した場合、原料となる血液に混入するリスクが否定できない場合はウイルス検査の必要性につい とから、注意深く安全対策を講ずることが必要である。
て検討するとともに、製造工程での十分なウイルスクリアランスが得られるか評価する必要がある。さら
に、原血漿以外の材料、例えば、動物由来の酵素やモノクローナル抗体を用いて製造する場合における動
物由来のウイルス汚染の可能性や製造環境からのウイルス汚染の可能性も推定されることから、注意深く
安全対策を講ずることが必要である。
1
序論
1.4 安全性確保の基本
血漿分画製剤のウイルスに対する安全対策は、次に示す複数の方法を適切かつ相補的に行うことにより
達成される。
(1)献(供)血者の問診を行う。
(2)献(供)血血液、ミニプール血漿又はプール血漿のウイルス検査を行う。
(3)製造工程でウイルス除去及び不活化処理を実施する。
(4)必要に応じて、製造工程でのウイルス検査を実施する。
(5)原血漿に関する最新の感染症情報を採血事業者等より入手するよう努める。
(6)採血後情報及び輸血後情報について遡及調査を行う。
(7)製品との関連が疑われる感染症の情報を集める。
1.4 安全性確保の基本
血漿分画製剤のウイルスに対する安全対策は、次に示す複数の方法を適切かつ相補的に行うことにより
達成される。
(1) 献(供)血者の問診を行う。
(2) 血漿のウイルス検査を実施する。
(3) 製造工程でウイルス除去及び不活化処理を実施する。
(4) 最終製品のウイルス検査を実施する。
(5) 採血後情報及び輸血後情報について遡及調査を行う。
1.5 検査の限界
ウイルスの検査方法は技術の進歩とともに向上するため、検査の実施に当たっては常に科学的に最高水
準の検査技術を取り入れるとともに適切に検査を行わなければならない。いかなる検査にも検出限界が存
在するため、ウイルス検査の結果が陰性であっても、ウイルスの存在を完全に否定できないこともある。
また、血液中には検査対象とされていないウイルスや未知のウイルスの存在も考えられる。したがって、
現在採用している検査技術には検出限界のあることを認識し、プールした血漿を原料として製造される血
漿分画製剤は、ウイルスが潜在する可能性を常に有することを前提とした上で安全対策を講ずる必要があ
る。
1.5 検査の限界
ウイルスの検査方法は技術の進歩とともに向上するため、検査の実施に当たっては常に科学的に最高水
準の検査技術を取り入れるとともに適切に検査を行われなければならない。いかなる検査にも検出限界が
存在するため、ウイルス検査の結果が陰性であっても、ウイルスの存在を完全に否定できないこともある。
また、血液中には未知のウイルスの存在も考えられる。したがって、現在採用している検査技術には検出
限界のあることを認識し、プールした血漿を原料として製造される血漿分画製剤は、ウイルスが潜在する
可能性を常に有することを前提とした上で安全対策を講ずる必要がある。
1.6 ウイルスクリアランス試験の役割
原料の血液には常にウイルスが潜在する可能性があることを前提にすると、製造工程においていかに既
知及び未知のウイルスを除去又は不活化できるかが安全対策上重要である。ウイルスクリアランス試験を
実施する目的は、血漿分画製剤の製造工程に導入されているウイルス除去技術及び不活化技術が、期待さ
れた効果をもたらしているか否かを実験的に検証することである。
(改行)
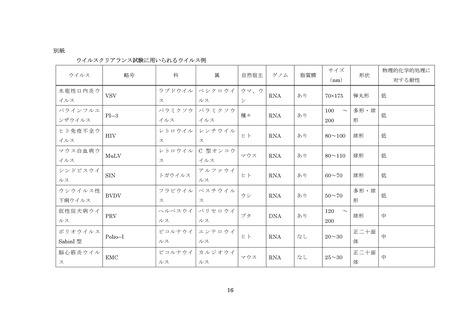
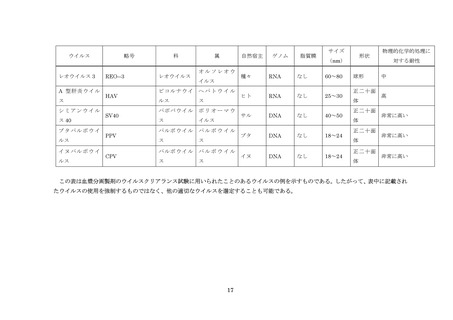
ウイルスクリアランス試験においては、ウイルスの大きさ、形状、脂質膜(エンベロープ)の有無、核
1.6 ウイルス・プロセスバリデーションの役割
原料の血液には常にウイルス潜在の可能性のあることを前提にすると、製造工程においていかに既知の
ウイルス及び未知のウイルスを除去及び不活化できるかが安全対策上重要である。ウイルス・プロセスバ
リデーションを実施する目的は、血漿分画製剤の製造工程に導入されているウイルス除去及び不活化技術
が、期待された効果をもたらしているか否かを実験的に検証することである。ウイルスの大きさ、形状、
脂質膜の有無、核酸の種類(DNA 型、RNA 型)、耐熱性などの特性を踏まえて適切なモデルウイルスを選択
2
21
1.2 対象
本ガイドラインは国内で使用される全ての原血漿、中間原料、及び製品に適用し、安全性確保対策の対
象とするウイルスは、「生物由来原料基準」(平成 15 年厚生労働省告示第 210 号)の「第2 血液製剤総
則」の「2 血漿分画製剤総則」において検査対象とされているB型肝炎ウイルス(HBV)
、C 型肝炎ウイ
ルス(HCV)及びヒト免疫不全ウイルス(HIV)に加え、健康被害をもたらす可能性が指摘され血液に混入
リスクのあるその他のウイルスも含むものとする。
1.2 対象
本ガイドラインは国内で使用されるすべての原料血漿及び製品に適用し、安全性確保対策の対象とする
ウイルスは、当分の間、ヒト免疫不全ウイルス(HIV)、C 型肝炎ウイルス(HCV)及び B 型肝炎ウイルス(HBV)
とする。
1.3 感染性因子
1.3 感染性因子
血漿分画製剤はヒトの血液を原料として製造されることから、血液を介して伝播するウイルスに対する
血漿分画製剤は人間の血液を原料として製造されることから、血液を介して伝播するウイルスに対する
十分な対策を講じなければならない。現在、HBV、HCV 及び HIV 等に係る高い感度のスクリーニング検査や 十分な対策を講じなければならない。現在ではスクリーニング検査、ウイルス除去及び不活化処理が実施
製造工程でのウイルス除去及び不活化処理が実施されており、血漿分画製剤の安全性は格段に向上してい されており、血漿分画製剤の安全性は格段に向上しているが、血液を介したウイルス感染の歴史的経過を
る。一方、血液を介したウイルス感染の歴史的経過を顧みると、ウイルス肝炎についての報告や 1980 年代 顧みると、ウイルス肝炎についての報告もあり、また、1980 年代の血漿分画製剤による HIV 感染も記憶に
の血漿分画製剤による HIV や HCV 感染があったことに加え、その後も国内外で複数の新興・再興感染症の 新しいところである。感染性ウイルスで現在までに明らかになっているものにはヒト免疫不全ウイルス
発症が報告されている。血漿分画製剤の安全性確保の上で問題になりうる主なウイルスとして、B 型肝炎 (HIV)、A 型肝炎ウイルス(HAV)、B 型肝炎ウイルス(HBV)、C 型肝炎ウイルス(HCV)、そしてパルボウイルス
ウイルス(HBV)、C 型肝炎ウイルス(HCV)
、ヒト免疫不全ウイルス(HIV)のほか、A 型肝炎ウイルス(HAV)、 B19 などがある。血漿分画製剤は、多くの人の血漿をプールして製造されるため、十分に検出ができない
E 型肝炎ウイルス(HEV)
、ヒトパルボウイルス B19 などが挙げられる。さらに血漿分画製剤は、多くのヒ ウイルスや未知のウイルスなどが潜在している可能性があり、安全対策を徹底して実施する必要がある。
トの血漿をプールして製造されるため、検査対象とされていないウイルスや未知のウイルスなどが潜在し さらに、原料血液以外の材料、例えば、製造工程で使用する酵素やモノクローナル抗体を用いて製造する
ている可能性があり、安全対策を徹底して実施する必要がある。例えば、新興感染症として新たなウイル 場合における動物由来のウイルス汚染の可能性や製造環境からのウイルス汚染の可能性も推定されるこ
スが出現した場合、原料となる血液に混入するリスクが否定できない場合はウイルス検査の必要性につい とから、注意深く安全対策を講ずることが必要である。
て検討するとともに、製造工程での十分なウイルスクリアランスが得られるか評価する必要がある。さら
に、原血漿以外の材料、例えば、動物由来の酵素やモノクローナル抗体を用いて製造する場合における動
物由来のウイルス汚染の可能性や製造環境からのウイルス汚染の可能性も推定されることから、注意深く
安全対策を講ずることが必要である。
1
序論
1.4 安全性確保の基本
血漿分画製剤のウイルスに対する安全対策は、次に示す複数の方法を適切かつ相補的に行うことにより
達成される。
(1)献(供)血者の問診を行う。
(2)献(供)血血液、ミニプール血漿又はプール血漿のウイルス検査を行う。
(3)製造工程でウイルス除去及び不活化処理を実施する。
(4)必要に応じて、製造工程でのウイルス検査を実施する。
(5)原血漿に関する最新の感染症情報を採血事業者等より入手するよう努める。
(6)採血後情報及び輸血後情報について遡及調査を行う。
(7)製品との関連が疑われる感染症の情報を集める。
1.4 安全性確保の基本
血漿分画製剤のウイルスに対する安全対策は、次に示す複数の方法を適切かつ相補的に行うことにより
達成される。
(1) 献(供)血者の問診を行う。
(2) 血漿のウイルス検査を実施する。
(3) 製造工程でウイルス除去及び不活化処理を実施する。
(4) 最終製品のウイルス検査を実施する。
(5) 採血後情報及び輸血後情報について遡及調査を行う。
1.5 検査の限界
ウイルスの検査方法は技術の進歩とともに向上するため、検査の実施に当たっては常に科学的に最高水
準の検査技術を取り入れるとともに適切に検査を行わなければならない。いかなる検査にも検出限界が存
在するため、ウイルス検査の結果が陰性であっても、ウイルスの存在を完全に否定できないこともある。
また、血液中には検査対象とされていないウイルスや未知のウイルスの存在も考えられる。したがって、
現在採用している検査技術には検出限界のあることを認識し、プールした血漿を原料として製造される血
漿分画製剤は、ウイルスが潜在する可能性を常に有することを前提とした上で安全対策を講ずる必要があ
る。
1.5 検査の限界
ウイルスの検査方法は技術の進歩とともに向上するため、検査の実施に当たっては常に科学的に最高水
準の検査技術を取り入れるとともに適切に検査を行われなければならない。いかなる検査にも検出限界が
存在するため、ウイルス検査の結果が陰性であっても、ウイルスの存在を完全に否定できないこともある。
また、血液中には未知のウイルスの存在も考えられる。したがって、現在採用している検査技術には検出
限界のあることを認識し、プールした血漿を原料として製造される血漿分画製剤は、ウイルスが潜在する
可能性を常に有することを前提とした上で安全対策を講ずる必要がある。
1.6 ウイルスクリアランス試験の役割
原料の血液には常にウイルスが潜在する可能性があることを前提にすると、製造工程においていかに既
知及び未知のウイルスを除去又は不活化できるかが安全対策上重要である。ウイルスクリアランス試験を
実施する目的は、血漿分画製剤の製造工程に導入されているウイルス除去技術及び不活化技術が、期待さ
れた効果をもたらしているか否かを実験的に検証することである。
(改行)
ウイルスクリアランス試験においては、ウイルスの大きさ、形状、脂質膜(エンベロープ)の有無、核
1.6 ウイルス・プロセスバリデーションの役割
原料の血液には常にウイルス潜在の可能性のあることを前提にすると、製造工程においていかに既知の
ウイルス及び未知のウイルスを除去及び不活化できるかが安全対策上重要である。ウイルス・プロセスバ
リデーションを実施する目的は、血漿分画製剤の製造工程に導入されているウイルス除去及び不活化技術
が、期待された効果をもたらしているか否かを実験的に検証することである。ウイルスの大きさ、形状、
脂質膜の有無、核酸の種類(DNA 型、RNA 型)、耐熱性などの特性を踏まえて適切なモデルウイルスを選択
2
21