よむ、つかう、まなぶ。
04 資料1-2_ワクチンの研究開発について (24 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_43850.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会研究開発及び生産・流通部会(第36回 9/25)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
開発優先度の高いワクチンの開発要請を依頼
健感発1216第1号
平成25年12月16日
一般社団法人日本ワクチン産業協会 理事長 殿
厚生労働省健康局結核感染症課長
開発優先度の高いワクチンの研究開発について(開発要請)
平素より、予防接種行政の運営に多大なご協力をいただき、厚く御礼申し上げます。
さて、平成25年10月31日に開催された第5回厚生科学審議会予防接種・ワクチン分科会研究開発及び生産・流通部会に
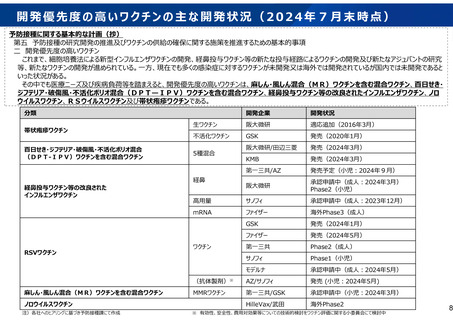
おいて、開発優先度の高いワクチンとして、①麻しん・風しん混合(MR)ワクチンを含む混合ワクチン、②百日せき・ジフテリア・
破傷風・不活化ポリオ混合(DPT-IPV)ワクチンを含む混合ワクチン、③経鼻投与ワクチン等の改良されたインフルエンザ
ワクチン、④ノロウイルスワクチン、⑤RSVワクチン及び⑥帯状疱疹ワクチンが選定されました。
また、同年11月28日に開催された第6回同部会において、百日せき・ジフテリア・破傷風・不活化ポリオ混合(DPT-
IPV)ワクチンを含む混合ワクチンの開発に当たっての留意事項として、初回接種の接種時期については、現在のHibワクチン
(生後2月~7月に開始し、20日から56日の間隔をおいて3回)にあわせる形で検討すべきとの方針が示されました。
上記の検討結果を踏まえ、貴会所属の会員企業に対し、これらのワクチンの開発を要請いたしますので、周知をお願いいたします。
なお、開発する混合ワクチンの接種時期については、必要に応じ、個別にご相談いただきますようお願いいたします。
今後とも、予防接種行政へのご理解及びご協力をいただきますよう、よろしくお願いいたします。
24
健感発1216第1号
平成25年12月16日
一般社団法人日本ワクチン産業協会 理事長 殿
厚生労働省健康局結核感染症課長
開発優先度の高いワクチンの研究開発について(開発要請)
平素より、予防接種行政の運営に多大なご協力をいただき、厚く御礼申し上げます。
さて、平成25年10月31日に開催された第5回厚生科学審議会予防接種・ワクチン分科会研究開発及び生産・流通部会に
おいて、開発優先度の高いワクチンとして、①麻しん・風しん混合(MR)ワクチンを含む混合ワクチン、②百日せき・ジフテリア・
破傷風・不活化ポリオ混合(DPT-IPV)ワクチンを含む混合ワクチン、③経鼻投与ワクチン等の改良されたインフルエンザ
ワクチン、④ノロウイルスワクチン、⑤RSVワクチン及び⑥帯状疱疹ワクチンが選定されました。
また、同年11月28日に開催された第6回同部会において、百日せき・ジフテリア・破傷風・不活化ポリオ混合(DPT-
IPV)ワクチンを含む混合ワクチンの開発に当たっての留意事項として、初回接種の接種時期については、現在のHibワクチン
(生後2月~7月に開始し、20日から56日の間隔をおいて3回)にあわせる形で検討すべきとの方針が示されました。
上記の検討結果を踏まえ、貴会所属の会員企業に対し、これらのワクチンの開発を要請いたしますので、周知をお願いいたします。
なお、開発する混合ワクチンの接種時期については、必要に応じ、個別にご相談いただきますようお願いいたします。
今後とも、予防接種行政へのご理解及びご協力をいただきますよう、よろしくお願いいたします。
24