よむ、つかう、まなぶ。
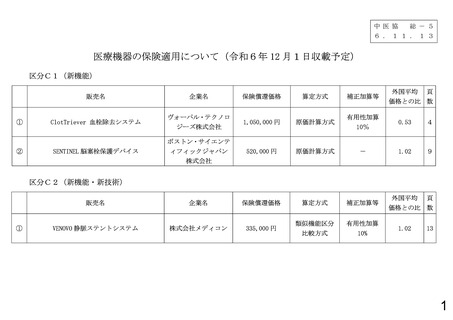
総-5医療機器、臨床検査及びPETの保険適用について (24 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_45183.html |
| 出典情報 | 中央社会保険医療協議会 総会(第598回 11/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
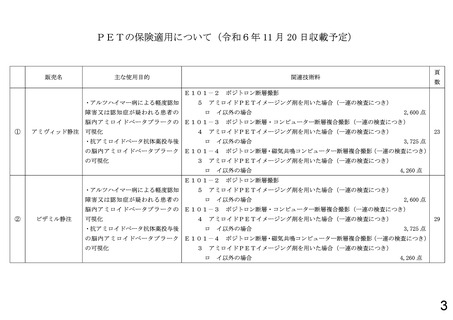
使用推進ガイドラインに沿って、アルツハイマー病による軽度認知障
害又は軽度の認知症が疑われる患者等に対し、レカネマブ(遺伝子組換
え)製剤効能又は効果としてアルツハイマー病による軽度認知障害及
び軽度の認知症の進行抑制を有する医薬品の投与の要否を判断する目
的でアミロイド β 病理を示唆する所見を確認する場合に、患者1人に
つき1回に限り算定する。ただし、レカネマブ(遺伝子組換え)製剤効
能又は効果としてアルツハイマー病による軽度認知障害及び軽度の認
知症の進行抑制を有する医薬品の投与中止後に初回投与から 18 か月を
超えて再開する場合は、さらに1回に限り算定できる。なお、この場合
においては、本撮影が必要と判断した医学的根拠を診療報酬明細書の
摘要欄に記載すること。
イ 略
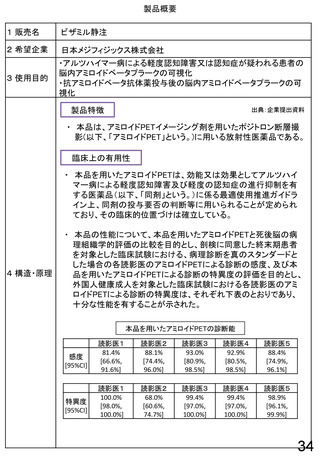
ウ 「5」の「ロ」イ以外の場合のうち、上記アの場合については、効能
又は効果として、アルツハイマー病による軽度認知障害又は認知症が
疑われる患者の脳内アミロイドベータプラークの可視化に用いるもの
として薬事承認を得ているアミロイドPETイメージング剤を使用し
た場合に限り算定する。なお、アミロイドPETイメージング剤の注入
に係る費用は所定点数に含まれ、別に算定できない。
エ 「5」の「ロ」イ以外の場合については、効能又は効果としてアルツ
ハイマー病による軽度認知障害及び軽度の認知症の進行抑制を有する
医薬品に係る厚生労働省の定める最適使用推進ガイドラインに沿って、
効能又は効果としてアルツハイマー病による軽度認知障害及び軽度の
認知症の進行抑制を有する医薬品の投与終了の可否を検討する場合及
び 18 か月を超える投与継続の可否を検討する場合は、それぞれの場合
につき、さらに1回に限り算定できる。
オ 「5」の「ロ」イ以外の場合のうち、上記エの場合については、効能
又は効果として、抗アミロイドベータ抗体薬投与後の脳内アミロイド
ベータプラークの可視化に用いるものとして薬事承認を得ているアミ
ロイドPETイメージング剤を使用した場合に限り算定する。なお、ア
ミロイドPETイメージング剤の注入に係る費用は所定点数に含まれ、
別に算定できない。
カ レカネマブ(遺伝子組換え)製剤の投与の要否を判断する目的で、
「E101-3」ポジトロン断層・コンピューター断層複合撮影(一連
の検査につき)の「4」アミロイドPETイメージング剤を用いた場合
(一連の検査につき)又は「E101-4」ポジトロン断層・磁気共鳴
コンピューター断層複合撮影(一連の検査につき)の「3」アミロイド
PETイメージング剤を用いた場合(一連の検査につき)を併せて実施
した場合には、主たるもののみ算定する。
(7)~(8) 略
24
害又は軽度の認知症が疑われる患者等に対し、レカネマブ(遺伝子組換
え)製剤効能又は効果としてアルツハイマー病による軽度認知障害及
び軽度の認知症の進行抑制を有する医薬品の投与の要否を判断する目
的でアミロイド β 病理を示唆する所見を確認する場合に、患者1人に
つき1回に限り算定する。ただし、レカネマブ(遺伝子組換え)製剤効
能又は効果としてアルツハイマー病による軽度認知障害及び軽度の認
知症の進行抑制を有する医薬品の投与中止後に初回投与から 18 か月を
超えて再開する場合は、さらに1回に限り算定できる。なお、この場合
においては、本撮影が必要と判断した医学的根拠を診療報酬明細書の
摘要欄に記載すること。
イ 略
ウ 「5」の「ロ」イ以外の場合のうち、上記アの場合については、効能
又は効果として、アルツハイマー病による軽度認知障害又は認知症が
疑われる患者の脳内アミロイドベータプラークの可視化に用いるもの
として薬事承認を得ているアミロイドPETイメージング剤を使用し
た場合に限り算定する。なお、アミロイドPETイメージング剤の注入
に係る費用は所定点数に含まれ、別に算定できない。
エ 「5」の「ロ」イ以外の場合については、効能又は効果としてアルツ
ハイマー病による軽度認知障害及び軽度の認知症の進行抑制を有する
医薬品に係る厚生労働省の定める最適使用推進ガイドラインに沿って、
効能又は効果としてアルツハイマー病による軽度認知障害及び軽度の
認知症の進行抑制を有する医薬品の投与終了の可否を検討する場合及
び 18 か月を超える投与継続の可否を検討する場合は、それぞれの場合
につき、さらに1回に限り算定できる。
オ 「5」の「ロ」イ以外の場合のうち、上記エの場合については、効能
又は効果として、抗アミロイドベータ抗体薬投与後の脳内アミロイド
ベータプラークの可視化に用いるものとして薬事承認を得ているアミ
ロイドPETイメージング剤を使用した場合に限り算定する。なお、ア
ミロイドPETイメージング剤の注入に係る費用は所定点数に含まれ、
別に算定できない。
カ レカネマブ(遺伝子組換え)製剤の投与の要否を判断する目的で、
「E101-3」ポジトロン断層・コンピューター断層複合撮影(一連
の検査につき)の「4」アミロイドPETイメージング剤を用いた場合
(一連の検査につき)又は「E101-4」ポジトロン断層・磁気共鳴
コンピューター断層複合撮影(一連の検査につき)の「3」アミロイド
PETイメージング剤を用いた場合(一連の検査につき)を併せて実施
した場合には、主たるもののみ算定する。
(7)~(8) 略
24