よむ、つかう、まなぶ。
総-5医療機器、臨床検査及びPETの保険適用について (37 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_45183.html |
| 出典情報 | 中央社会保険医療協議会 総会(第598回 11/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
る。
[参考]
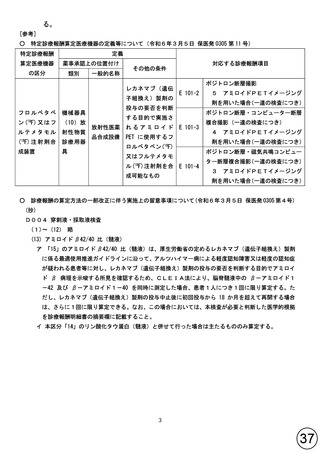
○ 特定診療報酬算定医療機器の定義等について(令和6年3月5日 保医発 0305 第 11 号)
定義
特定診療報酬
算定医療機器
薬事承認上の位置付け
の区分
類別
一般的名称
レカネマブ(遺伝
子組換え)製剤の
フロルベタベ
18
(10)放
ルテメタモル
射性物質
18
( F) 注 射 剤 合
診療用器
成装置
具
ポジトロン断層撮影
E 101-2
れるアミロイド
品合成設備
PET に使用するフ
E 101-3
4
アミロイドPETイメージング
ポジトロン断層・磁気共鳴コンピュー
又はフルテメタモ
成可能なもの
複合撮影(一連の検査につき)
剤を用いた場合(一連の検査につき)
ロルベタベン(18F)
ル(18F)注射剤を合
アミロイドPETイメージング
ポジトロン断層・コンピューター断層
する目的で実施さ
放射性医薬
5
剤を用いた場合(一連の検査につき)
投与の要否を判断
機械器具
ン ( F) 又 は フ
対応する診療報酬項目
その他の条件
E 101-4
ター断層複合撮影(一連の検査につき)
3
アミロイドPETイメージング
剤を用いた場合(一連の検査につき)
○ 診療報酬の算定方法の一部改正に伴う実施上の留意事項について(令和6年3月5日 保医発 0305 第4号)
(抄)
D004 穿刺液・採取液検査
(1)~(12) 略
(13) アミロイド β42/40 比(髄液)
ア 「15」のアミロイド β42/40 比(髄液)は、厚生労働省の定めるレカネマブ(遺伝子組換え)製剤
に係る最適使用推進ガイドラインに沿って、アルツハイマー病による軽度認知障害又は軽度の認知症
が疑われる患者等に対し、レカネマブ(遺伝子組換え)製剤の投与の要否を判断する目的でアミロイ
ド β 病理を示唆する所見を確認するため、CLEIA法により、脳脊髄液中の β-アミロイド1
-42 及び β-アミロイド1-40 を同時に測定した場合、患者1人につき1回に限り算定する。た
だし、レカネマブ(遺伝子組換え)製剤の投与中止後に初回投与から 18 か月を超えて再開する場合
は、さらに1回に限り算定できる。なお、この場合においては、本検査が必要と判断した医学的根拠
を診療報酬明細書の摘要欄に記載すること。
イ 本区分「14」のリン酸化タウ蛋白(髄液)と併せて行った場合は主たるもののみ算定する。
3
37
[参考]
○ 特定診療報酬算定医療機器の定義等について(令和6年3月5日 保医発 0305 第 11 号)
定義
特定診療報酬
算定医療機器
薬事承認上の位置付け
の区分
類別
一般的名称
レカネマブ(遺伝
子組換え)製剤の
フロルベタベ
18
(10)放
ルテメタモル
射性物質
18
( F) 注 射 剤 合
診療用器
成装置
具
ポジトロン断層撮影
E 101-2
れるアミロイド
品合成設備
PET に使用するフ
E 101-3
4
アミロイドPETイメージング
ポジトロン断層・磁気共鳴コンピュー
又はフルテメタモ
成可能なもの
複合撮影(一連の検査につき)
剤を用いた場合(一連の検査につき)
ロルベタベン(18F)
ル(18F)注射剤を合
アミロイドPETイメージング
ポジトロン断層・コンピューター断層
する目的で実施さ
放射性医薬
5
剤を用いた場合(一連の検査につき)
投与の要否を判断
機械器具
ン ( F) 又 は フ
対応する診療報酬項目
その他の条件
E 101-4
ター断層複合撮影(一連の検査につき)
3
アミロイドPETイメージング
剤を用いた場合(一連の検査につき)
○ 診療報酬の算定方法の一部改正に伴う実施上の留意事項について(令和6年3月5日 保医発 0305 第4号)
(抄)
D004 穿刺液・採取液検査
(1)~(12) 略
(13) アミロイド β42/40 比(髄液)
ア 「15」のアミロイド β42/40 比(髄液)は、厚生労働省の定めるレカネマブ(遺伝子組換え)製剤
に係る最適使用推進ガイドラインに沿って、アルツハイマー病による軽度認知障害又は軽度の認知症
が疑われる患者等に対し、レカネマブ(遺伝子組換え)製剤の投与の要否を判断する目的でアミロイ
ド β 病理を示唆する所見を確認するため、CLEIA法により、脳脊髄液中の β-アミロイド1
-42 及び β-アミロイド1-40 を同時に測定した場合、患者1人につき1回に限り算定する。た
だし、レカネマブ(遺伝子組換え)製剤の投与中止後に初回投与から 18 か月を超えて再開する場合
は、さらに1回に限り算定できる。なお、この場合においては、本検査が必要と判断した医学的根拠
を診療報酬明細書の摘要欄に記載すること。
イ 本区分「14」のリン酸化タウ蛋白(髄液)と併せて行った場合は主たるもののみ算定する。
3
37